Questões de Concurso
Sobre transformações químicas e energia em química
Foram encontradas 1.458 questões
O.uando 0,5 mol de etanol líquido sofre combustão sob pressão constante, produzindo CO2 e H2O gasosos, a energia liberada é de 148 kcal. Na combustão de 3,00 mols de etanol, nas mesmas condições, será de________ e a entalpia dos produtos, em relação à dos reagentes, é______________
Uma transformação química será exotérmica quando a quantidade de energia__________ na__________ das ligações entre os átomos dos reagentes for menor do que a quantidade de energia________ na __________das ligações entre os átomos dos produtos.
I. Dióxido de carbono sólido (gelo seco) → dióxido de carbono gasoso.
II. Ferro fundido → ferro sólido.
III. Água líquida → vapor d'água.
Dessas transformações, no sentido indicado e à temperatura constante, apenas:
H2S + l2 → S + 2 Hl,
as variações dos números de oxidação do enxofre e do iodo são, respectivamente:
A reação apresentada é exotérmica.
Dados: Valor enérgico em kJ . g-1: proteínas e carboidratos = 17 ; lipídios = 38 Energia de ligação em kJ . mol -1 : C – H : 412 ; O = O : 496 ; C = O : 743 ; H – O : 463
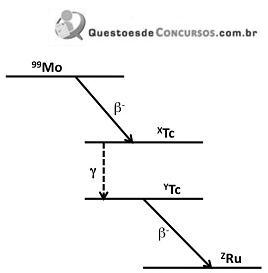
Assinale a alternativa que apresenta os valores corretos para X, Y e Z, respectivamente.
I. Quanto maior o número atômico de átomos radioativos, maior a probabilidade de emissão espontânea de partículas alfa.
II. Para que ocorra decaimento alfa, o valor da energia de desintegração deve ser positivo.
III. Devido à conservação do momento linear, como a massa do núcleo-filho é muito maior que a da partícula alfa, ela carrega quase toda a energia cinética.
É correto o que se afirma em
A equação química acima descreve a queima do gás metano, uma reação de combustão muito utilizada na indústria. A partir dessas informações, julgue os itens a seguir.
apresentado abaixo:

H2 O2 (aq) → H2 O(L) + ½ O2 (g),
é uma reação de oxirredução na qual o elemento
A corrosão química somente ocorre em meio aquoso, uma vez que há transferência de elétrons no meio.
A corrosão eletroquímica é um processo espontâneo no qual acontecem, simultaneamente, reações anódicas e catódicas.
A corrosão química ocorre apenas em metais.
