Questões de Concurso Para petroquímica suape
Foram encontradas 618 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
E° Ag+1 /Ago = + 0,80 V
E° Cu+2 /Cuo = + 0,34 V
Sobre a pilha, conclui-se que ela funciona de maneira espontânea e que
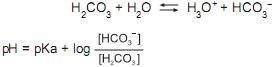
Sobre o equilíbrio de um sistema contendo 100 mL de solução 0,1 mol/L de H 2CO3 e 0,1 mol/L de HCO3– , quando se adiciona(m)
No meio aquoso, esses dois sais reagem instantaneamente, de acordo com a equação balanceada abaixo, e nela se forma um sal muito pouco solúvel.

A quantidade máxima, em gramas, de AgCL sólido (massa molar = 143,5 g/mol e Kps = 10-10 ) que se forma é de, aproximadamente,

Se, no frasco Erlenmeyer, há 25,00 mL de HCL(aq) 0,200 mol/L, o volume de NaOH(aq) 0,100 mol/L que deve escoar da bureta, em mL, até se atingir o ponto estequiométrico, é

