Questões de Concurso
Para professor - química
Foram encontradas 4.164 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
(Dados: C=12; H=1; O=16)
Assinale a alternativa que corresponde a reação de combustão do propano e a velocidade desta reação.
I. 2 MnO₂(s) + H₂O(ℓ) + 2 e⁻ → Mn₂O₃(s) + 2 OH⁻(aq)
II. Zn(s) + 2 OH- (aq) → ZnO(s) + H₂O(ℓ) + 2 e⁻
I. Os químicos admitem que, ao se chocarem, as moléculas transformam parte de sua energia cinética em potencial, adquirindo, o conjunto resultante do choque, alta energia potencial. Este conjunto forma um composto intermediário, chamado complexo ativado.
II. O complexo ativado representa um estado instável que se chama estado de transição. Esse estado de transição comum à reação direta e à inversa.
III. Ao romper-se, o complexo pode tanto ocasionar a formação dos produtos como a recuperação dos reagentes. Em outras palavras, só conseguem formar o complexo ativado as moléculas com energia cinética mínima necessária que se choquem adequadamente.
Estão corretas as afirmativas:
I. 2 MnO2(s) + H2O(ℓ) + 2 e⁻ → Mn2O3(s) + 2 OH⁻(aq)
II. Zn(s) + 2 OH- (aq) → ZnO(s) + H2O(ℓ) + 2 e⁻
As pilhas alcalinas começaram a ser produzidas no Brasil em 1978. A diferença básica entre essa pilha e a de Zn-C é que a primeira emprega célula eletroquímica com materiais ativos de maior grau de pureza. As pilhas alcalinas são mais resistentes a altas temperaturas, oferecem maior segurança contra vazamentos e duram de quatro a dez vezes mais que as Zn-C dependendo do uso. (https://www.scielo.br acesso em 16/04/2023)
Entre as vantagens dessa nova pilha está o fato de não ocorrer a formação de gases durante o processo redox, eliminando-se, portanto, os riscos de explosões. Sabendo-se que o potencial padrão de redução, E°, do zinco e do manganês, nos processos I e II, é -1,25 V e + 0,29 V, respectivamente, calcule a voltagem produzida pela pilha.
2HCl (aq) + CaCO3 (s) → CaCl2 (aq) + H2O (l) + CO2 (g)
Pensando nas condições normais de temperatura e pressão (CNTP), vamos calcular a massa de água, em gramas, e o volume de gás carbônico, que pode se formar a partir de 80g de carbonato de cálcio. Dados as massas atômicas de Ca= 40; C = 12; O=16. Assinale a alternativa que apresenta os valores encontrados.
O Regulamento Técnico SVS/MS nº 540/1997 considera o fermento químico como um aditivo, e como tal, necessita obrigatoriamente ser registrado na ANVISA de acordo com as orientações da Resolução nº 23 (ANVISA, 2000).
Basicamente, os fermentos químicos são constituídos de uma mistura de pirofosfato ácido de sódio, bicarbonato de sódio e fécula de mandioca. Além do conhecido bicarbonato de sódio, assinale a alternativa que apresente alguns ácidos que podem fazer parte da composição.
I. As ligações químicas nos compostos orgânicos podem ser do tipo s ou p . A ligação s é formada pela interação de dois orbitais atômicos, segundo o eixo que une os dois átomos, ao passo que na ligação p, a interação dos orbitais atômicos se faz segundo o plano que contém o eixo da ligação.
II Neste composto orgânico podemos encontrar 2 ligações s e 6 ligações p.
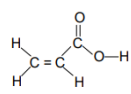
III. Neste composto orgânico podemos encontrar 3 ligações s e 6 ligações p.
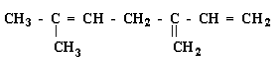
Estão corretas as afirmativas:
( ) É um tipo particular de ligação entre moléculas que possuem átomos de hidrogênio ligados a átomos de flúor, oxigênio ou nitrogênio.
( ) Nas pontes de hidrogênio, os elementos são muito eletronegativos e possuem pequenos raios atômicos, neste caso, fazendo com que o par de elétrons fique muito atraído pelo elemento mais eletronegativo, gerando dipolos (+) e (-) bastante intensos.
( ) As moléculas H2O ; NH3 ; HF são exemplos de ligações com formação de pontes de hidrogênio.
Assinale a alternativa que apresenta a sequência correta de cima para baixo.
I. Sabemos que as moléculas polares são aquelas que têm regiões ou polos de carga elétricas diferentes. Isto pode ser explicado pela diferença de eletronegatividade entre os ligantes. Costuma-se afirmar que as moléculas assimétricas são polares e que as moléculas simétricas são apolares, quando se refere justamente a de densidade eletrônica.
PORQUE
II. Elementos diferentes têm, geralmente, eletronegatividades diferentes, com isso, haverá regiões de densidades eletrônicas diferentes que não serão compensadas umas pelas outras.
Assinale a alternativa correta.
Em relação aos elementos químicos mencionados anteriormente, analise as afirmativas abaixo. ]
I. Os ametais citados pertencem ao grupo dos calcogênios e ao grupo dos halogênios, possuindo seis e sete elétrons no subnível mais energético respectivamente.
II. Todos os metais citados pertencem ao quarto período da classificação periódica e possuem elétrons distribuídos em quatro camadas eletrônicas.
III. Existem na relação acima dois ametais que apresentam propriedades semelhantes às do oxigênio, pois possuem o mesmo número de elétrons na camada de valência.
IV. Todos os metais citados são elementos de transição e apresentam na camada de valência elétrons distribuídos no subnível d.
Estão corretas as afirmativas:
I. Alta temperatura de fusão e ebulição.
II. Boa condutividade elétrica em solução aquosa.
III. Mau condutor de eletricidade no estado sólido.
IV. Com exceção do grafite, não conduzem corrente elétrica, se encontrados puros.
Estão corretas as afirmativas:
( ) Sommerfeld propõe que a energia do elétron seria determinada pela distância em que ele se encontra do núcleo e pelo tipo de órbita que descreve.
( ) Hantaro Nagaoka, em 1903, sugeriu um modelo atômico formado por pares de cargas positivas e negativas, aos quais chamou de “dinamidas”. E estes pares de cargas ficariam em blocos flutuantes no espaço.
( ) Em 1904, Philipp Lénard publicou no Japão uma descrição do carbono, bem moderna para época, ele sugeriu que o átomo era constituído de um anel de elétrons ao redor de um centro muito denso.
Assinale a alternativa que apresenta a sequência correta de cima para baixo.
I. O físico inglês J. J. Thomson, em 1887, mostrou que as partículas em raio catódico são carregadas negativamente e ele provou esta afirmação mostrando que o raio pode ser desviado se passar entre placas de metais carregados opostamente em um tudo de Crookes. Segundo suas pesquisas, a direção do desvio para a placa carregada positivamente, mostra que as partículas do raio catódico carregam uma carga elétrica negativa.
II. Segundo os pesquisadores dos modelos atômicos, foi no ano de 1908, que Robert Millikan, um físico americano realizou, um clássico experimento, que foi capaz de determinar a magnitude da carga negativa do elétron. Millikan acreditava que os raios x chocavam-se com os elétrons das moléculas do ar que circundavam as gotículas de óleo e que as gotículas poderiam captar estes elétrons. Através de seus experimentos, Milikan foi assim capaz de mostrar que todos os elétrons são idênticos, isto é, todos têm a mesma massa e carga.
III. Embora para a maioria dos cientistas da época o fato do átomo ser constituído por uma parte carregada positivamente e por alguns elétrons, em 1890, isto ainda não era totalmente claro. Em 1898, que J. J. Thomson sugeriu que um átomo poderia ser uma esfera carregada positivamente na qual alguns elétrons estão incrustados. Segundo ele, isto levaria a uma impossível remoção de elétrons dos átomos.
Estão corretas as afirmativas:
I. Maus-tratos envolvendo seus alunos.
II. Reiteração de faltas injustificadas e de evasão escolar, esgotados os recursos escolares.
III. Elevados níveis de repetência.
IV. Atrasos constantes e imprudência sem justificativa.
Estão corretas as afirmativas:
Art. 245. Deixar o médico, professor ou responsável por estabelecimento de ______ à saúde e de ensino fundamental, pré-escola ou creche, de comunicar à autoridade competente os casos de que tenha ______, envolvendo suspeita ou confirmação de maus-tratos contra criança ou adolescente: Pena - multa de ______ a vinte salários de referência, aplicando-se o dobro em caso de reincidência.
(Estatuto da Criança e do Adolescente e dá outras providências. Artigo 245 do Capítulo II - Das Infrações Administrativas encontrado na L8069 (planalto.gov.br) )
Assinale a alternativa que preencha correta e respectivamente as lacunas.
( ) Evitar situações, durante a formação dos alunos em grupo, de confronto dos seus pontos de vista, de debate de opiniões, para não comprometer o roteiro elaborado para a atividade.
( ) Estimular o compartilhamento de informações e opiniões. Planejar um espaço para que os alunos possam relatar o que compreenderam da proposta e comparar as próprias ideias.
( ) Elaborar critérios de rendimento e ação educativa em conjunto com os demais professores para ampliar as possibilidades concretas de explorar o trabalho em grupo.
( ) Estimular a interação decidindo por estratégias que possibilitem a ajuda mútua, a solidariedade, a colaboração, o afeto construindo a socialização.
Assinale a alternativa que apresenta a sequência correta de cima para baixo.