Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
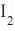 para cada quilograma de álcool, será de
para cada quilograma de álcool, será de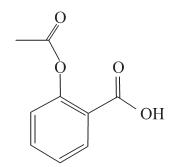
Na hidrólise da aspirina é formada uma substância que está presente no vinagre e também o ácido salicílico, que tem fórmula molecular
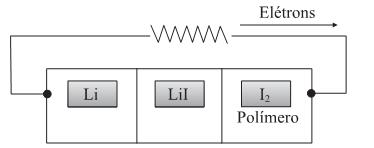
Para esta pilha, são dadas as semi-reações de redução:

São feitas as seguintes afirmações sobre esta pilha:
I. No ânodo ocorre a redução do íon Li + .
II. A ddp da pilha é + 2,51 V.
III. O cátodo é o polímero/iodo.
IV. O agente oxidante é o
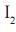 .
.São corretas as afirmações contidas apenas em
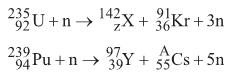
Nas equações, Z, X, A e o tipo de reação nuclear são, respectivamente,
Os compostos da função álcool são de grande importância, tanto pelo uso direto quanto pela utilidade na preparação de outros compostos orgânicos. O álcool isopropílico ou propan-2- ol, por exemplo, é usado para limpar componentes eletrônicos, pois seu baixíssimo teor de água praticamente não promove processos de oxidação.
Sobre esse composto são feitas as seguintes afirmativas:
I. É um álcool secundário que, ao ser oxidado, dá origem à propanona, conhecida comercialmente como acetona.
II. Sua composição centesimal é idêntica à do metoxi-etano, que é seu isômero funcional.
III. Por ter uma molécula simétrica, apresenta isomeria geométrica.
IV. Apresenta um carbono assimétrico e, portanto, tem atividade ótica.
As afirmativas corretas são, apenas,
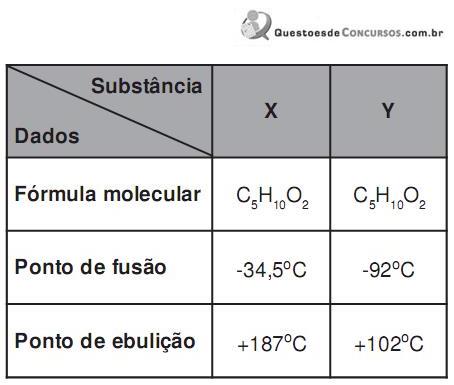
I. A substância X é o ácido carboxílico e a Y é o éster.
II. O éster é o único que apresenta cadeia carbônica homogênea.
III. As estruturas planas das substâncias X e Y são idênticas.
IV. O ácido apresenta maior ponto de ebulição em função das ligações de hidrogênio.
Analisadas as informações, conclui- se que estão corretas apenas as afirmativas
• Os sólidos foram misturados com água, em recipientes separados, e verificou- se que o de número 2 não dissolveu.
• As duas soluções obtidas foram testadas em relação à condutibilidade elétrica, e apenas a obtida pela dissolução do sólido número 3 resultou condutora.
Os resultados permitem concluir que os sólidos 1, 2 e 3 são, respectivamente,
Com base nessas informações, é correto afirmar que
Com base nessas informações, é correto afirmar que
Três amostras líquidas, identificadas pelas letras A, B e C, foram testadas por meio de indicadores ácido- base. Os resultados são apresentados no quadro a seguir:
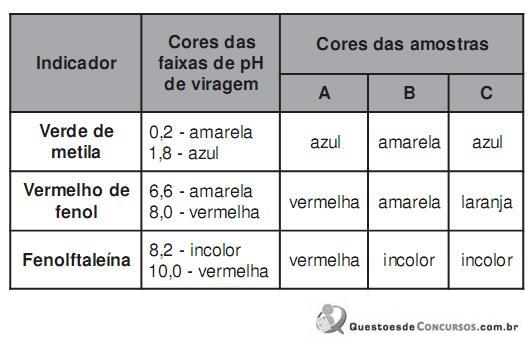
A análise dos resultados permite concluir que as amostras A, B e C são, respectivamente,
“Grande parte do interesse pelo sal, como os experimentos dos antigos chineses com o salitre, visava proporcionar aos militares métodos mais eficientes de detonar coisas e gente. No século XIX, descobriu- se que o clorato de potássio produzia uma explosão maior que a pólvora tradicional, o nitrato de potássio. E o magnésio tinha propriedades explosivas ainda mais impressionantes.”
KURLANSKY, Mark. Sal: uma história do mundo.
São Paulo: SENAC, 2004. p. 291.
O sal que produzia maior explosão provém da reação entre as substâncias de fórmulas


Essa frase fica correta quando as lacunas I, II e III são preenchidas, respectivamente, por:
