Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
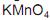 em meio de ácido sulfúrico a quente.
em meio de ácido sulfúrico a quente.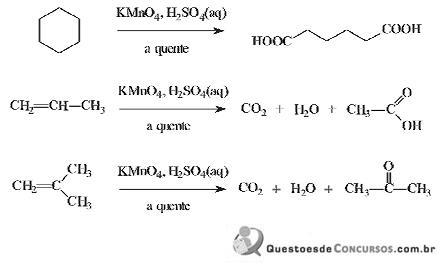
As amostras X, Y e Z são formadas por substâncias puras de fórmula
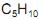 . Utilizando- se
. Utilizando- se 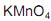 em meio de ácido sulfúrico a quente, foi realizada a oxidação enérgica de alíquotas de cada amostra. A substância X formou o ácido
em meio de ácido sulfúrico a quente, foi realizada a oxidação enérgica de alíquotas de cada amostra. A substância X formou o ácidopentanodióico, a substância Y gerou o ácido acético e a propanona, enquanto
que a substância Z produziu gás carbônico, água e ácido butanóico. As amostras X, Y e Z contêm, respectivamente,
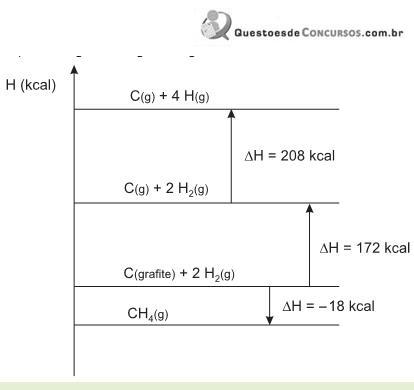
Os valores das energias de ligação H--H e C -- H obtidas a partir do diagrama são, respectivamente,
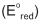
Em um estudo eletroquímico foram montadas 4 pilhas a partir de 4 pares redox distintos. Em todos os dispositivos o cátodo era constituído de uma solução aquosa de íons
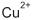 de concentração 1,0 mol/L e um eletrodo de cobre metálico. O ânodo era constituído de um metal ( M ), diferente em cada dispositivo,
de concentração 1,0 mol/L e um eletrodo de cobre metálico. O ânodo era constituído de um metal ( M ), diferente em cada dispositivo,imerso em solução do respectivo cátion
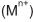 também de concentração 1,0mol/L.
também de concentração 1,0mol/L.A figura a seguir representa esquematicamente o aparato experimental.
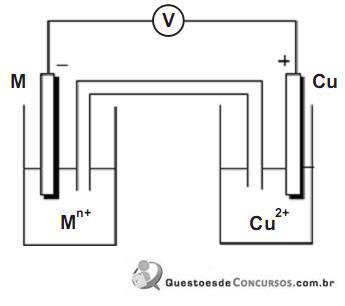
Os metais utilizados como ânodo foram zinco, níquel, chumbo e ferro. Em cada experimento foram determinadas a ddp inicial da pilha e a quantidade de carga gerada pela pilha durante a corrosão de 1,00 g do ânodo. Nestas condições, pode- se dizer que o ânodo cuja pilha apresenta a maior ddp e o ânodo cuja pilha gera a maior quantidade de carga são formados, respectivamente, pelos metais
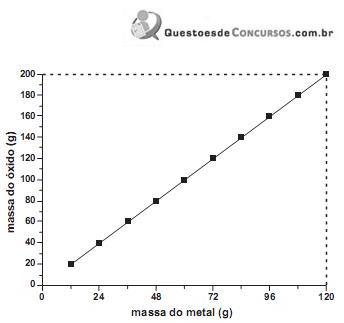
Durante um experimento, realizado em recipiente fechado, foi colocado para reagir 1,00 g do referido metal, obtendo-se 1,40 g do seu óxido. Considerando-se que todo o oxigênio presente no frasco foi consumido, pode-se determinar que a massa de oxigênio presente no sistema inicial é x . Em outro recipiente fechado, foram colocados 1,50 g do referido metal em contato com 1,20 g de oxigênio. Considerando que a reação ocorreu até o consumo total de pelo menos um dos reagentes, pode- se afirmar que amassa de óxido gerado é y . Sabendo que ometal emquestão forma apenas um cátion estável e considerando que em todas as reações o rendimento foi de 100 %, os valores de x e y são, respectivamente,
Um técnico de laboratório distraído preparou solições de carbonato de potássio (K2CO3),
hidróxido de sódio (NaOH) e de hidróxido de cálcio (Ca(OH)2), colocando- se em três frascos não rotulados ( frascos X, Y E Z ).
Para identificar as soluções, um aluno misturou, em três tubos de ensaio distintos,
amostras de cada frasco com solução aquosa de ácido clorídrico. Nada foi observado nas soluções dos frascos X e Z, mas ocorreu uma efervenscência no
tuboque continha a solução do frasco Y.
Em seguida, o aluno combinou, dois a dois, os conteúdos de cada frasco ( frasco X, Y e Z ) em tubos de ensaios limpos.
Observou que só houve formação de precipitado quando misturou as soluções dos frascos X e Y.
Assinale a alternativa que identifica corretamente o conteúdo dos frascos X, Y e Z.
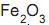 e impurezas. Ao se misturar 4,0 g de uma amostra deste minério com ácido clorídrico concentrado, obtêm- se 6,5 g de cloreto de ferro III. A porcentagem em massa de
e impurezas. Ao se misturar 4,0 g de uma amostra deste minério com ácido clorídrico concentrado, obtêm- se 6,5 g de cloreto de ferro III. A porcentagem em massa de 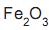 no minério é igual a
no minério é igual a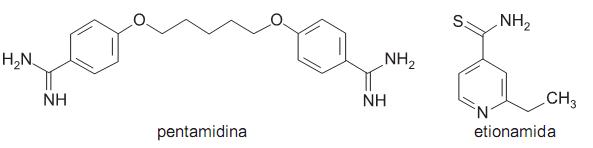
Sobre estas duas substâncias, é CORRETO afirmar que:
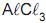 , a quantidade de eletricidade, em Coulomb, necessária para produzir 21,6 g de alumínio metálico é igual a:
, a quantidade de eletricidade, em Coulomb, necessária para produzir 21,6 g de alumínio metálico é igual a: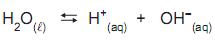
O produto iônico da água é
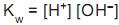 , cujo valor é 1 x
, cujo valor é 1 x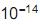 a 25 °C. Ao se adicionar 1,0 mL de NaOH 1,0 mol/L (base forte) a um copo bécher contendo 99 mL de água pura, o pH da solução será aproximadamente igual a
a 25 °C. Ao se adicionar 1,0 mL de NaOH 1,0 mol/L (base forte) a um copo bécher contendo 99 mL de água pura, o pH da solução será aproximadamente igual a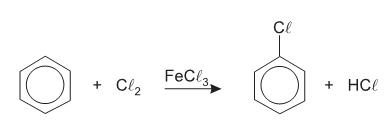
De acordo com esta reação, é CORRETO afirmar que:
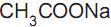 ) e ácido acético (
) e ácido acético (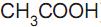 ). O pH desse tampão pode variar de 4,0 a 5,4 de acordo com a proporção dessa mistura.
). O pH desse tampão pode variar de 4,0 a 5,4 de acordo com a proporção dessa mistura. Sobre o tampão acetato, é ERRADO afirmar que:
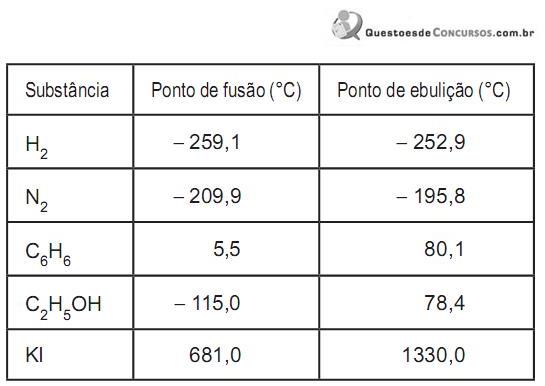
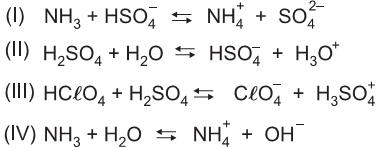
De acordo com a teoria ácido-base de Brönsted-Lowry, é CORRETO afirmar que:
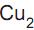 e CuO) se forma na superfície dos tachos, podendo se desprender e ser incorporado ao doce.
e CuO) se forma na superfície dos tachos, podendo se desprender e ser incorporado ao doce. Sobre o cobre e seus óxidos, é CORRETO afirmar que:
I – HCl(g) + NH 3(g) → NH4 Cl(s) (ácido clorídrico no estado gasoso reage com amônia no estado gasoso dando origem a cloreto de amônio no estado sólido).
II –CO2(g) + H2O(l) → H2 CO3(aq) (dióxido de carbono no estado gasoso reage com a água no estado líquido e dá origem a ácido carbônico em meio aquoso).
III – AgNO3(aq) + KI(aq) → Agl(s) + KNO3(aq) (solução aquosa de nitrato de prata reage com solução aquosa de iodeto de potássio formando iodeto de prata no estado sólido e nitrato de potássio insolúvel em água).
É correto APENAS o que se afirma em:
O pH da solução final é: