Questões Militares
Sobre equilíbrio químico em química
Foram encontradas 197 questões
Ag+ (aq) + e-
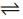 Ag(c); Eo = 0,799 e AgCl (c) + e-
Ag(c); Eo = 0,799 e AgCl (c) + e- 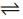 Ag(c) Cl- (aq); E = 0,222 V
Ag(c) Cl- (aq); E = 0,222 Vem que ο Eo é o potencial do eletrodo em relação ao eletrodo padrão de hidrogênio nas condições-padrão.
H2O(g) + C(s) + 31,4 kcal ⇄ CO(g) + H2(g)
pode-se afirmar que:
Considerando-se que a primeira ionização do H2SO4 seja praticamente completa e a segunda, parcial, é correto concluir que o pH da água do lago, após a contaminação pelo ácido, atinge valor inferior a 4,0.
Caso o acidente em questão tenha ocorrido em um dia frio, com a temperatura da água a 5 ºC, é correto concluir que, no instante imediatamente anterior ao derramamento, o pH da água do lago era superior a 7,0.
Dados: Kw = 10-14 (mol · L-1)2
Solução do frasco I: ficou rosa em fenolftaleína e amarela no metilorange.
Solução do frasco II: permaneceu incolor em fenolftaleína e vermelha no metilorange.
Solução do frasco III: permaneceu incolor em fenolftaleína e amarela no metilorange.
Sabe-se que a fenolftaleína, em pH acima de 9 apresenta coloração vermelha, enquanto que, em pH abaixo desse valor, é incolor. Sabe-se ainda que o metilorange apresenta coloração vermelha em pH abaixo de 3,5 e amarela em pH acima deste valor.
Sendo assim, os estudantes chegaram à conclusão de que os frascos I, II e III contêm, respectivamente, solução de
A 25 °C, três frascos (I, II e III) contêm, respectivamente, soluções aquosas 0,10 mol L−1 em acetato de sódio, em cloreto de sódio e em nitrito de sódio.
Assinale a opção que apresenta a ordem crescente CORRETA de valores de pHx (x = I,II e III) dessas soluções, sabendo que as constantes de dissociação (K) , a 25 °C, dos ácidos clorídrico (HCl) , nitroso (HNO2) e acético (CH3COOH) , apresentam a seguinte relação:
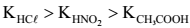
Entretanto, dados experimentais de Ka e Kb não estão de acordo com esta estrutura mas, sim, com *NH3CHRCOO¯. Com relação aos aminoácidos e seus
grupos ácidos e básicos, é correto afirmar que:
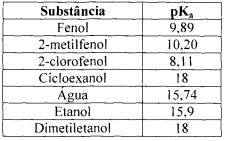
Com base nos valores apresentados no quadro, assinale a alternativa correta.

I. a reação direta representada em (a) é a mais espontânea.
II. a reação representada em (c) apresenta maior constante de equilíbrio.
III. a reação inversa mais espontânea é aquela representada em(b).
IV. no equilíbrio, a menor concentração de Cl2(g) será em (c).
V. no equilibrio, o produto em maior concentração é o da reação (a).
Das afirmações acima, são verdadeiras:
I. Segundo o princípio de Le Châtelier a adição de H+ ao sistema tampão faz liberar mesma quantidade de OH-.
II. O sistema tampão funciona no sistema digestivo, mas não no sistema sanguíneo.
III. Por adição do sal à solução do ácido para formar o tampão, a percentagem de dissociação do ácido diminui.
IV. A solução tampão sofre pequena variação de pH quando a ela são adicionados íons H+ ou OH-.
Uma solução aquosa saturada em fosfato de estrôncio [Sr3(PO4)2] está em equilíbrio químico à temperatura de 25 °C, e a concentração de equilíbrio do íon estrôncio, nesse sistema, é de 7,5 x 10–7 mol L–1.
Considerando-se que ambos os reagentes (água e sal inorgânico) são quimicamente puros, assinale a alternativa CORRETA com o valor do pKPS(25ºC) do Sr3(PO4)2.
Dado: KPS = constante do produto de solubilidade.
Em cinco béqueres foram adicionados 50 mL de uma solução de referência, que consiste de uma solução aquosa saturada em cloreto de prata, contendo corpo de fundo, a 25 °C e 1 atm. A cada béquer, foram adicionados 50 mL de uma solução aquosa diluída diferente, dentre as seguintes:
I. Solução de cloreto de sódio a 25 °C.
II. Solução de Glicose a 25 °C.
III. Solução de Iodeto de sódio a 25 °C.
IV. Solução de Nitrato de prata a 25 °C.
V. Solução de Sacarose a 50 °C.
Considere que o corpo de fundo permanece em contato com as soluções após rápida homogeneização das
misturas aquosas e que não ocorre formação de óxido de prata sólido. Nestas condições, assinale a opção que
indica a(s) solução(ões), dentre as acima relacionadas, que altera(m) a constante de equilíbrio da solução de
referência.
Uma barra de ferro e um fio de platina, conectados eletricamente a um voltímetro de alta
impedância, são parcialmente imersos em uma mistura de soluções aquosas de FeSO4 (1,0 mol L–1) e HCl isenta de oxigênio. Um fluxo de gás hidrogênio é mantido constante sobre a parte imersa da superfície da
platina, com pressão nominal (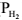 ) de 1,0 atm, e a força eletromotriz medida a 25 °C é igual a 0,292 V.
) de 1,0 atm, e a força eletromotriz medida a 25 °C é igual a 0,292 V.
Considerando-se que ambos os metais são quimicamente puros e que a platina é o polo positivo do elemento galvânico formado, assinale a opção CORRETA que apresenta o valor calculado do pH desse meio aquoso.
Dados: 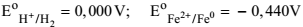
Uma solução aquosa de HCl 0,1 mol L–1 foi titulada com uma solução aquosa de NaOH 0,1 mol L–1. A figura ao lado apresenta a curva de titulação obtida em relação à condutância da solução de HCl em função do volume de NaOH adicionado.
Com base nas informações apresentadas nesta figura, assinale a opção ERRADA.