Questões Militares
Sobre equilíbrio químico em química
Foram encontradas 200 questões
Com relação ao equilíbrio das reações químicas, analise as afirmativas abaixo.
I - A expressão matemática da constante de equilíbrio (K) relaciona as concentrações de reagentes e produtos no equilíbrio.
II - Os efeitos da perturbação de um equilíbrio químico são previstos pelo Princípio de Le Chatelier.
III- Quando o valor da constante de equilíbrio for grande (K muito maior que 1), a reação é favorável aos reagentes e as concentrações dos produtos no equilíbrio são menores que as dos reagentes.
Assinale a opção correta.
0 hidróxido de sódio (NaOH),também conhecido como soda cáustica, é muito utilizado na indústria como base química na fabricação de papel, tecidos e detergentes. Um técnico em química necessita saber o valor do pH de uma solução aquosa de NaOH, a qual será utilizada na fabricação de um grande lote de detergentes. Para tanto, recebeu uma amostra de 500mL da solução aquosa que contém 0,700g de NaOH. Qual o valor do pH da solução aquosa de NaOH?
Dados:
Constante de ionização da água
(Ka) = [H+ ] [OH-] = 1,0 . 10-14
[H+ ] : concentração do íon H+
[OH- ] : concentração do íon OH-
log (2,9) = 0,46 e log(3,5) = 0,54
O cloreto de chumbo II é ligeiramente solúvel em água, conforme descrito na equação química abaixo.
PbCl2(s)  Pb2+(aq) + 2Cl-(aq)
Pb2+(aq) + 2Cl-(aq)
Sabendo que a concentração do íon chumbo, na solução saturada, é de 0,02 mol/L, qual é o valor do produto de solubilidade do cloreto de chumbo II?
Dados:
Produto de solubilidade
(Kps) : Kps = [Pb2+] [ Cl- ] 2
[Pb2+ ] : concentração do íon Pb2+
[Cl-] : concentração do íon Cl-
Marque a opção correta.
Para a reação representada abaixo, a constante de equilíbrio, Keq, é descrita como:

Considere as duas reações representadas a seguir:
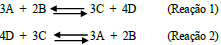
Se Keq para a reação 1 é igual a 0,1, qual é o Keq para a reação 2?
Marque a opção correta.
A dissociação do ácido acético em água ocorre de acordo com a seguinte equação:

Ao adicionar acetato de sódio ao sistema representado acima, supõe-se que o(s) efeito(s) observado(s) é(são):
I. pH diminui.
II. pH aumenta.
III. pKa diminui.
IV. pKa aumenta.
N2(g) + O2(g) ⇌ 2NO(g) K1 2NO(g) + O2(g) ⇌ 2NO2(g) K2
NO2(g) ⇌ 1/2 N2(g) + O2(g) K3
A análise dos dados termodinâmicos de reações permite a previsão da espontaneidade. Na tabela a seguir estão apresentados os dados termodinâmicos de duas reações químicas.
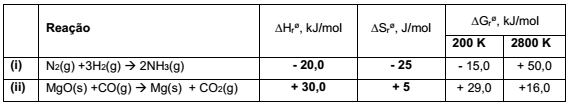
A partir dos dados apresentados, identifique as seguintes afirmativas como verdadeiras (V) ou falsas (F):
( ) A diminuição da temperatura desfavorece a espontaneidade da reação (i).
( ) O aumento da temperatura favorece a espontaneidade da reação (ii).
( ) Na temperatura de 400 K, a reação (i) será espontânea.
( ) Na temperatura de 4000 K, a reação (ii) será espontânea.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
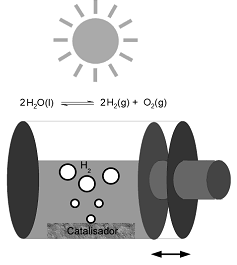
Recentemente, a produção fotocatalítica de hidrogênio vem atraindo atenção devido ao processo que gera um combustível limpo, o qual é utilizado em células a combustível. O processo se baseia na separação da água nos seus componentes, conforme equilíbrio inserido no esquema, utilizando luz solar e um fotocatalisador (p. ex. NaTaO3:La). O processo é extremamente endotérmico, necessitando 1,23 eV para ocorrer. Num experimento, o processo foi realizado num sistema fechado, como esquematizado abaixo. Considerando essas informações, identifique as afirmativas a seguir como verdadeiras (V) ou falsas (F):
( ) A quantidade de fotocatalisador limita a conversão.
( ) O aumento da temperatura irá favorecer a conversão.
( ) A diminuição do volume do sistema irá favorecer a conversão.
( ) É condição necessária para a produção de hidrogênio que o fotocatalisador absorva energia solar superior a 1,23 eV.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
A biodegradação da matéria orgânica produz substâncias húmicas, nas quais os principais componentes são os ácidos húmicos. Estes correspondem a diversas estruturas complexas, que possuem na maioria substituintes fenólicos (pKa = 8) e carboxílicos (pKa = 4). Além de alterar o pH do meio, também são capazes de se ligar a íons metálicos formando coloides. Sobre esse tema, considere as seguintes afirmativas:
1. A presença de substâncias húmicas torna o pH menor que 7. 2. A presença de substâncias húmicas ligadas a íons metálicos é detectada pelo turvamento do meio.
3. O valor medido de pH 6 em uma amostra indica que praticamente todos os substituintes fenólicos estão protonados, enquanto que os substituintes carboxílicos estão desprotonados.
4. O valor medido de pH 4 em uma amostra indica que 50% dos substituintes carboxílicos estão protonados.
Assinale a alternativa correta.
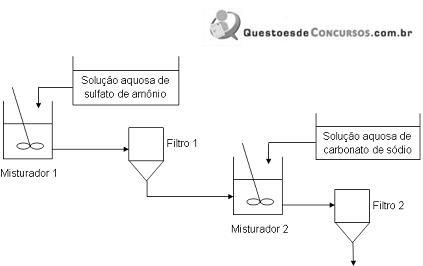
No Misturador 1, antes da adição de 100 mL de uma solução aquosa de sulfato de amônio 20 g/L, encontram-se 100 mL de uma solução aquosa composta por massas iguais de nitrato de prata, nitrato cúprico e nitrato de chumbo (II), de concentração total 60 g/L.
Ao Misturador 2, que contém o material passante do Filtro 1, adicionam-se 100 mL de uma solução aquosa de carbonato de sódio 40 g/L e uma pequena quantidade de uma solução de hidróxido de sódio objetivando o adequado ajuste do pH de precipitação para, em seguida, proceder a filtração. Sobre os produtos de filtração, pode se dizer que:
I – solução cuja [H+ ] = 10-7 mol/L
II – solução de HCl cuja concentração é 10-7 mol/L
São valores do pH das soluções, respectivamente:
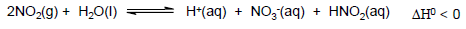
Num ensaio em laboratório, foram acondicionados num sistema fechado N2(g), O2(g), NO2(g) e vapor de água que está em equilíbrio com água líquida. A partir desses dados, considere as seguintes afirmações:
1. O aumento na pressão total do sistema tenderá a diminuir o pH da solução dentro do sistema.
2. Um aquecimento brando tenderá a aumentar o pH da solução dentro do sistema.
3. A adição de excesso de água líquida no sistema tenderá a deslocar o equilíbrio, diminuindo o pH da solução dentro do sistema.
4. A contribuição do ácido nitroso (HNO2) para o pH da solução dentro do sistema é desprezível.
Assinale a alternativa correta
Dado Kps(MX) = 5 x 10─12.
São feitas as seguintes comparações de valores de pKa de compostos orgânicos:
I. pKa (CH3COOH) > pKa (CℓCH2COOH)
II. pKa (F3CCOOH) > pKa (Cℓ3CCOOH)
III. pKa (CH3CH2CHCℓCOOH) > pKa (CH3CHCℓCH2COOH)
Das comparações acima, está(ão) CORRETA(S) apenas