Questões Militares
Sobre equilíbrio químico em química
Foram encontradas 196 questões
Considerando que: - a solução básica foi parcialmente neutralizada pela solução do ácido; - o ácido clorídrico é um ácido forte (α=100%); - o hidróxido de sódio é uma base forte (α=100%).
O pH da mistura resultante dessa reação de neutralização é
Dado: log 4 = 0,60
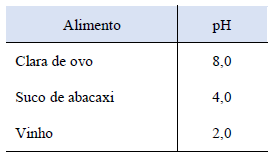
Com base nas informações da tabela abaixo, assinale a alternativa CORRETA.
“Quando um eletrólito é adicionado à água, independentemente se a solubilidade é alta ou baixa, ocorre a sua dissociação (liberação de íons) ou ionização (produção de íons). Porém, ao mesmo tempo, esses íons voltam a formar o eletrólito, ocorrendo um equilíbrio químico de dissolução.”
(Produto de solubilidade - Manual da Química (manualdaquimica.uol.com.br). Acesso em: 15/02/2018).
Considere os carbonatos apresentados na tabela abaixo e seus respectivos valores da constante de produto de solubilidade (Kps) a 25°C.

A partir dos dados da tabela, foram feitas as seguintes afirmações sobre as solubilidades molares.
I. Carbonato de zinco é mais solúvel do que carbonato de cádmio.
II. Carbonato de zinco é mais solúvel do que carbonato de prata.
III. Carbonato de prata é mais solúvel do que carbonato de cádmio.
É verdadeiro o que se afirma em:
A figura abaixo demonstra a típica curva de titulação de uma substância.
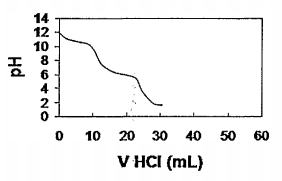
Que substância é indicada na figura acima?
Considere a seguinte substância:

Com relação à reação abaixo, considerando a tabela acima e o pH da água igual a 7,00, assinale a opção correta.
CH3NH2(aq) + H2O(I) ⇄ CH3NH+3(aq) + OH-(aq)
Analise a seguinte reação.
2NO2(g) ⇄ N2O4(g) ΔH = -57,2 kJ/mol
Na reação acima, o equilíbrio se desloca para a esquerda
quando, considerando conjuntamente os efeitos da
compressão e temperatura sobre o sistema:
Quando se dissolvem ácidos fortes em um solvente muito básico, como a água, ocorre a ionização completa desses ácidos e fica impossível comparar a força relativa dos mesmos. Para se evitar esse efeito, chamado de Efeito Nivelador da água, é comum dissolver ácidos fortes em um solvente menos básico, como o ácido acético, sendo possível, assim, comparar a força relativa de ácidos fortes. A esse respeito são dadas, abaixo, as equações de dissociação do HCIO4 e HCI em CH3COOH:
1) HCIO4 + CH3COOH → CH3COOH2- + CIO4- pK1 = 4,88
2) HCI + CH3COOH → CH3COOH2+ + Cl- pK2 =8,55
Com relação á Teoria de ácidos e bases de Bronsted-Lowry
e com base nas equações acima, assinale a opção
INCORRETA.
CONSTANTES
Constante de Avogadro (NA) = 6,02 x 1023 mol-1
Constante de Faraday (F) = 9,65 x 104 C mol-1 = 9,65 x 104 A s mol-1 = 9,65 x 104 J V-1 mol-1
Volume molar de gás ideal = 22.4 L (CNTP)
Carga elementar = 1,602 x 10-19 C
Constante dos gases (R) = 8,21 x 10-2 atm L K -1 mol-1 = 8,31JK-1 mol-1 = 1,98 cal K-1 mol-1 =
= 62,4 mmHg L K-1 mol-1
Constante gravitacional (g) = 9,81 m s-2
Constante de Planck (h) = 6,626 x 10-34 m2kg s-1
Velocidade da luz no vácuo = 3,0x 108 ms-1
Número de Euler (e) = 2,72
DEFINIÇÕES
Pressão: 1 atm = 760mmHg = 1,01325 x 105 N m-2 = 760 Torr = 1,01325 bar
Energia: 1 J = 1N m = 1 kg m2 s-2
Condições normais de temperatura e pressão (CNTP): 0°C e 760 mmHg
Condições ambientes: 25° C e 1 atm
Condições padrão: 1 bar; concentração das soluções = 1 mol L-1 (rigorosamente: atividade unitária das espécies); sólido com estrutura cristalina mais estável nas condições de pressão e temperatura em questão.
(s) = sólido. (L) = líquido, (g) = gás. (aq) = aquoso. (CM) = circuito metálico, (conc) = concentrado.
(ua) = unidades arbitrárias. [X] = concentração da espécie química X em mol L-1

CONSTANTES
Constante de Avogadro (NA) = 6,02 x 1023 mol-1
Constante de Faraday (F) = 9,65 x 104 C mol-1 = 9,65 x 104 A s mol-1 = 9,65 x 104 J V-1 mol-1
Volume molar de gás ideal = 22.4 L (CNTP)
Carga elementar = 1,602 x 10-19 C
Constante dos gases (R) = 8,21 x 10-2 atm L K -1 mol-1 = 8,31JK-1 mol-1 = 1,98 cal K-1 mol-1 =
= 62,4 mmHg L K-1 mol-1
Constante gravitacional (g) = 9,81 m s-2
Constante de Planck (h) = 6,626 x 10-34 m2kg s-1
Velocidade da luz no vácuo = 3,0x 108 ms-1
Número de Euler (e) = 2,72
DEFINIÇÕES
Pressão: 1 atm = 760mmHg = 1,01325 x 105 N m-2 = 760 Torr = 1,01325 bar
Energia: 1 J = 1N m = 1 kg m2 s-2
Condições normais de temperatura e pressão (CNTP): 0°C e 760 mmHg
Condições ambientes: 25° C e 1 atm
Condições padrão: 1 bar; concentração das soluções = 1 mol L-1 (rigorosamente: atividade unitária das espécies); sólido com estrutura cristalina mais estável nas condições de pressão e temperatura em questão.
(s) = sólido. (L) = líquido, (g) = gás. (aq) = aquoso. (CM) = circuito metálico, (conc) = concentrado.
(ua) = unidades arbitrárias. [X] = concentração da espécie química X em mol L-1

Considere dadas as constantes de dissociação ácida (Ka) ou básica (Kb) das seguintes substâncias, a 25°C: fenol (C6H5OH), Ka= 1 x 10-10 e anilina (C6H5NH2), Kb = 7 x 10-10.
Sobre o pH de soluções aquosas dessas substâncias são feitas as seguintes afirmações:
I. A solução aquosa de fenol a 1 x 10-4 mol L-1 tem pH<5.
II. A solução aquosa de anilina a 1 x 10-4 mol L-1 tem pH>9.
III. Ambas as soluções aquosas a 1 x 10-4 mol L-1 têm pH aproximadamente iguais.
Das afirmações acima está(ão) CORRETA(S)
CONSTANTES
Constante de Avogadro (NA) = 6,02 x 1023 mol-1
Constante de Faraday (F) = 9,65 x 104 C mol-1 = 9,65 x 104 A s mol-1 = 9,65 x 104 J V-1 mol-1
Volume molar de gás ideal = 22.4 L (CNTP)
Carga elementar = 1,602 x 10-19 C
Constante dos gases (R) = 8,21 x 10-2 atm L K -1 mol-1 = 8,31JK-1 mol-1 = 1,98 cal K-1 mol-1 =
= 62,4 mmHg L K-1 mol-1
Constante gravitacional (g) = 9,81 m s-2
Constante de Planck (h) = 6,626 x 10-34 m2kg s-1
Velocidade da luz no vácuo = 3,0x 108 ms-1
Número de Euler (e) = 2,72
DEFINIÇÕES
Pressão: 1 atm = 760mmHg = 1,01325 x 105 N m-2 = 760 Torr = 1,01325 bar
Energia: 1 J = 1N m = 1 kg m2 s-2
Condições normais de temperatura e pressão (CNTP): 0°C e 760 mmHg
Condições ambientes: 25° C e 1 atm
Condições padrão: 1 bar; concentração das soluções = 1 mol L-1 (rigorosamente: atividade unitária das espécies); sólido com estrutura cristalina mais estável nas condições de pressão e temperatura em questão.
(s) = sólido. (L) = líquido, (g) = gás. (aq) = aquoso. (CM) = circuito metálico, (conc) = concentrado.
(ua) = unidades arbitrárias. [X] = concentração da espécie química X em mol L-1

Com base nas informações obtidas pelo aluno, por meio do experimento descrito acima, indique a alternativa que apresenta uma conclusão INCORRETA a respeito deste experimento.
Dadas as seguintes equações que representam supostas reações químicas irreversíveis em meio aquoso e temperaturas moderadas:
I) 6 HBr + 2 Al → 2 AlBr3 + 3 H2
II) H2SO4 + BaCl2 → BaSO4 + 2 HCl
III) 2 KOH + NiSO4 → Ni(OH)2 + K2SO4
IV) 2 HBr + K2S → 2 KBr + H2S
V) BaCl2 + Na2CO3 → BaCO3 + 2 NaCl
Pode-se afirmar que a reação:
A hidrazina é um composto químico cuja fórmula química é N2H4 . Ela é usada, entre outras aplicações, como propelente para satélites artificiais, para produção de produtos químicos da agricultura e como removedor de oxigênio de caldeira. Usualmente, uma de suas principais reações conhecidas é a liberação dos gases quentes, quando em contato com um oxidante.
Considere a reação:
2N2H4(l) + N2O4(l) ↔ 3N2(g) + 4H2O(g) ΔH = -1094KJ
Interpretando a reação acima, o equilíbrio da reação desloca-se no sentido dos produtos
A afirmativa a seguir contextualiza a questão. Leia‐a atentamente.
“A corrosão é a deterioração de um material, geralmente metálico, por ação química ou eletroquímica do meio ambiente associada ou não a esforços mecânicos.”
(GENTIL, V. corrosão. LTC. 6ª ed. 2012.)
Analise a reação a seguir com seus respectivos sentidos:
• Mn+ + e– → M (sentido 1).
• M → Mn+ + e– (sentido 2).
Considerando o princípio de Le Châtelier, o equilíbrio da reação será influenciado no sentido 1 de acordo com qual
alternativa?