Questões Militares Sobre química
Foram encontradas 2.062 questões

O composto 1 apresenta duas aminas terciárias.

O nome do composto 2 é etano-1,2-diol.
Na reação de dupla troca do (NH4)2SO4 com o CaCl2, um dos compostos gerados é o sulfato de cálcio, de fórmula CaSO4.
A partir das informações do texto apresentado, julgue o item a seguir, considerando que MH = 1,00 g/mol, MN = 14,00 g/mol, MO = 16,00 g/mol, MP = 31,00 g/mol e MS = 32,00 g/mol.
Considere que a obtenção do NH4H2PO4 se dê pela reação do
ácido fosfórico (H3PO4) com a amônia (NH3) em uma reação
com 100% de rendimento. Nesse caso, para a obtenção de
120 kg de NH4H2PO4, são necessários menos de 100 kg de
ácido fosfórico.
A partir das informações do texto apresentado, julgue o item a seguir, considerando que MH = 1,00 g/mol, MN = 14,00 g/mol, MO = 16,00 g/mol, MP = 31,00 g/mol e MS = 32,00 g/mol.
Os dois compostos apresentados no texto apresentam
ligações iônicas e ligações covalentes.
A partir das informações do texto apresentado, julgue o item a seguir, considerando que MH = 1,00 g/mol, MN = 14,00 g/mol, MO = 16,00 g/mol, MP = 31,00 g/mol e MS = 32,00 g/mol.
Em uma solução de NH4H2PO4, de concentração 12,0 g/L, a
concentração em quantidade de matéria do elemento fósforo
é maior que 0,1 mol/L.
A partir das informações do texto apresentado, julgue o item a seguir, considerando que MH = 1,00 g/mol, MN = 14,00 g/mol, MO = 16,00 g/mol, MP = 31,00 g/mol e MS = 32,00 g/mol.
O número de oxidação do fósforo no di-hidrogenofosfato de
amônio é uma unidade maior que o número de oxidação do
enxofre no (NH4)2SO4.
Os íons sulfato e amônio no composto (NH4)2SO4 têm geometrias tetraédricas.
Dados: fórmulas moleculares: metano: CH4; propano: C3H8; butano: C4H10; etanol: C2H6O; e metanol: CH4O.
Considerando a reação de combustão completa desses combustíveis, o que necessitará de maior quantidade de gás oxigênio por molécula de combustível é o
http://pibid-bio-uepg.blogspot.com/2013/08/as-funcoes-inorganicas-esua.html. Acesso em 09/06/2020. Adaptado.
A reação química descrita é:
AgNO3 + NaCl → AgCl + NaNO3
As substâncias X, Y e Z, descritas no texto, são denominadas, respectivamente,
http://www.crianca.mppr.mp.br/2020/03/233/ESTATISTICAS-Estupro-bate-recorde-e-maioria-das-vitimas-sao-meninas-de-ate-13-anos.html Acesso em 23/06/2020.
Para indicar a presença de esperma, que pode ser encontrado em um crime sexual, podem ser feitos dois testes simples em uma amostra recolhida do fluido biológico da vítima: uma reação utiliza o reativo de Florence, constituído por I2, KI e H2O; a outra, uma solução saturada de ácido pícrico (C6H3N3O7) em glicerina (C3H8O3). Nas duas reações, a presença do esperma é observada devido ao aparecimento de uma coloração amarelada. Embora exista a possibilidade de falsos positivos, estes testes podem ajudar a identificar indícios. A natureza das ligações químicas que formam as substâncias utilizadas nos testes permite classificá-las, respectivamente, como
ÂNGELIS, R. Descubra a importância da química forense. http://www.ung.br/noticias/descubra-importancia-da-quimica-forense. Acesso em 10/06/2020. Adaptado.
Dados: massas atômicas (u): H = 1, C = 12, N = 14 e O = 16.
A substância detectada possuía massa molecular 162; portanto, é possível saber que se tratava da
Três frascos foram encontrados sem rótulo na bancada de um laboratório. Um deles continha solução de KOH a 0,1 mol/L; o outro, solução de CaCl2 a 0,05 mol/L; e o outro, solução de CH3CH2COOH a 0,1 mol/L. Na tentativa de identificar a solução contida em cada um deles, um técnico usou volumes iguais das soluções dos frascos para medir a pressão de vapor sob mesma temperatura, utilizando um sistema adequado. Os resultados obtidos estão indicados pelos ponteiros dos manômetros nesta figura.
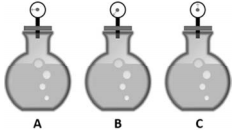
Com base nas informações e na figura apresentadas, é correto
afirmar que os frascos identificados por A, B e C contêm,
respectivamente, as soluções de
Em meados do século XX, as pilhas alcalinas surgiram como uma alternativa muito mais eficiente energeticamente em comparação às pilhas tradicionais. Como mostra a seguinte figura, a pilha alcalina utiliza os mesmos eletrodos da tradicional, porém o seu eletrólito é uma solução aquosa de hidróxido de sódio concentrada (~30% em massa) contendo uma dada quantidade de óxido de zinco ― daí a denominação alcalina para essa pilha.
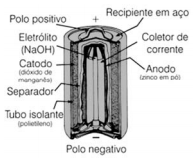
Internet:<http://qnesc.sbq.org.br> (com adaptações).
Uma mistura de carbonato de sódio decahidratado e bicarbonato de sódio foi colocada em um cadinho e levada a uma mufla a 350 °C por 3 h, tendo ocorrido as seguintes reações.
Na2CO3 · 10 H2O(s) → Na2CO3(s) + 10 H2O(v)
2 NaHCO3(s) → Na2CO3(s) + H2O(v) + CO2(g)
Finalizado o processo, restou unicamente carbonato de
sódio no cadinho, verificando-se uma perda total de massa de
6,70 g.
Sabendo que M(H) = 1 g/mol, M(C) = 12 g/mol,
M(O) = 16 g/mol e M(Na) = 23 g/mol, e supondo que a
quantidade de CO2 seco desprendido do cadinho seja igual a
2,20 g, assinale a opção que indica a quantidade, em gramas, de
Na2CO3 · 10 H2O existente na mistura inicial.
O gás propano, um dos componentes do gás de cozinha, pode ser preparado pela reação entre carvão — C(s) — e hidrogênio gasoso — H2(g).
C3H8(g) + 5 O2(g) → 3 CO2(g) + 4 H2O(l) ΔH° = −2.220 kJ
C(s) + O2(g) → CO2(g) ΔH° = −394 kJ
H2(g) + ½ O2(g) → H2O(l) ΔH° = −286 kJ
Com base nos calores de formação fornecidos, e sabendo-se que
M(H) = 1 g/mol, M(C) = 12 g/mol e M(O) = 16 g/mol, é correto
concluir que o módulo da variação de entalpia (ΔH1g) obtida na
preparação de 1 g de propano pelo processo citado, nas
condições padrão, é tal que
As aminas de cadeia curta, como as mostradas a seguir, possuem cheiro rançoso e desagradável, semelhante ao odor de peixe.
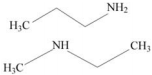
A intensidade do cheiro depende fundamentalmente da estrutura
da molécula, ainda que a fórmula molecular seja a mesma. Isso
decorre do fenômeno da isomeria, que, no caso das aminas em
apreço, é do tipo
Visando estudar o equilíbrio a seguir, um experimentador adicionou quantidades equimolares de tricloreto de fósforo e cloro gasoso em um reator a 180 °C.
PCl3(g) + Cl2(g) ⇌ PCl5(g)
Atingido o equilíbrio, foi verificada uma concentração de 1 x 10−4 mol/L de pentacloreto de fósforo.
Admitindo que, a 180 °C, a constante do equilíbrio em apreço
seja igual a 0,64, assinale a opção que indica a concentração de
cloro gasoso presente no equilíbrio.
Industrialmente, o PCl5 é sintetizado em reator fechado por meio da cloração do PCl3, de acordo com a equação química a seguir.
PCl3(g) + Cl2(g) ⇌ PCl5(g) ΔH = −124 kJ/mol
Conforme o princípio de Le Châtelier, o rendimento desse
processo pode ser aumentado