Questões Militares
Sobre transformações químicas e energia em química
Foram encontradas 361 questões
Considere a expansão de um gás ideal inicialmente contido em um recipiente de 1 L sob pressão de 10 atm. O processo de expansão pode ser realizado de duas maneiras diferentes, ambas à temperatura constante:
I. Expansão em uma etapa, contra a pressão externa constante de 1 atm, levando o volume final do recipiente a 10 L.
II. Expansão em duas etapas: na primeira, o gás expande contra a pressão externa constante de 5 atm até atingir um volume de 2 L; na segunda etapa, o gás expande contra uma pressão constante de 1 atm atingindo o volume final de 10 L.
Com base nestas informações, assinale a proposição CORRETA.
Considere as entalpias padrão de formação dos seguintes compostos:

Sabendo que a capacidade calorífica da água, à pressão constante, vale 75,9 J·mol-1 e que sua entalpia de vaporização é igual a 40,66 kJ·mol−1, assinale a alternativa que melhor corresponda ao número de mols de metano necessários para vaporizar 1 L de água pura, cuja temperatura inicial é 25°C, ao nível do mar.
Considere uma célula eletrolítica na forma de um tubo em H, preenchido com solução aquosa de NaNO3 e tendo eletrodos inertes mergulhados em cada ramo vertical do tubo e conectados a uma fonte externa. Num determinado instante, injeta-se uma solução aquosa de CuCrO4 verde na parte central do ramo horizontal do tubo. Após algum tempo de eletrólise, observa azul e uma amarela, separadas (em escala) de acordo com o esquema da figura.
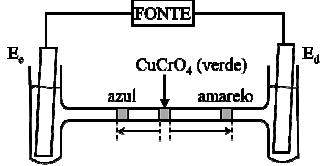
Com base nas informações do enunciado e da figura, assinale a opção ERRADA.
No estado padrão, é de 0,240 V o potencial da pilha cuja reação pode ser descrita pela seguinte equação química:
2 NO + ½ O2 + H2O → 2 HNO2.
Assinale a alternativa que apresenta o valor da energia livre padrão da reação, em kJ·mol-1.
Considere a reação descrita pela seguinte equação química:
H2(g, 1bar) + 2AgBr(s) → 2H+ (aq) + 2Br−(aq) + 2Ag(s).
Sendo X o potencial padrão (E°) da reação, o pH da solução a 25 °C quando o potencial da reação (E) for Y
será dado por
Observe o átomo de neptúnio representado a seguir:
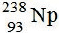
Após a emissão de uma partícula de acordo com Lei de Soddy, Fajans e Russel dá origem ao átomo de:
Considerando as reações a seguir:
 .
.
 ,
,
OΔH da reação a seguir é igual a:
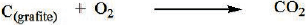 .
.
( ) No meio não aerado, o hidrogênio pode ficar adsorvido na superfície do catodo, polarizando a pilha formada com conseqüente redução do processo corrosivo.
( ) Se o oxigênio puder ser rápido e uniformemente fornecido a uma superfície metálica, é possível reparar fraturas que ocorram na película, diminuindo-se, assim, a velocidade de corrosão.
( ) O cobre tem uma velocidade de corrosão rápida em presença de ácidos não oxidantes, e em presença de oxigênio este vai funcionar como estimulador de corrosão.
( ) A corrosão eletroquímica será tanto mais intensa quanto maior o valor do pH.
( ) O cobre se mostra eficaz quando disperso em resina, geralmente epóxi, ou em silicatos inorgânicos ou orgânicos.
( ) No mecanismo de barreira, a eficiência da proteção depende da espessura do revestimento e da resistência das tintas ao meio corrosivo.
( ) No mecanismo de inibição, as tintas de fundo contêm determinados pigmentos inibidores que dão origem à formação de uma camada passiva sobre a superfície do metal, impedindo a sua passagem para a forma iônica.
Diferentes marcas de telefones celulares buscam ganhar novos clientes, anunciando que a bateria de seus aparelhos é mais eficiente que a dos concorrentes, por manterem o telefone celular ligado por mais tempo. Quando descarregada, a bateria do celular é conectada a uma rede elétrica para que sua carga seja restabelecida.
Esse processo é um exemplo de:
Observe as reações químicas a seguir.
H2O(I) → H2(g) + 1/2O2(g) Δh = +283 kJ
H2(g) + 1/2O2(g) → H2O(g) Δh = -242 kJ
Qual é o valor do calor de vaporização da água?
Observe a reação de oxirredução não balanceada a seguir.
Cu(s) + Ag+(aq) → Ag(s) + Cu2+(aq)
A soma de todos os coeficientes estequiométricos da reação
balanceada é :
O esquema abaixo, ilustra uma pilha eletroquímica conhecida como Pilha da Daniell.
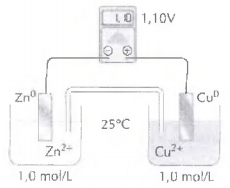
Assinale a opção correta com relação ao processo eletroquímico que ocorre na pilha de Daniell.
Observe a tabela a seguir.
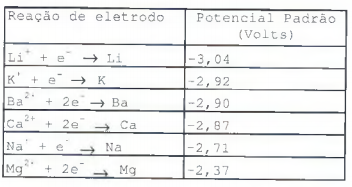
O potencial padrão de eletrodo é uma expressão quantitativa
da facilidade com que um elemento perde elétrons. A tabela
acima exibe valor do potencial padrão de eletrodos de metal.
Sendo assim, é correto afirmar que o agente redutor mais
forte do Cálcio é o: