Questões de Farmácia - Legislação em Farmácia para Concurso
Foram encontradas 2.936 questões
Ao analisar a Lei Federal nº 3.820/60, conseguimos definir algumas atribuições dos conselhos federal e regional de farmácia e a seguir estão listadas algumas dessas atribuições. Sendo assim, analise as atribuições dos Conselhos Regionais de Farmácia.
I. Registrar os profissionais de acordo com a presente lei e expedir a carteira profissional.
II. Examinar reclamações e representações escritas acerca dos serviços de registro e das infrações desta lei e decidir.
III. Deliberar sobre questões oriundas do exercício de atividades afins às do farmacêutico.
IV. Ampliar o limite de competência do exercício profissional, conforme o currículo escolar ou mediante curso ou prova de especialização realizados ou prestados em escola ou instituto oficial.
V. Dirimir dúvidas relativas à competência e âmbito das atividades profissionais farmacêuticas, com recurso suspensivo para o Conselho Federal.
Estão corretas apenas as afirmativas
Considere o procedimento abaixo, descrito na Farmacopeia Brasileira, 5ª edição (Anvisa, 2010), para o doseamento de cloridrato de pilocarpina (C11H16N2O2.HCl) matéria prima.
Pesar, exatamente, cerca de 2 g de amostra e dissolver em 60 mL de água. Titular com hidróxido de sódio M SV e determinar o ponto final potenciometricamente. Cada mL de hidróxido de sódio M SV equivale a 244,720 mg de C11H16N2O2.HCl.
O volume de hidróxido de sódio M SV a ser gasto na titulação de 2,1 g de cloridrato de
pilocarpina é
Um teste de uniformidade de doses unitárias foi realizado segundo o método geral 5.1.6 da Farmacopeia Brasileira, 5ª edição (Anvisa, 2010), e foram obtidos os seguintes valores:
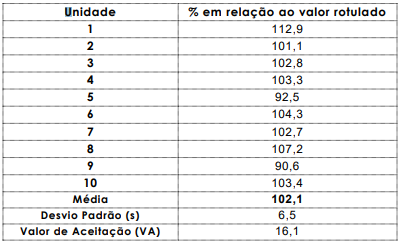
Com base nesses dados, conclui-se que
Considere a informação presente no texto abaixo.
Segundo a Farmacopeia Brasileira, 5ª edição (Anvisa, 2010), a máxima diluição válida (MDV) é "a máxima diluição permitida da amostra em análise onde o limite de endotoxina pode ser determinado. Ela se aplica para injeções ou soluções de administração parenteral na forma reconstituída ou diluída para administração, quantidade de fármaco por peso, se o volume da forma da dosagem for variável".
Para o produto Ciprofloxacino solução injetável 2 mg/mL, o limite de endotoxinas é 1,76 UE/mL. Utilizando-se um reagente LAL de sensibilidade rotulada (λ), de 0,25 UE/mL, o valor da MDV para esse teste é
O procedimento a seguir é descrito na Farmacopeia Brasileira, 5ª edição (Anvisa, 2010) para a avaliação de substâncias relacionadas na monografia de Varfarina matéria prima .
Substâncias relacionadas. Proceder conforme descrito em Cromatografia em camada delgada (5.2.17.1), utilizando sílica-gel GF254, como suporte, e mistura de ácido acético glacial, cloreto de metileno e cicloexano (20:50:50) como fase móvel. Aplicar, separadamente, à placa, 20 μL de cada uma das soluções, recentemente preparadas, descritas a seguir.
Solução (1): dissolver 0,20 g da amostra em acetona e diluir para 10 mL com o mesmo solvente.
Solução (2): diluir 2 mL da Solução (1) em 10 mL de acetona.
Solução (3): diluir 1 mL da Solução (2) em 200 mL de acetona.
Solução (4): dissolver 40 mg de varfarina SQR em acetona e diluir para 10 mL com o mesmo solvente.
Solução (5): transferir 10 mg de acenocumarol SQR e 1 mL da Solução (1) para balão volumétrico de 10 mL, diluir com acetona e completar o volume com o mesmo solvente.
Desenvolver o cromatograma. Remover a placa, deixar secar ao ar. Examinar os
cromatrogramas obtidos sob luz ultravioleta (254 nm). Qualquer mancha obtida no
cromatograma com a Solução (1), com exceção da mancha principal, não pode ser mais
intensa que a obtida no cromatograma com a Solução (3) (___%). O teste não é válido a
não ser que o cromatograma obtido com a Solução (5) mostre duas manchas claramente
separadas e que a mancha do cromatograma obtida com a Solução (3) seja claramente
visível.
O limite individual de substâncias relacionadas para a Varfarina, em porcentagem, é
As Parcerias para o Desenvolvimento Produtivo (PDP) visam ampliar o acesso a medicamentos e produtos para saúde considerados estratégicos para o Sistema Único de Saúde (SUS), por meio do fortalecimento do complexo industrial do país. O objetivo principal é financiar o desenvolvimento nacional para reduzir os custos de aquisição dos medicamentos e produtos que atualmente são importados ou que representam um alto custo para o sistema. Tendo como base a RDC 2531 de 2014, considere as afirmações abaixo.
I As PDP são parcerias que envolvem a cooperação mediante acordo entre instituições públicas e entre instituições públicas e entidades privadas para desenvolvimento, transferência e absorção de tecnologia, produção, capacitação produtiva e tecnológica do país em produtos estratégicos para atendimento às demandas do SUS.
II No caso da empresa detentora da tecnologia utilizar o insumo farmacêutico ativo (IFA) internacional, a empresa a internalizar a tecnologia deve manter o IFA internacional após conclusão da internalização.
III Para a primeira aquisição, o registro sanitário do produto objeto da PDP poderá ser da instituição pública ou da entidade privada, desde que esteja em processo comprovado de desenvolvimento, transferência e absorção de tecnologia.
IV O ano 1 da PDP se iniciará a partir da assinatura do termo de compromisso e formalização de acordo ou contrato entre as partes, iniciando as etapas de desenvolvimento, transferência e absorção de tecnologia do produto objeto da PDP com observância dos critérios, diretrizes e orientações da RDC 2531 supra mencionada.
Em relação ao exposto, estão corretas as afirmações
Considere a seguinte informação:
“Evidência documentada que as instalações, sistemas de suporte, utilidades, equipamentos e processos foram desenhados de acordo com os requisitos de BPF”
De acordo com a RDC nº 17, de 2010, essa informação diz respeito à