Questões de Concurso Comentadas sobre química
Foram encontradas 7.320 questões
Nossas reservas d’água são afetadas por várias formas de poluição: biológica, térmica, sedimentar e química. Embora os sedimentos constituam a maior quantidade de poluentes, os agentes químicos são os potencialmente mais nocivos.
Os tratamentos dos efluentes devem considerar os agentes poluidores, as características do corpo d’água e sua utilização.
Sobre os tratamentos empregados, assinale a afirmativa correta.
A Norma ABNT NBR ISSO/IEC 17025:2005 especifica os requisitos gerais que os laboratórios precisam cumprir para ter a competência de realizar ensaios e/ou calibrações, incluindo amostragem.
Sobre o processo de validação de um método, analise as ações a seguir.
I. Calibração com utilização de padrões de referência.
II. Comparações interlaboratoriais.
III Comparações com resultados obtidos por outros métodos.
Segundo a Norma ABNT NBR ISSO/IEC 17025:2005 pode(m) ser adotada(s):
Os resíduos gerados nos laboratórios comumente precisam ser tratados antes do descarte na rede de esgoto. Os tratamentos devem considerar suas características e periculosidade.
O tratamento de sais de metais pesados deve incluir
Para padronizar uma solução de ácido clorídrico, um analista pesou 0,764 g de bórax e transferiu quantitativamente para um erlenmeyer, dissolvendo em 50 mL de água destilada. Esta solução foi titulada até coloração rosa com o ácido clorídrico em presença de três gotas do indicador vermelho de metila consumindo 40,00 mL do ácido clorídrico.
A concentração do ácido titulado (em mol.L-1 ) é igual a
Dados: Massa molar do bórax (Na2B4O7.10H2O) = 382g.mol-1
Uma das etapas do tratamento de água envolve a retirada de impurezas coloidais que não sedimentam com facilidade. Essa etapa do processo ocorre em misturadores adequados, nos quais são adicionadas à água substâncias químicas que promovem a formação de flocos coloidais. Em seguida, a água é conduzida para tanques e o processo de tratamento prossegue.
A operação de separação que ocorre nesses tanques é denominada
O tratamento convencional da água inclui os processos de coagulação, floculação, filtração, desinfecção, ajuste do pH e fluoretação. Nas etapas do tratamento da água podem ser utilizados os produtos químicos permanganato de potássio, cloreto de ferro (III), sulfato de ferro (III), carbonato de sódio e hipoclorito de sódio.
Estes produtos são adequadamente utilizados nos processos
Os sais de nitrato são compostos iônicos muito solúveis em água. Quando se coloca 1 mol de nitrato de cálcio em 1 litro de água ocorre a formação de uma solução na qual os íons estão separados e solvatados por moléculas de água.
Nessa solução, as concentrações em mol.L-1 dos íons cálcio e nitrato, presentes na solução são, respectivamente,
A piretrina e a aletrina, cujas estruturas estão representadas a seguir, são inseticidas naturais muito utilizados no controle de pragas agrícolas, antes da Segunda Guerra Mundial.
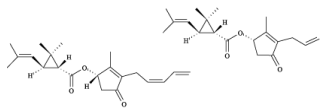
Hoje, esses e outros compostos naturais inspiram a busca por biopesticidas, substâncias produzidas pela natureza que são capazes de atuar no controle de pragas. O objetivo é que os biopesticidas, que causam menos danos ao ecossistema, substituam paulatinamente os inseticidas sintéticos.
As cadeias carbônicas da piretrina e da aletrina possuem
A amônia atmosférica é de fundamental importância para a química ambiental, pois se trata de um composto capaz de neutralizar, em determinada extensão, gases ácidos e espécies ácidas adsorvidas em partículas.
Em uma determinada temperatura, a amônia apresenta pKb= 5. Nessas condições uma solução 0,1mol.L–1 de amônia apresentará valor de pH igual a
Dado: pKw = 14
Uma mistura gasosa de 10 mmol de CO e 10 mmol de H2O é colocada em um reator de 500 mL e aquecida até 500 °C, atingindo o equilíbrio:
CO(g) + H2O(g) ⇄ CO2(g) + H2(g) com Kc = 4,00
A concentração, em mol.L–1 de dióxido de carbono nesse
equilíbrio é de
A reação de cloro gasoso com uma base forte pode ser descrita pela equação
Cℓ2(g) + 2 NaOH(aq) → NaCℓ(aq) + NaOCℓ(aq) + H2O(ℓ)
Para o posterior preparo de 0,5 litro de solução 0,2 mol.L–1 de hipoclorito de sódio obtido por meio desse processo, a massa de hidróxido de sódio que deve reagir em presença de excesso de cloro gasoso é, no mínimo, igual a
Dados: Massas molares H = 1g.mol–1 ; O = 16g.mol–1 Na = 23g.mol–1
A concentração de NaCl é, em mol/L,
4 análises são realizadas ao mesmo tempo, nas mesmas condições e com a mesma concentração de Ag+ .
Dado:
Composto / Kps Agl / 8,3 x 10-17 AgBr / 5,2 x 10-13 AgCl / 1,8 x 10-10 AgIO3 / 3 x 10-8
Se as análises envolverem os íons I- , Br- , Cl- e IO3 - qual deles precipitará primeiro?
Considere as figuras abaixo:

A figura
Na mistura, a pressão parcial, em atm, do CO2 é