Questões de Química - Representação das transformações químicas para Concurso
Foram encontradas 1.436 questões
Fe2 (SO4 )3 + Cr2 (SO4 )3 + K2SO4 + H2O → K2Cr2O7 + H2SO4 + FeSO4
Considere a reação entre o ácido sulfúrico e o hidróxido de sódio e assinale a alternativa que apresenta a soma dos índices m, n, o e p.
mH2SO4(aq) + nNaOH(aq) oNas2SO4(s) + pH20(l)
Referente à seguinte reação:
Mg (s) + O2 (g) MgO(s) ------------>
analise as assertivas e assinale a alternativa que aponta as corretas.
I. É uma reação de combinação.
II. A molécula de oxigênio é formada por ligação iônica.
III. A queima de 2 mol de Mg(s) resulta em 1 mol de MgO.
IV. O produto da reação é um sólido iônico.
O dióxido de carbono gerado em estações espaciais pode ser convertido em oxigênio pela reação com o superóxido de potássio, conforme a equação a seguir.
2CO2(g) + 4KO2(s) → 2K2CO3(s) + 3O2(g)
Tendo como referência a reação precedente, assinale a opção que apresenta a massa exata de KO2 necessária para a conversão total de 11,2 L de CO2 em oxigênio nas condições normais de temperatura e pressão (CNTP), considerando que o valor do volume molar de um gás ideal nas CNTP seja 22,4 L e que todos os gases comportem-se idealmente.
Texto 19A1AAA
O titânio, um metal de transição do “bloco d” da tabela periódica, é bastante empregado em ligas metálicas devido a sua elevada resistência mecânica e baixa tendência à corrosão, além da baixa densidade. Ele é obtido a partir, principalmente, da ilmenita (FeTiO3) e do rutilo (TiO2).
O sulfato de alumínio pode ser obtido a partir da reação representada na equação não balanceada:
Al2 O3 (s) + H2 SO4 (aq) → Al2 (SO4 )3(aq) + H2 O(l)
Quando o balanceamento da equação é feito usando-se o coeficiente 1 para Al2 O3 , os coeficientes para o H2 SO4 e para H2 O são, correta e respectivamente,
A Aspirina, como é conhecida o ácido acetilsalicílico (C9H8O4), é um fármaco que apresenta propriedades antitérmicas, anti-inflamatórias e analgésicas. Esse fármaco pode ser sintetizado pela reação entre o ácido salicílico (C7H6O3) e o anidrido acético (C4H6O3), catalisada por um ácido.
A equação a seguir representa o processo de síntese da aspirina.
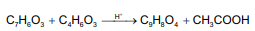
Considere, hipoteticamente, que 3 g de ácido salicílico foram misturados com 6 mL de uma solução de anidrido acético cuja densidade e grau de pureza são 1,2 g/mL e 80% m/m, respectivamente.
Se o rendimento da reação química é 100%, qual a
massa aproximada de aspirina produzida em gramas?
A densidade é o coeficiente entre o volume ocupado por um material e a massa desse material.
Em relação à nomenclatura química de ácidos, bases e sais, julgue o item a seguir.
O composto Al(OH)Cl2
possui o nome de
(mono-)hidroxi-cloreto de alumínio.
Em relação à nomenclatura química de ácidos, bases e sais, julgue o item a seguir.
O sal sulfato cúprico penta-hidratado possui
a fórmula molecular CuSO4
.5H2O.
Os diferentes tipos de átomos podem se reunir das mais variadas maneiras, formando uma infinidade de agrupamentos diferentes ou os aglomerados iônicos, e cada molécula representa uma substância pura ou espécie química. Sobre as substâncias químicas, elementos e misturas, julgue o item a seguir.
O gás oxigênio e o gás ozônio são formas
alotrópicas do elemento oxigênio.
Os diferentes tipos de átomos podem se reunir das mais variadas maneiras, formando uma infinidade de agrupamentos diferentes ou os aglomerados iônicos, e cada molécula representa uma substância pura ou espécie química. Sobre as substâncias químicas, elementos e misturas, julgue o item a seguir.
A substância permanganato de potássio é
composta por 6 elementos.
De acordo com o sistema internacional de unidades e as conversões para medida de volume, julgue o item a seguir.
Em uma semana de práticas laboratoriais,
foram consumidos 1.000 litros de água; ou
seja, esse volume é equivalente a 1 m3
ou
1.000 dm3
de água.
É comum, nos laboratórios químicos, efetuar a mistura de duas (ou mais) soluções de um mesmo soluto, ou a mistura de soluções cujos solutos reagem entre si. A respeito desse assunto e os cálculos relacionados, julgue o item a seguir.
Misturando-se 300 mL de HCl 0,4 M a
200 mL de NaOH 0,6 M, a solução final
apresentará excesso de um dos reagentes.
Em relação às reações de neutralização, as quais formam diversos tipos de sais, julgue o item a seguir.
A reação, devidamente balanceada, entre ácido fosfórico e hidróxido de cálcio, é expressa por:
2 H3PO3
+ 3 Ca(OH)2
→ Ca3(PO3
)2
+ 6 H2O
Sobre as características dos ácidos de grande importância industrial, julgue o item a seguir.
O HCl puro é conhecido como gás clorídrico
ou cloridreto ou cloreto de hidrogênio.
