Questões de Concurso
Sobre sistemas homogêneos: equilíbrio químico na água: ph e poh, indicadores ácido-base, solução tampão. em química
Foram encontradas 584 questões
A ordem crescente de pKaH é:
Analisando as propriedades mencionadas no texto, para o grupo 12 e partindo do zinco em direção ao mercúrio, é possível prever tendência de:
(Dados, em g/mol; H=1, S=32 e O=16; log 2=0,3)
Dado: pKb NH4OH = 4,7
O aumento do pH da água é provocado por um ácido.
Considere as informações apresentadas no quadro a seguir para responder à questão abaixo :

I. O intervalo aceitável para o valor de pH no sistema de distribuição se situa entre 6,0 e 9,5.
II. A determinação da cor, turbidez e teor residual de desinfetante deve ser realizada em todas as amostras coletadas para análises microbiológicas.
III. A concentração mínima de cloro residual deve ser de 0,2 mg/mL em toda a extensão do sistema de distribuição; nos pontos de consumo deve ser de 2 mg/mL.
IV. A coleta de amostras para pesquisa de coliformes totais e Escherichia coli em mananciais superficiais deve ser realizada mensalmente e o volume mínimo de amostra a ser analisado deve ser de 1.000 mL.
V. Na água tratada para consumo humano, o parâmetro microbiológico para coliformes totais e Escherichia coli usado como indicador de contaminação fecal e de eficiência de tratamento é “ausência em 0,1 L de amostra”.
Está correto o que se afirma apenas em
N2(g) + H2(g) ⇌ NH3(g)
Considerando, ainda, as propriedades do equilíbrio químico citado, assinale a afirmativa correta.
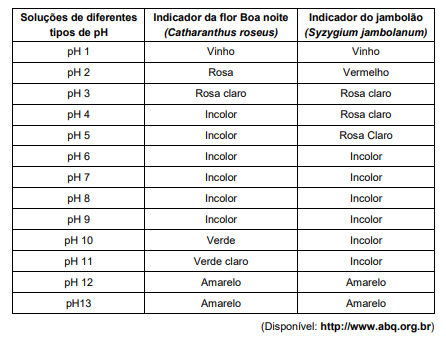
Ao testar uma solução aquosa de NaOH de concentração 0,001 mol/L observou-se as seguintes cores, respectivamente, para os indicadores de flor Boa noite e do jambolão:
( ) O eletrodo combinado possui dois eletrodos de referência (Ag/AgCl) que medem a diferença de potencial elétrico por meio da membrana de vidro.
( ) O eletrodo combinado possui um bulbo de vidro com um anel externo de prata metálica (Ag) sensível a íons H+.
( ) O termo eletrodo de vidro combinado é sinônimo de eletrodo de vidro, tendo a mesma estrutura e funcionamento.
( ) As principais interferências para esse tipo de eletrodo são os íons metálicos alcalinos, como o Na+, Li+ e K+.
A sequência correta é
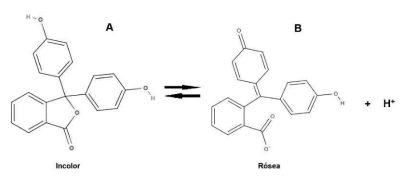
Sobre as espécies envolvidas na reação acima, assinale a alternativa correta:
Dentre os indicadores de pH, citam-se:
A fórmula química que representa sua estrutura é apresentada abaixo:
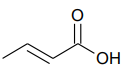
Uma solução aquosa de ácido crotônico foi preparada pela dissolução de 2,15g do ácido em água, sendo o volume final igual a 500mL.
[Dados: massas molares (em g.mol-1). C: 12; H: 1; O: 16.]
O pH dessa solução é igual a
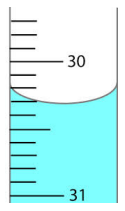
Baseado nessas informações, assinale a alternativa correta.