Questões de Concurso
Sobre sistemas homogêneos: solubilidade dos sais, hidrólise dos sais e curvas de titulação. em química
Foram encontradas 197 questões
A figura a seguir apresenta duas curvas quase que sobrepostas, correspondentes ao mesmo procedimento: a curva de titulação entre um fármaco ácido e NaOH e a curva obtida quando se tira a 1ª derivada da curva de titulação. Analise as afirmações e escreva V para verdadeiro ou F para falso:
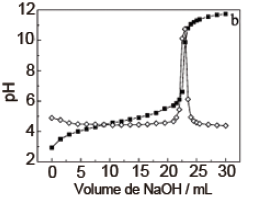
( ) A titulação envolve ácido fraco e base forte, se não fosse potenciométrica a utilização de fenolftaleína como indicador, teria preferência a utilização de alaranjado de metila.
( ) O p.e. (ponto de equivalência) será em pH igual 7.
( ) o pKa do titulado é próximo a 5.
( ) A derivada da curva tem por finalidade indicar o volume gasto até o p.e. para a neutralização.
( ) O sitema atua como um tampão na faixa 4<pH<5,5.
Assinale a alternativa correta quanto ao verdadeiro ou falso:
Uma amostra de 50 mL de água contendo cátions Fe3+ foi tratada com excesso de NH4OH. O precipitado obtido depois de lavado, secado e calcinado pesou 0,320 g. A quantidade de ferro, em mol/L presente na amostra é
Dados:
Massas molares em g/mol
Fe = 56
O = 16
H = 1
N = 14
Considere o gráfico abaixo.
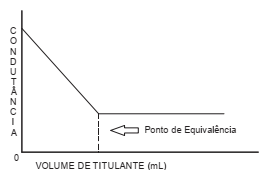
Esse gráfico representa uma titulação condutométrica cuja reação pode ser entre soluções aquosas de
Observe a tabela de solubilidade abaixo.
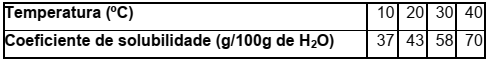
Em uma solução, preparada em um laboratório, foram dissolvidas 27 gramas de soluto em 100
gramas de água, à temperatura de 20 °C. Essa solução será
Íons Ba2+(aq) são altamente tóxicos e suas soluções não podem ser descartadas na rede de esgoto. Esses íons devem, portanto, ser removidos de misturas que se pretende descartar, o que pode ser feito através de reações de precipitação. Para a remoção de íons Ba2+(aq) de 1,0 L de resíduo de concentração 0,01 mol L -1 foram propostos os seguintes procedimentos:
I. Adição de 0,1 L de solução de Na2CO3 0,1 mol L-1
II. Adição de 0,1 L de solução de Na2SO4 0,1 mol L-1
III. Adição de 0,1 L de solução de Na3PO4 0,01 mol L-1
IV. Adição de 0,1 L de solução de NaOH, 0,01 mol L-1
Dado: Constante do produto de solubilidade dos compostos de bário (Ks)
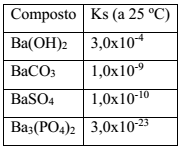
O procedimento que resulta na produção de um material mais adequado ao descarte é:
O íon potássio em 250,0 mL de uma amostra de água mineral foi precipitado com tetrafenilborato de sódio:
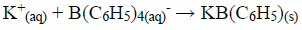
O precipitado foi filtrado, lavado e redissolvido em um solvente orgânico. Um excesso de quelato EDTA/mercúrio(II) foi adicionado:
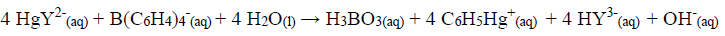
O EDTA liberado foi titulado com 30,00 mL de Mg2+ 0,0550 mol L-1.
(Dado: K = 39 g mol-1, Mg = 24 g mol-1)
Após a análise, a concentração aproximada do íon potássio em partes por milhão será:
Excesso de ferro no solo pode atrofiar o crescimento de algumas espécies de plantas. Espécies como a Sophora tomentosa, popularmente conhecida como feijão-da-praia, têm seu crescimento comprometido caso o solo tenha porcentagem de ferro (III) acima de 40%. Como forma de avaliar a qualidade do solo para a plantação de feijão-da-praia, foi realizada análise em uma amostra de 0,97 g de solo, devidamente coletado, contendo ferro (II) e (III). O laboratorista realizou os seguintes procedimentos:
1º. Oxidou todo ferro (II) a ferro (III) na presença de ácido nítrico.
2º. Precipitou o ferro (III), com excesso de hidróxido de amônio, a óxido de ferro hidratado (Fe2O3.xH2O).
3º. Filtrou o precipitado com cuidado.
4º. Lavou, calcinou e pesou o precipitado, obtendo 0,496g de óxido de ferro (III).
Após realizar essas etapas, emitiu o laudo que atestava:
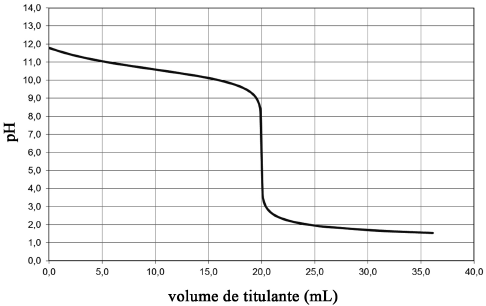
Uma amostra de 50 mL de água recolhida de um aquário contendo
dezenas de peixes mortos foi titulada com ácido clorídrico
0,01 mol/L. A curva do pH × volume de HC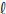 obtida para essa
titulação é mostrada acima. A partir dessas informações
e considerando que, nessa amostra de água, apenas uma das
substâncias — para as quais os valores das constantes de
dissociação ácida (Ka) ou básica (Kb) são fornecidos — está
presente, assinale a opção que indica, corretamente, a substância
titulada.
obtida para essa
titulação é mostrada acima. A partir dessas informações
e considerando que, nessa amostra de água, apenas uma das
substâncias — para as quais os valores das constantes de
dissociação ácida (Ka) ou básica (Kb) são fornecidos — está
presente, assinale a opção que indica, corretamente, a substância
titulada.
Com base nas informações, tem-se que o(a)
Assinale a alternativa que apresenta a resposta correta:

O pH da maior parte das águas naturais contendo organismos vivos está entre 6,5 e 8,5. Para níveis de pH abaixo de 4,0, todos os vertebrados, a maioria dos invertebrados e muitos microrganismos são destruídos. Os lagos mais suscetíveis ao estrago são os de baixas concentrações de íons básicos, como HCO3 - , que os tamponam contra variações de pH. Mais de 300 lagos no estado de Nova York não contêm peixes e 140 lagos em Ontário, Canadá, são destituídos de vida. A chuva ácida que parece ter matado os organismos nesses lagos origina-se a centenas de quilômetros no sentido contrário ao vento nas regiões do Vale de Ohio e dos Grandes Lagos. Fonte: BROWN, Theodore; LEMAY, H. Eugene; BURSTEN, Bruce E. Química: a ciência central. 9 ed. Prentice-Hall, 2005.p.660.
Com relação aos efeitos sobre o ecossistema, analise as afirmativas:
I. Como os ácidos reagem com os metais e com os carbonatos, a chuva ácida é corrosiva
tanto para metais quanto para materiais de construção em pedra.
II. A acidez tem afetado muitos lagos no norte da Europa, dos Estados Unidos e do Canadá, reduzindo as populações de peixes, bem como afetando outras partes do ecossistema dentro dos lagos e nas florestas das redondezas.
III.O dióxido de enxofre por si só é prejudicial tanto à saúde humana quanto à propriedade; além disso, SO2 atmosférico pode ser oxidado a SO3 por quaisquer dos vários diferentes caminhos e este, se dissolve na água, produzindo ácido sulfúrico, causando efeitos ambientais desastrosos; constituindo o “maior vilão” da chuva ácida.
A alternativa que indica, apenas afirmação (ões) verdadeira(s) é: