Questões de Concurso
Sobre transformações químicas e energia em química
Foram encontradas 1.539 questões
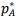 = 12 kPa e de B é
= 12 kPa e de B é 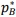 = 8 kPa. Considerando que a mistura líquida das duas substâncias a 80 °C apresenta pressão de vapor total p = 10 kPa, calcule a fração molar de A (yA) e de
B (yB) na fase vapor e assinale a alternativa correta.
= 8 kPa. Considerando que a mistura líquida das duas substâncias a 80 °C apresenta pressão de vapor total p = 10 kPa, calcule a fração molar de A (yA) e de
B (yB) na fase vapor e assinale a alternativa correta. Disponível em: <http://cfq.org.br/noticia/>. Acesso em: 3 mar. 2021, com adaptações.
Com base nessas informações, é correto afirmar que a eletrólise consiste em um processo
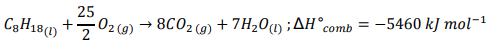
Sobre a reação de combustão do isoctano, é INCORRETO afirmar que
I. A eletrólise é um processo no qual o trabalho elétrico gera a reação química.
II. Se o cloreto de sódio for submetido a uma eletrólise ígnea ou aquosa, os produtos dessa reação são os mesmos: sódio metálico e gás cloro.
III. Na eletrólise em meio aquoso, quem irá definir a ordem de descarga dos íons é o potencial de redução padrão, E°red, de cada substância durante esse processo.
IV. A quantidade formada de produtos eletroquímicos será definida pela primeira lei de Faraday.
É CORRETO o que se afirma em
Diante do exposto, assinale a alternativa correta.
4 Ag(s) + O2(g) + 4 H+ (aq) → 4 Ag+ (aq) + 2 H2O(l)
Com base nessa reação, o valor da variação de energia livre de Gibbs padrão (ΔG0) é, aproximadamente, igual a
Dados: E0 Ag+/Ag0 = −0,80 V; E0 O2(g)/H2O = 1,23 V; Constante de Faraday (F) = 96500 C mol-1
Acerca de radioatividade, de biomoléculas e de aplicações da química em sabões e detergentes, julgue o item.
A radioatividade é a emissão espontânea de radiação
por núcleos radioativos, ou seja, a desintegração ou a
decomposição de núcleos atômicos. Assim, um núcleo é
radioativo se ele pode mudar sua estrutura
espontaneamente e emitir radiação.
Quanto ao equilíbrio químico e às características das soluções-tampão e das pilhas, julgue o item.
O termo pilha é empregado para se referir a um
dispositivo constituído de dois eletrodos e um eletrólito,
arranjados de maneira a produzir energia elétrica.
Quando os eletrodos são conectados a um aparelho
elétrico, uma corrente flui pelo circuito, pois o material
de um dos eletrodos oxida-se espontaneamente,
liberando elétrons (ânodo), enquanto o material do
outro eletrodo reduz-se, usando esses elétrons (cátodo).
Com relação à termoquímica, à entropia, à espontaneidade de reações e à cinética química, julgue o item.
A liberação de energia não pode ser usada para predizer,
com certeza, se uma reação irá ocorrer ou não. Em uma
dada temperatura e em uma dada pressão, um processo
que libera energia (processo exotérmico) e que leva a
um aumento da entropia é duplamente favorecido, pois
os dois fatores levam à diminuição da energia livre do
sistema.
Com relação à termoquímica, à entropia, à espontaneidade de reações e à cinética química, julgue o item.
Entropia é a quantidade termodinâmica da medida do
grau de desordem em um sistema, sendo que a variação
de entropia é igual ao calor fornecido reversivelmente a
um sistema, multiplicado pela temperatura em que a
transferência de calor ocorre na vaporização, conversão
da substância do estado líquido para o estado de vapor.
Com relação à termoquímica, à entropia, à espontaneidade de reações e à cinética química, julgue o item.
Pela lei de Hess, na mesma temperatura e na mesma
pressão, a entalpia de uma reação é a soma das entalpias
de qualquer sequência de reações em que a reação total
possa ser dividida.

Com base nas informações apresentadas, a variação de entalpia da hidrogenação do propeno corresponde a:
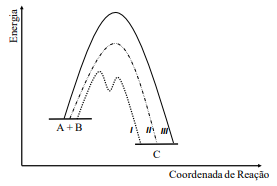
Assinale a alternativa INCORRETA.
Sabendo-se que o equivalente eletroquímico da prata é 1,118mg/C, o tempo foi de cerca de:
Um metal que tenha sofrido processo corrosivo por formação de trincas microscópicas ao longo do contorno dos grãos da estrutura metalúrgica, sem alteração significativa nas dimensões da peça, foi vítima de corrosão: