Questões de Concurso
Sobre transformações químicas e energia em química
Foram encontradas 1.539 questões
A matéria pode sofrer diversos tipos de transformações. A transformação química sempre há formação de novos materiais, em uma transformação química ocorre:
A diferença entre a energia livre dos produtos e a energia livre dos reagentes em uma reação química, sob condições normais, é chamada de energia livre de Gibbs (Δ𝐆°). A figura abaixo mostra dois diagramas da coordenada de reação onde se pode observar a energia livre de Gibbs.
Figura - Diagramas da coordenada de reação. (Fonte: BRUICE, 2006).
Considere os dois diagramas da coordenada de reação para as reações 1 e 2 mostradas na figura e assinale a alternativa correta que descreve cada uma das reações.
As transformações químicas são ações que resultam na formação de novas substâncias e estão presentes em nosso dia a dia. Analise os fenômenos abaixo e assinale a alternativa correta que contém apenas transformações químicas.
I. O escurecimento de um metal.
II. A destruição da camada de ozônio.
III. A explosão de uma panela de pressão.
IV. A queima da madeira.
A entalpia média de ligação é a média da entalpia de dissociação de ligação para uma série de ligações A-B em moléculas diferentes. Assim, a entalpia de reação pode ser determinada através da entalpia de ligação média. Nesse sentido, considere a reação abaixo.
𝑆𝐹4(𝑔)+𝐹22(𝑔)→𝑆𝐹6(𝑔)
As entalpias médias de ligação para 𝐅2,𝐒𝐅4, e 𝐒𝐅6 são +158, +343, e +327 KJ mol-1, respectivamente, com base nestas informações, assinale a alternativa correta que indica o valor da entalpia de reação para a produção de 𝐒𝐅6(𝐠) a partir do 𝐒𝐅4(𝐠).
No calorímetro da figura abaixo, que opera em volume constante, 1000 moléculas de glicose foram queimadas.
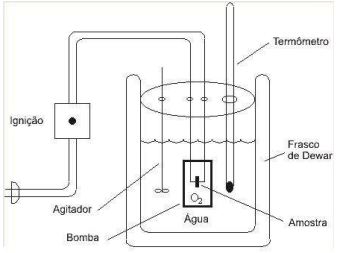
Figura: Bomba Calorimétrica. https://www.ebah.com.br/content/ABAAABOZIAG/bomba-calorimetrica
O calor do processo foi da ordem de 6397,5 KJ em temperatura igual a 25 °C. Dados: R = 8,314 JK-Mol- A variação de entalpia nesta reação foi igual a
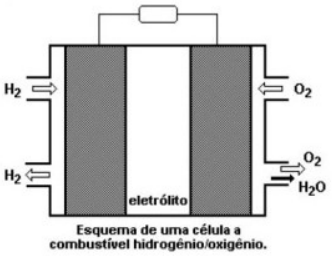
Sobre a pilha de hidrogênio, pode-se afirmar que
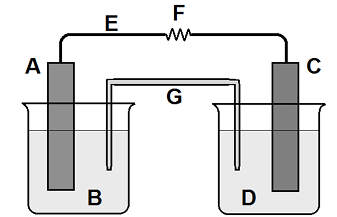
Legenda da figura: (A) placa de estanho, (B) solução aquosa contendo íons Sn2+, (C) placa de alumínio, (D) solução aquosa contendo íons Aℓ3+, (E) fio metálico, (F) resistência elétrica e (G) ponte salina.
Considerando os seguintes dados:
E°(Sn2+/Sn) = -0,14 V E°(Aℓ3+/Aℓ) = -1,68 V
Durante o funcionamento da pilha, o estudante fez algumas afirmações:
I. A concentração de íons alumínio aumenta na solução da direita (D). II. Na placa de alumínio ocorre a corrosão. III. O fluxo de elétrons ocorre pelo fio metálico a partir da placa de estanho em direção à placa de alumínio. IV. Na placa de estanho ocorre a redução. V. A placa de estanho é o polo negativo da cela galvânica.
Dessas afirmações,
Reação 1: ΔH1 = +15,3 kJ/mol e ΔS1 =+30 J/K.mol Reação 2: ΔH2 = +1,8 kJ/mol e ΔS2 =-159 J/K.mol.
Escolha a alternativa que representa os valores de ΔG1 e ΔG2 em kJ/mol, respectivamente, e as previsões corretas de espontaneidade ou não espontaneidade da reação nessa temperatura:
Para que um átomo de tório com número de massa igual a 228 se desintegre espontaneamente para formar um átomo, do mesmo elemento químico com número de massa igual a 220, os números de partículas alfa e beta que deverão ser emitidas, respectivamente, são:
Dados das massas molares em g.mol-1 : C = 12 e O = 16.
I. O polo positivo de uma célula eletrolítica chama-se catodo.
II. O processo de oxidação ocorre no anodo.
III. A pilha seca de zinco-carbono é um exemplo de aplicação prática dos processos eletroquímicos.
IV. Uma reação que no sentido desejado apresente ΔE° > 0 não será espontânea.
Estão corretas as sentenças:
[Feº (s) l Fe2+ (aq) (1 mol/ L) II Pb2+(aq) (1mol/L) I Pbº (s) ]
Nessa pilha, a espécie química que atua como oxidante é:
I. A corrosão eletroquímica é o tipo de corrosão mais comum, pois é a que ocorre com os metais, geralmente na presença de água. II. O reator tubular é um exemplo de equipamento para reação química utilizado na indústria química. III. Na Internet, ao criar uma senha, é recomendável usar apenas números, em uma combinação de até 5 caracteres. Marque a alternativa CORRETA:
I. Os alcanos contêm somente C e H em ligações simples na sua estrutura. II. A corrosão eletrolítica é um processo eletroquímico que ocorre pelo efeito da radiação solar nos metais. III. O conceito de parâmetro, em estatística, inclui os valores singulares que existem na população e que impedem a sua caracterização. Marque a alternativa CORRETA:
I. A série química dos metais alcalinoterrosos inclui elementos que reagem com facilidade com a água para formar hidróxidos fortemente básicos. II. Existem três tipos de corrosão, a corrosão eletrolítica, a corrosão química e a corrosão eletroquímica. III. A corrosão química é o ataque de algum agente físico diretamente sobre determinado material, que pode ou não ser um metal. Marque a alternativa CORRETA: