Questões de Concurso
Sobre transformações químicas: elementos químicos, tabela periódica e reações químicas em química
Foram encontradas 1.107 questões
O carbonato de cálcio, CaCO3(s), decompõe-se com aquecimento para produzir CaO(s) e CO2(g). Uma amostra de CaCO3 é decomposta e o dióxido de carbono é coletado num frasco de 300 mL. Depois de completada a decomposição, o gás tem pressão de 1,5 atm à temperatura de 27°C. Qual é a quantidade aproximada de matéria, em mol de CO2, produzida na decomposição?
Dados:
R = 0,0821 L atm/K.mol
Massas molares (g/mol): C = 12; Ca = 40 e O = 16.
No século XVIII, houve um grande estabelecimento da Química como uma ciência bem fundamentada e os cientistas passaram a adotar o “método científico” em seus estudos. Por meio de estudos meticulosos e experiências cuidadosas, foram introduzidas leis importantes que conseguiram explicar como as reações químicas ocorrem e como as substâncias se comportam com uma regularidade de modo geral. Entre essas leis estavam as leis ponderais, que eram aquelas que relacionavam massas dos participantes de uma reação química.
Assinale a alternativa CORRETA que apresenta o
nome do criador de uma das Leis Ponderais,
denominada de Lei de Conservação das Massas:
As reações de precipitação caracterizam-se pela formação de um precipitado (sólido)- que é um sólido pouco solúvel - a partir de uma solução aquosa de duas substâncias. Resumindo, quando se juntam duas soluções aquosas de duas substâncias diferentes formam-se novas substâncias, e uma delas é menos solúvel e precipita.
Assinale a alternativa CORRETA que corresponde a um tipo de reação e precipitação:
I. A formação das grutas calcárias, das estalactites e das estalagmites.
II. A formação de recifes de corais.
III. A formação das conchas de alguns moluscos.
IV. A deposição do calcário nos canos e nas resistências das máquinas de lavar .
Estão CORRETAS:

A introdução de átomo de halogênio no anel aromático do esqueleto básico de substâncias ilícitas se tornou uma importante ferramenta
para a obtenção de novas drogas sintéticas, o que deixou o mercado ilegal dessas substâncias um passo a frente da legislação que controla
o tráfico de drogas. Considerando essas informações e as figuras I e II, acima, que representam, respectivamente, estruturas químicas de
algumas drogas sintéticas comuns e as dessas mesmas drogas, na forma halogenada, julgue item que segue.
Basicamente, existem dois tipos de pólvora: a pólvora negra e a pólvora sem fumo. Quase todas as armas de fogo modernas usam a pólvora sem fumo. A pólvora negra, classificada como explosivo, é composta por enxofre, carvão e nitrato de potássio. Entre as várias reações que ocorrem na explosão da pólvora negra, a mais simples está descrita pela seguinte equação química:
2KNO3(s) + S(s) + 3C(s) 6 K2S(s) + N2(g) + 3CO2(g).
Com base nessas informações, julgue o item.
A redução do nitrato, que consome três moles de elétrons por
mol de NO3
–
em meio ácido, gera o óxido nítrico, que é um
agente complexante mais forte que o íon nitrato.
Basicamente, existem dois tipos de pólvora: a pólvora negra e a pólvora sem fumo. Quase todas as armas de fogo modernas usam a pólvora sem fumo. A pólvora negra, classificada como explosivo, é composta por enxofre, carvão e nitrato de potássio. Entre as várias reações que ocorrem na explosão da pólvora negra, a mais simples está descrita pela seguinte equação química:
2KNO3(s) + S(s) + 3C(s) 6 K2S(s) + N2(g) + 3CO2(g).
Com base nessas informações, julgue o item.
Se o gás carbônico reagir com a água para formar o ácido
carbônico, o CO2 receberá um par de elétrons da água, que é
uma base de Lewis.
Basicamente, existem dois tipos de pólvora: a pólvora negra e a pólvora sem fumo. Quase todas as armas de fogo modernas usam a pólvora sem fumo. A pólvora negra, classificada como explosivo, é composta por enxofre, carvão e nitrato de potássio. Entre as várias reações que ocorrem na explosão da pólvora negra, a mais simples está descrita pela seguinte equação química:
2KNO3(s) + S(s) + 3C(s) 6 K2S(s) + N2(g) + 3CO2(g).
Com base nessas informações, julgue o item.
O nitrato reage com a água conforme a reação
NO3 – + H2O-> HNO3 + OH– ,
aumentando significativamente o pH da solução formada,
haja vista que o caráter básico do OH–
é mais forte que o
caráter ácido do NO3
–
.
Nos anos de 1950, tanto os Estados Unidos quanto a antiga União Soviética tinham programas para usar o decaborano (B10H14) como combustível de foguete. Esse composto reage violentamente com oxigênio, de acordo com a equação química a seguir.
B10H14 + 11 O2 → 5 B2O3 + 7 H2O
Na tentativa de simular a eficiência máxima do foguete, considere que um engenheiro elaborou um projeto que consumiu o decaborano (B10H14) com 80% de pureza.
Sabendo que 10 mil kg do decaborano foram colocados para reagir com oxigênio, aproximadamente quantos mols de moléculas do B2O3 foram produzidos na reação?
Uma substância branca, solúvel em água e sólida A foi aquecida em uma mufla a altas temperaturas. Essa substância se decompõe para formar novas substâncias B e C. A substância B é muito útil na produção de vidros e cerâmicas. A substância C é um gás, da combustão completa entre carbono e oxigênio.
Baseando-se nessas informações, é correto afirmar que as substâncias A,B e C são, respectivamente:
O acetileno (etino) é um gás incolor, instável e altamente combustível e produz uma chama de elevada temperatura (mais de 3000°C ou 5400°F) em presença de oxigênio. Este gás tem cheiro agradável, quando puro, mas o seu odor é comumente desagradável devido às impurezas que o acompanham. O acetileno é a matéria prima na fabricação de solventes industriais, de plásticos de borracha sintética, de explosivos e na síntese de compostos orgânicos, como ácido acético e álcool etílico. A produção industrial do gás etino está representada, abaixo, em três etapas, conforme as equações balanceadas:
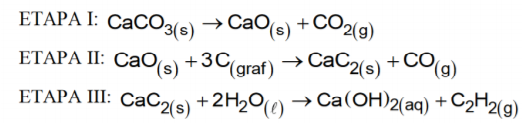
Considerando-se as etapas citadas e admitindo-se que o rendimento de cada etapa da obtenção do gás etino, por esse método, é de 100%, a massa de carbonato de cálcio, necessária para produzir 10,4g do gás etino (C2H2), é
Dados:
H = 1u, C =12u, O = 16u, Ca = 40u.
Foi realizada uma aula experimental visando a síntese de uma amida aromática, a acetanilida (ou N-fenil-acetamida), de acordo com o procedimento experimental resumidamente descrito a seguir:
Em um béquer limpo e seco, misturar o ácido acético glacial e o acetato de sódio anidro. Adicionar a anilina e, em seguida, o anidrido acético. Após 10 minutos de reação, verter o meio reacional sobre água destilada gelada, sob agitação. A acetanilida precipita. Filtrar em funil de Büchner e lavar o produto bruto com água destilada gelada até pH neutro. Purificar a acetanilida por recristalização usando água quente e carvão ativado.
Sobre esse procedimento, considere as seguintes afirmativas:
1. A reação envolvida na síntese da acetanilida é uma reação de acilação.
2. Foi utilizada água gelada na etapa de precipitação da acetanilida bruta para reduzir as perdas de produto por solubilidade em água.
3. A purificação do produto bruto foi realizada em água quente porque a acetanilida é mais solúvel em água quente que em água fria.
4. O carvão ativado foi utilizado para acelerar a precipitação da acetanilida.
Assinale a alternativa correta.
A utilização de conversores catalíticos no escapamento de automóveis diminui a emissão de gases tóxicos que são também geradores de compostos ácidos, como indicado nas seguintes equações:
2CO + 2NO → 2CO2 + N2
2CO + O2 → 2CO2
2NO → N2 + O2
Em um teste de laboratório, foram colocadas em um reator inextensível quantidades estequiométricas de CO, NO, O2 e
catalisador. Considerando que o experimento foi realizado nas CNTP, que os reagentes e os produtos são gases ideais e
que a conversão foi de 100%, qual será a pressão final do sistema, em atm?