Questões de Concurso
Sobre velocidade de reação, energia de ativação, concentração, pressão, temperatura e catalisador em química
Foram encontradas 397 questões
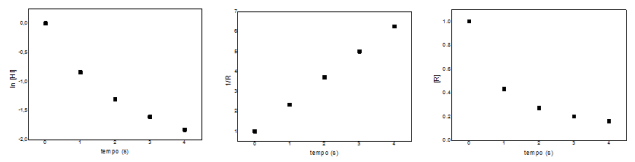
Baseado nos gráficos, assinale a alternativa correta.
I. Existem três variáveis que afetam as velocidades de reação: concentração, estado físico dos reagentes e temperatura. II. As equações de velocidade podem ser escritas para expressar como as concentrações variam com o tempo. III. Em nível molecular, as velocidades de reação dependem da frequência das colisões entre as moléculas, quanto maior a frequência das colisões, menor a velocidade de reação.
É correto afirmar que:
(CH3)3C-Br(l) + OH- (aq) → (CH3)3C-OH(l) + Br- (aq)
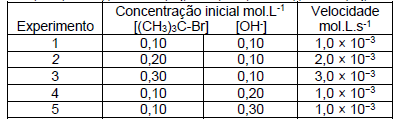
A partir dos dados fornecidos, assinale a alternativa que indica a equação da velocidade e a ordem da reação corretas.
Identifique abaixo as afirmativas verdadeiras ( V ) e as falsas ( F ).
( ) O valor numérico da constante de equilíbrio de reações químicas sofre alteração quando há variação da temperatura da reação.
( ) A velocidade de reações químicas é alterada pela presença de catalisadores e estes (catalisadores) são totalmente consumidos durante a reação.
( ) A diminuição da temperatura de uma reação exotérmica desfavorece a formação de produtos.
( ) O tempo necessário para que a concentração do reagente se reduza a um quarto da concentração inicial é denominado de meia-vida.
( ) As leis de velocidades são determinadas experimentalmente e geralmente não podem ser escritas a partir da estequiometria da equação química da reação.
Assinale a alternativa que indica a sequência correta, de cima para baixo.
Considere certa reação química, representada pela equação genérica abaixo:
A + B → Produtos
Na temperatura de 20°C, apresenta um lei de velocidade (V1 ), V1 = k.[A].[B].
Qual será a sua lei de velocidade (v2 ) na temperatura de 30°C, admitindo-se que essa reação obedece ao princípio de Van’t Hoff, nas mesmas concentrações iniciais dos reagentes.

A partir dos dados extraídos do gráfico responda aos itens abaixo:
Admitindo-se que, para uma certa reação, o segmento AB representa o nível da entalpia dos reagentes e o segmento FG o nível da entalpia dos produtos, podemos afirmar que:
1. A reação direta é exotérmica.
2. A energia de ativação desse processo é representada pelo segmento FG. 3. O perfil do gráfico permite afirmar que a reação direta representa uma reação de combustão. 4. A variação de entalpia (energia) de reação direta é de ΔH = – 600,00 kJ. 5. A reação inversa é exotérmica.
Assinale a alternativa que indica todas as afirmativas corretas.
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item
As expressões da constante de equilíbrio são muito
importantes porque permitem que os químicos possam
prever a direção e a extensão de uma reação química.
Contudo, uma expressão da constante de equilíbrio não
fornece informações relacionadas à velocidade na qual
o equilíbrio é alcançado.
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item
Catalisador é a substância ou espécie que aumenta a
velocidade de reação, não é consumida e fornece um
mecanismo alternativo de baixa energia de ativação
para a reação. Um catalisador é capaz de afetar a
constante de equilíbrio da reação considerada, por
modificar a velocidade da reação direta, aumentando o
tempo requerido para o estabelecimento do equilíbrio.
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item
A velocidade de uma reação é proporcional às
concentrações dos reagentes, com exceção das reações
de ordem zero, em que as variações de concentração
não produzem nenhum efeito.
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item
A velocidade de uma reação química depende,
essencialmente, do número total de colisões por
unidade de tempo entre as partículas (átomos,
moléculas ou íons) das espécies que participam da
reação, bem como da fração de tais colisões que,
efetivamente, promove a reação química.
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item
A velocidade de uma reação química é calculada pela
multiplicação da variação de concentração de uma
substância pelo intervalo de tempo em que a variação
considerada ocorre, levando em conta o coeficiente
estequiométrico da substância.
I. acelera a reação, mas não altera a composição química dos reagentes e produtos envolvidos. II. não altera a quantidade de substância produzida na reação. III. não altera a variação de entalpia. É correto o que está contido em
Em relação ao aumento das velocidades de reações químicas, é CORRETO afirmar que
Nessas condições, a velocidade da reação química aumenta quantas vezes se as concentrações das espécies A e B forem duplicadas?
( ) Catalizadores são substâncias que, quando participam da reação, são consumidas e podem ser classificados como homogêneos ou heterogêneas. ( ) A ordem de reação é sempre determinada pelos coeficientes estequiométricos da reação. ( ) A velocidade de uma reação de ordem zero é independente da concentração do reagente. ( ) O tempo de meia-vida de uma substância numa reação química é o tempo necessário para que sua concentração se reduza à metade da inicial. ( ) A constante de equilíbrio de uma reação química é adimensional e seu valor numérico depende da temperatura.
Assinale a alternativa que indica a sequência correta, de cima para baixo.