Questões de Concurso
Sobre velocidade de reação, energia de ativação, concentração, pressão, temperatura e catalisador em química
Foram encontradas 397 questões
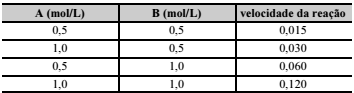
De acordo com a lei da ação das massas, a velocidade de uma reação é diretamente proporcional ao produto das concentrações molares dos reagentes. Assim, para a reação aA + bB ⇄ cC + dD, a equação da velocidade é V = K·[A]a ·[B]b . Considerando essas informações e que, na tabela acima, são apresentados resultados experimentais para essa mesma reação, assinale a opção correta.
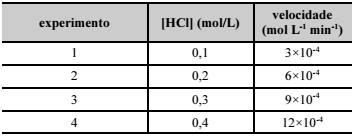
Considerando a tabela acima, que apresenta os valores de
concentração de HCl e das velocidades de decomposição do gás
cloreto de hidrogênio obtidos experimentalmente, conforme reação
elementar 2HCl(g) → H2(g) + Cl2(g), e que não houve variação de
temperatura, assinale a opção que apresenta a constante de
velocidade característica dessa reação.
CO2(g) ⇌ CO2(aq)
CO2(aq) + H2O(ℓ) ⇌ H2CO3(aq)
H2CO3(aq) ⇌ HCO3-(aq) + H+(aq)
A composição da solução e o efeito de eventuais perturbações deste sistema são tais que a(o)
O gás dióxido de enxofre (SO2) reage com o gás NO2 formando o trióxido de enxofre, que promove a acidificação da água da chuva.
SO2(g) + NO2(g) ⇌ SO3(g) + NO(g)
A constante de equilíbrio (Kc) dessa reação é igual a 25 a 400 K. Nessas condições, coloca-se em um reator, de volume fixo, a quantidade de gases necessária para se ter, inicialmente, 1 mol L-1 de cada um dos quatro gases.
Ao se atingir o equilíbrio, a concentração de SO3(g) no sistema, em mol L-1, será mais próxima de
A gordura trans é formada no processo de hidrogenação da gordura vegetal, sobre catalisador metálico. A gordura vegetal é rica em ácidos graxos insaturados de simetria cis. A equação genérica para o processo de hidrogenação da gordura vegetal é mostrada a seguir.
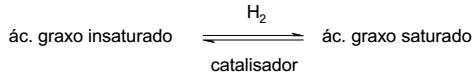
Com base no exposto acima, identifique como verdadeiras (V) ou falsas (F) as seguintes afirmativas:
( ) O catalisador acelera a reação nos dois sentidos e proporciona a formação do isômero mais estável.
( ) O catalisador metálico impede a formação do isômero cis.
( ) O catalisador promove na sua superfície a reação de isomerização.
( ) O ácido graxo insaturado é instável.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
O ciclopropano é utilizado como anestésico. Com aquecimento, esse composto se rearranja em propeno. A constante cinética da reação é k = 5,4 x 10-2 h -1 .
Dado: ℓn(2) = 0,693.
O tempo de meia-vida (em horas) do ciclopropano é:
Qual será a equação matemática que representa a velocidade de transformação da seguinte reação? (Considere todos os compostos como gasosos.)
CO + NO2 → CO2 + NO
O cloreto de titânio(IV), TiCl4, é um importante produto químico industrial. Esse pode ser usado tanto na obtenção do TiO2 quanto de titânio metálico. O TiCl4 pode ser obtido a partir de um minério contendo titânio (TiO2 impuro), utilizado em excesso, com carbono e gás cloro, conforme a equação química a seguir.
TiO2(s) + 2 Cl2(g) + C(s) → TiCl4(l) + CO2(g)
Considere que a obtenção do TiCl4 seja feita a partir de 852 g de C e 852 g de Cl2.
Dados: Cl2 (71 g mol-1 ); C (12 g mol-1 ) e TiCl4 (190 g mol-1 )
O reagente limitante e a massa em gramas de TiCl4 obtida são, respectivamente:
A velocidade das reações químicas é uma área estudada pela Cinética Química. Esse estudo é importante porque é possível encontrar meios de controlar o tempo de desenvolvimento das reações, tornando-as mais lentas ou mais rápidas, conforme a necessidade. Alguns dos fatores que interferem na velocidade das reações.
Assinale a alternativa CORRETA que apresenta alguns desses fatores:
I. Temperatura.
II. Concentração.
III. Pressão.
IV. Superfície de contato.
V. Catalisador.
Estão CORRETAS:

O processo de Haber-Bosh, que opera em altas temperaturas e altas
pressões, é bastante utilizado para a produção industrial da amônia
(NH3). Nesse processo, os gases nitrogênio (N2) e hidrogênio (H2)
reagem exotérmica e reversivelmente para formar amônia gasosa
(NH3). No processo inverso, a reação de decomposição da amônia
em nitrogênio e hidrogênio em superfície de platina apresenta
cinética que segue comportamento conforme representado no
gráfico acima, que mostra a variação da concentração molar da
amônia gasosa [NH3] em função do tempo. Acerca dessas reações,
julgue o item a seguir.
Se a taxa de formação da amônia for de 3,2 × 10-2 mol.L-1.s-1 , então as taxas de consumo dos gases N2 e H2, serão, respectivamente, 1,6 × 10-2 mol.L-1.s-1 e 4,8 × 10-2 mol.L! 1.s-1 .

O processo de Haber-Bosh, que opera em altas temperaturas e altas
pressões, é bastante utilizado para a produção industrial da amônia
(NH3). Nesse processo, os gases nitrogênio (N2) e hidrogênio (H2)
reagem exotérmica e reversivelmente para formar amônia gasosa
(NH3). No processo inverso, a reação de decomposição da amônia
em nitrogênio e hidrogênio em superfície de platina apresenta
cinética que segue comportamento conforme representado no
gráfico acima, que mostra a variação da concentração molar da
amônia gasosa [NH3] em função do tempo. Acerca dessas reações,
julgue o item a seguir.
O biodísel pode ser obtido a partir da reação de transesterificação do óleo de soja catalisada por base. Com o objetivo de aumentar o rendimento do produto dessa reação em bancada, foi aplicada a metodologia de planejamento fatorial, sendo os fatores, níveis estudados e efeitos obtidos apresentados na tabela abaixo.

Considerando as informações acima apresentadas, julgue o item a
seguir, relativo à otimização da reação e ao planejamento de
experimentos realizados.
O ozônio pode ser convertido em oxigênio por meio de sua reação com dióxido de nitrogênio, de acordo com a equação química abaixo.
NO2(g) + O3(g) → NO3(g) + O2(g)
Com o intuito de estudar a cinética da reação, três experimentos foram realizados, tendo sido obtidos os seguintes resultados:

A partir das informações e dos dados apresentados acima e dos conceitos usados em cinética química, julgue o item subsecutivo.
A lei da velocidade para essa reação pode ser expressa por:
v = 5,47×104
[NO2][O3].
O ozônio pode ser convertido em oxigênio por meio de sua reação com dióxido de nitrogênio, de acordo com a equação química abaixo.
NO2(g) + O3(g) → NO3(g) + O2(g)
Com o intuito de estudar a cinética da reação, três experimentos foram realizados, tendo sido obtidos os seguintes resultados:

A partir das informações e dos dados apresentados acima e dos conceitos usados em cinética química, julgue o item subsecutivo.
As ordens da reação para O3 e NO2 são, respectivamente, 2 e 1.
O ozônio pode ser convertido em oxigênio por meio de sua reação com dióxido de nitrogênio, de acordo com a equação química abaixo.
NO2(g) + O3(g) → NO3(g) + O2(g)
Com o intuito de estudar a cinética da reação, três experimentos foram realizados, tendo sido obtidos os seguintes resultados:

A partir das informações e dos dados apresentados acima e dos conceitos usados em cinética química, julgue o item subsecutivo.
Em uma reação de ordem zero, a constante de velocidade dessa
reação não depende da concentração dos reagentes, sendo
constante durante toda a reação. Nessas reações, a
concentração dos reagentes diminui linearmente em função do
tempo.
O ozônio pode ser convertido em oxigênio por meio de sua reação com dióxido de nitrogênio, de acordo com a equação química abaixo.
NO2(g) + O3(g) → NO3(g) + O2(g)
Com o intuito de estudar a cinética da reação, três experimentos foram realizados, tendo sido obtidos os seguintes resultados:

A partir das informações e dos dados apresentados acima e dos conceitos usados em cinética química, julgue o item subsecutivo.
A velocidade de consumo de O3 é o dobro da velocidade de
consumo de NO2 e igual à velocidade de produção de O2.
Considere, hipoteticamente, que, em um estudo cinético de formação do composto AB, a reação ocorre nas seguintes condições experimentais: uma reação de primeira ordem em relação a A e de segunda ordem em relação a B.
Nessas condições, a velocidade da reação química aumenta quantas vezes se as concentrações das espécies A e B forem duplicadas?