Questões de Concurso
Foram encontradas 1.343 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
I - Os principais indicadores de contaminação fecal são os Coliformes Termotolerantes e Cianobactérias. II - As principais formas de fósforo encontradas nas águas residuárias são os ortofosfatos, os polifosfatos, o fósforo orgânico e o fósforo tenso. III - A quantidade de Nitrogênio Total dosada em uma amostra é proporcional à soma do Nitrogênio Kjeldahl Total e do Nitrito. IV - A temperatura é um parâmetro controlado nas águas residuárias porque elas provocam elevações da temperatura do corpo receptor, ocasionando o aumento da solubilidade do oxigênio dissolvido e da taxa das reações químicas e biológicas. V - A quantidade de Sólidos Totais contida em um efluente é constituída por Sólidos em Suspensão e Sólidos Dissolvidos, sendo as suas características físicas e físico-químicas classificadas em sólidos voláteis e fixos.
É(São) correta(s) APENAS a(s) afirmação(ões)
J = K . A . ΔP
em que K é a permeabilidade da membrana, A é a área de filtração e ΔP é a diferença de pressão absoluta entre o lado da alimentação e o lado do filtrado.
Considere um processo industrial de clarificação de suco de maracujá no qual a pressão manométrica no lado da alimentação seja de 2,5 bar e que o lado do filtrado esteja à pressão atmosférica e, ainda, que a membrana usada tem área de 1,5 m² e permeabilidade de 7,0 x 10⁻¹⁰ m² s . Com base nessas informações, determine, em l/h, o fluxo de suco de maracujá filtrado.
Dado: 1 bar = 10⁵ Pa e desprezar os efeitos de fouling.
Considere que uma determinada indústria afirma que utiliza gás natural como combustível para a operação de uma caldeira em sua planta. No entanto, a análise da amostra dos gases da chaminé, logo após a caldeira, revela que há emissão de SO2 , indicando que o combustível utilizado não é gás natural.
Para a determinação do tipo de combustível, foram disponibilizadas as informações presentes nas seguintes tabelas.
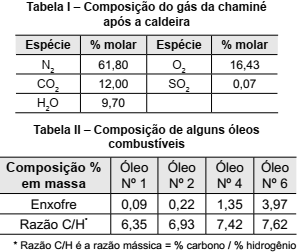
Dados: Massas molares C = 12 g/mol; H = 1 g/mol e S = 32 g/mol.
Considerando que o combustível seja composto apenas
por carbono, hidrogênio e enxofre, o óleo utilizado na
caldeira, de acordo com os dados da tabela II, é o de
número
Indústrias que operam com compostos sulfurados geralmente geram ácido sulfídrico (H2S), um gás altamente irritante para os olhos e vias respiratórias, além de possuir um odor desagradável de ovo podre. O processo Claus é uma alternativa para o tratamento desse poluente. Nele, parte do H2S é queimado em uma fornalha para se produzir SO2 , conforme apresentado na equação 1 a seguir.
H2S + 3/2 O2 → SO2 + H2O (1)
Os gases que saem da fornalha são misturados à outra parte de H2S e são alimentados em um reator catalítico, onde o enxofre elementar é formado, conforme equação 2 a seguir.
2H2S + SO2 → 2H2O + 3S (2)
Com base nesse processo, é correto afirmar que
Considere, em um sistema ideal, que uma chaminé recebeu 2,4 x 1019 moléculas de SO2 que foram misturadas com 10 g do carbonato de cálcio. Nessas condições, quantos miligramas, aproximadamente, de sulfato de cálcio ficariam retidos na chaminé?
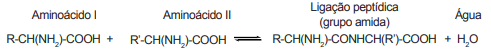 Considere que 2 mols de molécula do aminoácido I são adicionados para reagir com 1 mol de molécula do aminoácido II.
Quando o equilíbrio químico é estabelecido (equilíbrio 1), 20% do aminoácido I é consumido. Em seguida, adicionou-se
certa quantidade de mols de molécula do aminoácido II, e 10% do aminoácido I foi consumido até reestabelecer um novo
equilíbrio (equilíbrio 2).
Nessas condições, qual é a razão aproximada entre o primeiro e segundo equilíbrios?
Considere que 2 mols de molécula do aminoácido I são adicionados para reagir com 1 mol de molécula do aminoácido II.
Quando o equilíbrio químico é estabelecido (equilíbrio 1), 20% do aminoácido I é consumido. Em seguida, adicionou-se
certa quantidade de mols de molécula do aminoácido II, e 10% do aminoácido I foi consumido até reestabelecer um novo
equilíbrio (equilíbrio 2).
Nessas condições, qual é a razão aproximada entre o primeiro e segundo equilíbrios?2H2 (g) + 2NO (g) → N2(g) + 2H2O (g)
Para compreender a velocidade da reação química em função das concentrações dos reagentes, um técnico realizou os seguintes experimentos.
Experimento 1 – Quando dobrou a concentração do gás hidrogênio e reduziu à metade a concentração do óxido nítrico, a velocidade da reação dobrou.
Experimento 2 – Quando quadruplicou a concentração do gás hidrogênio e dobrou a concentração do óxido nítrico, a velocidade da reação química quadruplicou.
A partir dessas informações, é correto afirmar que a expressão matemática da Lei de Velocidade é representada por:
C6 H12O6 (s) + 6O2 (g) → 6CO2 (g) + 6H2O (g)
Nessas condições, e considerando que os gases são ideais, é correto afirmar que a variação de entalpia da mesma reação é, em quilojoules, aproximadamente igual a:
Dado: Constante dos gases (R) = 8,31 JK–1mol–1
Sendo assim, os reatores
Se a decomposição desse composto ocorre a 27°C, o valor aproximado da constante de velocidade, em s-1, é
Dados R = 8,31 J/mol.K ln (5x10-4 ) = -7,6
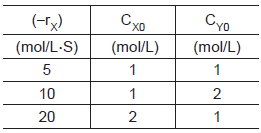
Com base nos dados da Tabela, a equação da velocidade pode ser
Nessas condições, a razão h/k, em 1/m, entre o coeficiente convectivo h e a condutividade térmica k, em W/(K.m), para uma parede de tamanho típico de 10 cm, é
Se uma malha de realimentação negativa com um controlador do tipo proporcional for aplicada ao sistema, como será o comportamento do sistema em malha fechada?
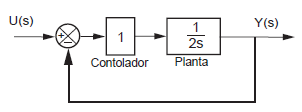
Qual será o erro em regime permanente para uma entrada do tipo rampa unitária?
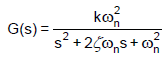
O valor inicial da resposta desse sistema para uma entrada doublê unitário, quando ele se encontra em repouso, é
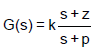
na qual k > 1 e z < p, para altas frequências da entrada, será
