Questões de Vestibular
Sobre fórmulas, balanceamento e leis ponderais das reações químicas em química
Foram encontradas 380 questões
I. Cu(OH)2 + H4P2O7-> Cu2P2O7 + H2O
II. H2S + O2 -> H2O + S8
III. Aℓ(OH)3 + H4SiO4 -> Aℓ4 (SiO4)3 + H2O
Assinale a alternativa que mostra corretamente os coeficientes estequiométricos das reações I, II e III.
De acordo com as informações acima, os valores de x e y são, respectivamente,
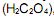 por exemplo, é um composto utilizado para corrigir a concentração de soluções alcalinas por meio da técnica de titulometria. Uma alíquota de 5,0 mL de uma solução de H2C2O4 0,100 mol/L foi titulada com uma solução de NaOH 0,100 mol/L, utilizando-se a fenolftaleí na como indicador. De acordo com a equação química (não balanceada) apresentada a seguir
por exemplo, é um composto utilizado para corrigir a concentração de soluções alcalinas por meio da técnica de titulometria. Uma alíquota de 5,0 mL de uma solução de H2C2O4 0,100 mol/L foi titulada com uma solução de NaOH 0,100 mol/L, utilizando-se a fenolftaleí na como indicador. De acordo com a equação química (não balanceada) apresentada a seguir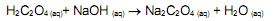
o volume esperado para observação do ponto de viragem é:
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.

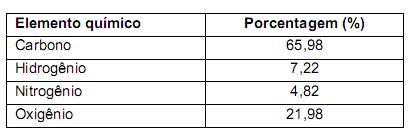
Linus Pauling, ganhador dos prêmios Nobel de Química e da Paz, ingeria diariamente entre 4 e 6 gramas dessa vitamina, por acreditar nos seus efeitos terapêuticos. No entanto, recomenda-se somente a ingestão diária de 3,5 x 10-4 mol dessa vitamina. Sobre essas informações, assinale o que for correto.
A fórmula mínima da vitamina C é C3H4O3.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Al(OH)3(aq) + 3/2 H2SO4(aq) ===> 1/2 Al2(SO4)3(s) + x H2O(l)
Em meio mol do sal, existem 2 mols de átomos de alumínio.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Al(OH)3(aq) + 3/2 H2SO4(aq) ===> 1/2 Al2(SO4)3(s) + x H2O(l)
O coeficiente “x” é igual a 6.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
O H2CrO4 é mais conhecido como ácido crômico, mas também pode ser chamado de ácido ortocrômico.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
O Ca(OH)Cl é chamado de cloreto básico de cálcio ou hidróxi-cloreto de cálcio.

O peróxido de hidrogênio, H2O2(l), é um líquido incolor espesso, empregado como antisséptico e alvejante, a depender da concentração. Ao reagir com algumas substâncias, o peróxido de hidrogênio pode atuar como oxidante ou redutor. A equação química não balanceada representa a reação do íon permanganato com o peróxido de hidrogênio.
A partir dessas informações e após o balanceamento dessa
equação química com os menores coeficientes
estequiométricos inteiros, é correto afirmar:
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO
Misturando-se 3,0 g de hidrogênio (H2) e 20,0 g de nitrogênio (N2) em um balão de vidro, provocando a reação entre os gases, de acordo com a equação abaixo
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

Misturando-se 3,0 g de hidrogênio (H2) e 20,0 g de nitrogênio (N2) em um balão de vidro, provocando a reação entre os gases, de acordo com a equação abaixo
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

Misturando-se 3,0 g de hidrogênio (H2) e 20,0 g de nitrogênio (N2) em um balão de vidro, provocando a reação entre os gases, de acordo com a equação abaixo
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

Misturando-se 3,0 g de hidrogênio (H2) e 20,0 g de nitrogênio (N2) em um balão de vidro, provocando a reação entre os gases, de acordo com a equação abaixo
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

Misturando-se 3,0 g de hidrogênio (H2) e 20,0 g de nitrogênio (N2) em um balão de vidro, provocando a reação entre os gases, de acordo com a equação abaixo
Em uma indústria do Estado de São Paulo que produz ácido sulfúrico 98% a partir da queima de enxofre elementar, com capacidade de produção inicial de 600 toneladas por dia, ocorreu uma emissão de gás dióxido de enxofre (SO2). Essa emissão de gás ultrapassou as fronteiras da fábrica de ácido sulfúrico e atingiu a população do entorno. Várias pessoas apresentaram agravos à saúde relacionados ao caso, como irritação das vias aéreas, desmaios, vômitos e enjoos, demandando atendimento hospitalar de emergência em hospitais da região. Também foram acionados o Serviço de Atendimento Médico de Urgência (SAMU) e o Corpo de Bombeiros.
JÚNIOR, L.M.; LORENZI, R.L. Revista brasileira de saúde ocupacional. São Paulo: 32(116): 31-37, 2007. (Adaptado)
Sobre o assunto, é CORRETO afirmar que:
para a produção de 600 toneladas de ácido sulfúrico são necessárias cerca de 400 toneladas
de S.
A ferrugem contém uma substância que é formada pela reação do oxigênio do ar com o ferro presente em uma superfície metálica. Esse processo pode ser representado pela seguinte equação química:
4 Fe(s) + 3 O2 (g) ---- > 2 Fe2 O3 (s)
Nesse processo, o oxigênio sofre a transformação química denominada:
I- .... C (grafita) + ..... O2(g) -> ...... CO2(g) ∆H = - 94,1 kcal/mol; II- .....C (grafita) + ..... H2(g) + ...... O2(g) -> ..... C2H5OH(l) ∆H = - 66,2 kcal/mol; III- .... H2(g) + ......O2(g) -> ..... H2O(l) ∆H = - 68,3 kcal/mol.
Sabendo-se que a variação de entalpia (∆H) de uma reação qualquer depende somente dos estados iniciais dos reagentes e do estado final dos produtos, marque a alternativa que corresponde aos coeficientes mínimos para a correta estequiometria das reações I, II e III, assim como a quantidade de calor produzida na combustão de 9,2 kg de álcool etílico líquido produzido [C2H5OH(l)], a partir dos coeficientes mínimos encontrados.