Questões de Vestibular
Sobre fórmulas, balanceamento e leis ponderais das reações químicas em química
Foram encontradas 380 questões
Os fogos de artifício são dispositivos envolvidos em um cartucho de papel. Na parte inferior, está a carga explosiva, que dispara os fogos para o alto. O propelente mais utilizado é a pólvora negra, uma mistura de nitrato de potássio, enxofre e carvão. Para a produção de fogos coloridos, misturam-se sais de diferentes metais à pólvora. Elétrons dos metais, quando são excitados pelo calor, emitem, ao retornarem a níveis de energia mais baixos, radiação eletromagnética de diferentes cores. Na tabela abaixo, são listados alguns metais e a coloração característica que deles pode ser emitida.

A seguir, é apresentada uma reação da pólvora, sem balanceamento e sem os estados físicos das substâncias.

Tendo como referência as informações acima, julgue os itens seguintes.
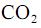 com
com 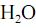 , fotocatalisada, resulte, exclusivamente, na formação de
, fotocatalisada, resulte, exclusivamente, na formação de 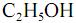 e
e 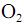 e que a densidade do
e que a densidade do 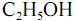 seja igual a 0,80 g/mL, calcule, em litros, o volume de
seja igual a 0,80 g/mL, calcule, em litros, o volume de 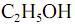 que seria formado a partir de 100,0 kg de
que seria formado a partir de 100,0 kg de 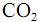 . Para marcação no Caderno de Respostas, despreze, caso exista, a parte fracionária do resultado final obtido, após ter efetuado todos os cálculos necessários.
. Para marcação no Caderno de Respostas, despreze, caso exista, a parte fracionária do resultado final obtido, após ter efetuado todos os cálculos necessários. 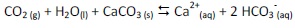
De acordo com essa equação química, dadas as afirmativas seguintes,
I. A reação química é reversível.
II. As espécies químicas presentes no lado dos produtos são chamadas de íons.
III. A equação química não está corretamente balanceada.
IV. A reação química para estar em equilíbrio, a velocidade da reação direta tem que ser igual à velocidade da reação inversa.
verifica-se que estão corretas
Leia o texto abaixo e assinale a alternativa que apresenta corretamente os termos que estão faltando nas lacunas, respeitando a sequência em que estas aparecem no texto.
Brasil será um dos campeões da mortalidade
cardiovascular em 2040; portanto, cuidado com o sal
Bate certa culpa – e receio – na hora de pegar o saleiro e despejar o pozinho branco sobre a comida? É bem provável que sim, principalmente se você é do tipo que se interessa e lê sobre nutrição e saúde. Afinal, não é de hoje que médicos alertam que o componente, em excesso, aumenta o risco de doenças do coração, especialmente a pressão alta, também conhecida como hipertensão. O Brasil deverá ocupar o posto de campeão de mortalidade cardiovascular em 2040, entre os países emergentes, de acordo com dados da OMS (Organização Mundial da Saúde). Mas não é o caso de eliminar totalmente o sal da alimentação. Ele tem sua importância para a saúde. “O sal de cozinha tradicional, ou cloreto de sódio, é composto por _______, mineral que representa o principal íon positivo dos fluidos corporais, e ________, íon negativo. Ambos têm funções importantes, como conter a pressão osmótica, quer dizer, o volume de água que passa através da membrana celular.
(Fonte: Disponível em: www.uol.com.br. Acesso em 3/10/2012)
Em maio de 2003, começaram a surgir as primeiras mortes relacionadas ao uso do contraste radiológico Celobar, comercializado pelo laboratório Enila. Pelo menos 21 pessoas podem ter morrido em decorrência da ingestão de Celobar (suspensão aquosa de sulfato de bário preparada em solução de sulfato de potássio) em todo o país. Depois das primeiras mortes relacionadas ao medicamento, a Anvisa (Agência Nacional de Vigilância Sanitária) interditou o laboratório Enila, que teve a falência decretada e continua fechado. O Celobar é utilizado para radiografar órgãos transparentes aos raios-X e seu princípio ativo é o sulfato de bário, que é um agente radiopaco que bloqueia os raios-X. Áreas do corpo em que o sal se localiza aparecerão brancas na radiografia. Em junho do mesmo ano, a Anvisa verificou que o referido laboratório havia comprado 600 kg de carbonato de bário - usado na formulação de raticidas. A indústria informou que a substância foi usada para sintetizar o sulfato de bário, matéria-prima do Celobar. Embora o laboratório Enila tenha informado que descartou todo carbonato de bário, o laudo da Fundação Oswaldo Cruz relatou que foi detectada grande quantidade de carbonato no lote (14%).
(Fonte: texto adaptado do site: http://sites.ffclrp.usp.br/ceiq/p_olimpiadas_iii_situacao.htm)
As fórmulas dos três compostos citados, na ordem em que aparecem no texto, são:
KMnO4 (aq) +HF (aq) → KF (aq) + MnF2 (aq) + H2O (l) + F2 (g)
Balanceie a equação química e, baseando-se na equação balanceada, assinale a proposição correta acerca dos estados de oxidação das espécies químicas e da estequiometria da reação:
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO NÚMERO MASSA ATÔMICA
QUÍMICO ATÔMICO
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
S 16 32,0
Cl 17 35,5
Ca 20 40,0
Fe 26 56,0
Cu 29 63,5
Zn 30 65,4
Ag 47 108,0
Sn 50 119,0
Xe 54 131,0
W 74 184,0
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO NÚMERO MASSA ATÔMICA
QUÍMICO ATÔMICO
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
S 16 32,0
Cl 17 35,5
Ca 20 40,0
Fe 26 56,0
Cu 29 63,5
Zn 30 65,4
Ag 47 108,0
Sn 50 119,0
Xe 54 131,0
W 74 184,0
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO NÚMERO MASSA ATÔMICA
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Si 14 28,0
S 16 32,0
Cl 17 35,5
Ca 20 40,0
Mn 25 55,0
Fe 26 56,0
Br 35 80,0
Rb 37 85,5
Zr 40 91,0
Ag 47 108,0
Cd 48 112,5
Ba 56 137,0
Pb 82 207,0
U 92 238,0
Pu 94 244,0
Ag(s) + H2S(g) + O2(g) → Ag2S(s) + H2O(l)
Considerando esse processo, assinale a opção correta.
CH3CH2OH + CrO3 -> CH3CHO + Cr3+ + HO-
A cor original do trióxido de cromo é vermelha e o produto tem a cor esverdeada. Analisando a equação acima, pode-se afirmar corretamente que
K2Cr2O7(aq.) + H2SO4(aq.) + C2H5OH(v) → C2H4O(g) + K2SO4(aq.) + Cr2(SO4)3(aq.) + H2O(l)
Analise as afirmativas referentes a esse processo químico.
I. A equação química corretamente balanceada tem como soma dos menores números inteiros 31.
II. A equação química corretamente balanceada tem como soma dos menores coeficientes inteiros 20.
III. O etanol é oxidado a aldeído acético e o dicromato
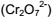 , amarelo-alaranjado, da
origem ao sulfato de íon crômio (III), verde.
, amarelo-alaranjado, da
origem ao sulfato de íon crômio (III), verde.
IV. O agente oxidante é o dicromato de potássio; portanto, ele contém o elemento que recebe elétrons, sofrendo redução.
V. O agente redutor é o ácido sulfúrico; portanto, contém o elemento que perde elétrons, sofrendo oxidação.
É correto o que se afirma APENAS em:
Bicarbonato de sódio e carbonato de sódio são duas substâncias químicas muito presentes no cotidiano. Entre várias aplicações, o bicarbonato de sódio é utilizado como antiácido estomacal e fermento de pães e bolos, e o carbonato de sódio, conhecido como barrilha ou soda, tem sua principal aplicação na fabricação de vidro comum.
As fórmulas químicas do bicarbonato de sódio e do carbonato de sódio estão correta e respectivamente representadas em

As moléculas cis-[Pt(NH3)2Cl2] e trans-[Pt(NH3)2Cl2] proporcionam resultados biológicos iguais, pois possuem a mesma fórmula estrutural.
Em uma jazida que contenha nióbio com número de oxidação +5, a fórmula do óxido predominante desse metal corresponde a:
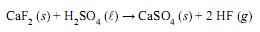
Considere que a massa molar do HF seja igual a 20 g·mol –1 e que a massa molar do CaF2 seja igual a 78 g·mol –1 . Se 100 kg de ácido fluorídrico são obtidos a partir de 260 kg de fluorita impura, é correto afirmar que o teor percentual, em massa, de CaF2 nesse minério é
Supondo rendimento de 100%, a massa, em gramas, de cloreto de cálcio que deve reagir para produzir 10 g de carbonato de cálcio é, aproximadamente,
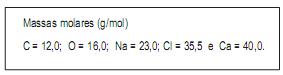
I) X H2 + O2 → H2O
II) Ca(OH)2 + H3PO4 → H2O + A
III) Na + ZnCl2 → NaCl + Zn.
