Questões de Vestibular
Sobre representação das transformações químicas em química
Foram encontradas 889 questões
TEXTO 1
Queimada
À fúria da rubra língua
do fogo
na queimada
envolve e lambe
o campinzal
estiolado em focos
enos
sinal.
É um correr desesperado
de animais silvestres
o que vai, ali, pelo mundo
incendiado e fundo,
talvez,
como o canto da araponga
nos vãos da brisa!
Tambores na tempestade
[...]
E os tambores
e os tambores
e os tambores
soando na tempestade,
ao efêmero de sua eterna idade.
[...]
Onde?
Eu vos contemplo
à inércia do que me leva
ao movimento
de naufragar-me
eternamente
na secura de suas águas
mais à frente!
Ó tambores
ruflai
sacudi suas dores!
Eu
que não me sei
não me venho
por ser
busco apenas ser somenos
no viver,
nada mais que isso!
(VIEIRA, Delermando. Os tambores da tempestade. Goiânia: Poligráfica, 2010. p. 164, 544, 552.)
O Texto 1 faz menção a água, bem cuja disponibilidade e qualidade têm causado sérias preocupações. Sabe-se que em muitos casos, a água da chuva pode superar em qualidade as águas superficiais e subterrâneas. Por não entrar em contato com o solo nem estar diretamente sujeita ao lançamento de poluentes de origem antropogênica, a água da chuva pode constituir uma fonte alternativa, com qualidade razoável para diversos usos. A qualidade do ar tem grande influência sobre a qualidade da água da chuva. Dependendo da localização, suas características podem ser afetadas por fatores naturais ou pela ação antrópica. Em regiões próximas a oceanos, há maior probabilidade de se encontrar sódio, potássio, magnésio e cloro na água da chuva. A concentração de cloretos na água da chuva varia de 0,1 a 2,0 mgL-1, podendo chegar a valores maiores, dependendo da proximidade com os oceanos.
Considerando-se uma precipitação de 100 mm, ou seja, que em 1m2 , houve a precipitação de 100 litros de água, e que a água desse 1 m2 possa ser armazenada em um recipiente, qual seria a quantidade molar aproximada de íons cloreto presente nessa água?
Considere a média aritmética da concentração de íons cloreto para realizar esse cálculo.
Assinale a alternativa que apresenta a resposta correta:
A pólvora é considerada a primeira mistura explosiva, usada na China, na Arábia e na Índia. Há textos chineses antigos que a denominam “substância química do fogo”, mesmo sendo uma mistura de nitrato de potássio, carvão e enxofre. A combustão da pólvora pode ser representada pela seguinte equação:
4KNO3 + 7C + S → 3CO2 + 3 CO + 2 N2 + K2CO3 + K2S
O que caracteriza a explosão é o súbito aumento de
volume, com grande liberação de energia. Nas CNTP,
520 g de pólvora produzem, por explosão,
INSTRUÇÃO: Para responder à questão, analise o texto a seguir.
Construir casas e edifícios exige uma escolha criteriosa
de materiais de construção, levando em conta aspectos
de segurança, durabilidade e custo adequado. Por
exemplo, certos elementos, como vigas, colunas e paredes,
precisam ter boas propriedades mecânicas; as
partes expostas devem resistir à erosão causada pela
água e pelo ar; o risco de incêndio deve ser minimizado
pelo uso de materiais não inflamáveis.
Consideradas essas exigências, duas substâncias que
poderiam estar presentes na composição desses materiais
são:
Após determinado processo industrial, obtém-se uma mistura contendo sulfato de sódio (Na2 SO4 ) e carbonato de sódio (Na2CO3 ). Uma amostra contendo 10,0 g dessa mistura foi completamente neutralizada com 100 mL de uma solução 1,00 mol.L–1 de HCl.
O sulfato de sódio não reage com ácido clorídrico e o carbonato de sódio reage segundo a reação representada a seguir.
Na2CO3 (s) + 2 HCl(aq) → 2 NaCl(aq) + CO2(g) + H2O(l)
O teor de carbonato de sódio na mistura é de
A criolita é um minério cujo principal componente é o fluoreto de alumínio e sódio. Sua principal aplicação é na produção do alumínio, onde é adicionada à alumina (óxido de alumínio), obtendo-se uma mistura de o temperatura de fusão de 950°C, tornando economicamente viável a eletrólise da alumina e a obtenção do metal alumínio.
A relação entre a massa de sódio e de alumínio na
criolita é de 23/9 e, portanto, a fórmula mínima do
fluoreto de alumínio e sódio é
As tabelas I, II e III mostram os valores limites para o veículo em questão e os valores medidos.

Analisando-se esses dados, conclui-se que o veículo submetido à inspeção deve ter sido
Esses indicadores foram selecionados devido à sua maior frequência na atmosfera e também devido aos efeitos adversos que causam ao meio ambiente. Para cada um deles, foram definidos padrões de qualidade do ar, ou seja, limites máximos de concentração que, quando ultrapassados, podem afetar a saúde, a segurança e o bem-estar da população, bem como ocasionar danos ao meio ambiente em geral.
Assim, por exemplo, o estudo de um desses indicadores demonstrou que não se devem deixar veículos com o motor em funcionamento em ambientes pouco ventilados, como garagens fechadas e túneis sem circulação adequada de ar, porque ele se combina com moléculas de hemoglobina, inutilizando-as irreversivelmente para o transporte de oxigênio.
Esse indicador é um gás inodoro representado pela fórmula molecular
Um veículo de passeio, movido a gasolina, deixou a capital paulista com o tanque cheio, dirigindo-se a uma cidade do interior situada a 480 km, na região noroeste do estado. Ao final da viagem, verificou-se que o consumo médio do veículo foi de 16 km por litro de combustível.
Admitindo-se que a composição média da gasolina seja dada pela fórmula C8 H18 e que a combustão seja completa, conclui-se que o volume de CO2 , em litros, medido nas CATP e lançado ao ar durante a viagem foi de, aproximadamente,
Dados
Volume molar de gás nas CATP = 25 L / mol
Densidade da gasolina = 8 x 102 g / L
Massas molares em g / mol:
C = 12; H = 1 e O = 16
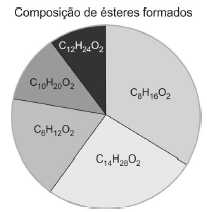
O ácido carboxílico presente em maior quantidade na amostra analisada é o:
Um certo polímero é produzido a partir de um monômero, que é um hidrocarboneto que contém somente uma instauração. A análise elementar por combustão completa de 0,5 mol de moléculas desse hidrocarboneto resultou em 1,5 mol de moléculas de CO2 .
A massa molar, em g.mol–1 , desse monômero é
Os palitos de fósforo são dispositivos simples empregados para fazer fogo. A chama se produz por meio de reações que ocorrem com as substâncias da “cabeça” do palito. Quando o palito é esfregado na superfície áspera da lateral da caixa, as substâncias reagem formando Sb2 O5 , KCl e SO2 . Essa reação é muito exotérmica e rápida e promove a reação de combustão e a propagação da chama pela madeira do palito.
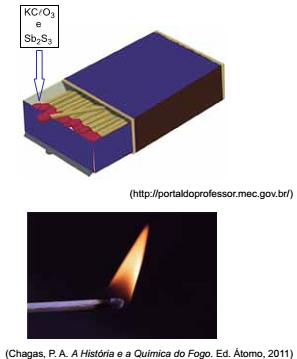
Equacionando-se e fazendo-se corretamente o balanceamento
da reação que ocorre pelo atrito da cabeça do palito de
fósforo com a lateral da caixa, a soma dos menores valores
inteiros dos coeficientes estequiométricos é
Um novo tipo de material especial, seleneto de bismuto, capaz de conduzir eletricidade em sua superfície, não em seu interior, quando em contato com um semicondutor, arseneto de gálio, resulta em um material que conduz eletricidade em várias direções e com níveis de energia diferentes. Esses compostos seguem a fórmula XyYx e suas ligações podem ser consideradas iônicas. Os íons negativos seguem a regra do octeto, enquanto que os íons positivos apresentam a mesma carga que o íon alumínio.
(Revista Pesquisa Fapesp, 234, agosto de 2015. Adaptado)
Os índices y e x nas fórmulas do material especial e do semicondutor são, respectivamente:
A bioluminescência é o fenômeno de emissão de luz visível por certos organismos vivos, resultante de uma reação química entre uma substância sintetizada pelo próprio organismo(luciferina) e oxigênio molecular, na presença de uma enzima (luciferase). Como resultado dessa reaçãobioquímica é gerado um produto em um estado eletronicamenteexcitado (oxiluciferina*). Este produto, por suavez, desativa-se por meio da emissão de luz visível, formandoo produto no estado normal ou fundamental (oxiluciferina).Ao final, a concentração de luciferase permanece constante.

O esquema ilustra o mecanismo geral da reação de bio-luminescência de vagalumes, no qual são formados dois produtos diferentes em estados eletronicamente excitados,responsáveis pela emissão de luz na cor verde ou na cor vermelha.

A luz branca é composta por ondas eletromagnéticas de todas as frequências do espectro visível. O espectro de radiação emitido por um elemento, quando submetido a um arco elétrico ou a altas temperaturas, é descontínuo e apresenta uma de suas linhas com maior intensidade, o que fornece “uma impressão digital” desse elemento. Quando essas linhas estão situadas na região da radiação visível, é possível identificar diferentes elementos químicos por meio dos chamados testes de chama. A tabela apresenta as cores características emitidas por alguns elementos no teste de chama:
Elemento Cor
sódio laranja
potássio violeta
cálcio vermelho-tijolo
cobre azul-esverdeada
PbCO3(s) + 2 HNO3(aq) ® Pb(NO3)2(aq) + H2O (ℓ) + CO2(g) (Equação 1)
Pb(NO3)2(aq) + H2SO4(aq) ® PbSO4(s) + 2 HNO3(aq) (Equação 2)
Supondo que uma amostra de 0,79 g do mineral tenha produzido 0,84 g de PbSO4, pode-se concluir que a porcentagem em massa de PbCO3 na amostra é, em valores arredondados, de
TEXTO 5
NA VIRADA DO SÉCULO, o biólogo Roosmarc conheceu o ápice da fama ao descobrir um novo gênero de primata: o sagui-anão-de-coroa-preta. Foi considerado pela revista Time o grande herói do planeta. Entre os mais de 500 primatas no mundo, Roosmarc descobrira o Callibella humilis, o macaquinho mais saltitante e alegre, anãozinho, com aquela coroa preta. Enquanto outros primatólogos matavam os animais para descrevê-los, dissecando-os em laboratórios, longe da Amazônia, ele criava macacos em sua casa. Esperava que morressem de forma natural e, aí sim, dissecava-os.
O sagui-anão-de-coroa-preta foi a sensação mundial. Então, ele viveu o ápice da glória. As publicações científicas não se cansaram de elogiá-lo. Quase todos os dias, jornais e revistas estampavam: “Protetor dos animais”, “O bandeirantes da Amazônia”, “O último primatólogo”. De Manaus para o mundo. Os ribeirinhos o saudavam; os políticos o pajeavam; os estudantes de biologia o veneravam. Sim, Roosmarc era visto e considerado como herói do planeta.
Vida simples, com suas vestes quase sempre largas cobrindo o corpo magro e alto, enfiado semanas na floresta, nunca quisera dinheiro, jamais almejara fortuna. O verdadeiro cientista, dizia, quer, antes de tudo, reconhecimento. Não havia prêmio maior do que isso. Sequer gastava o que ganhava. Aprendera com os bichos que, na vida, não se precisa de muitas coisas...
Nascera no sul da Holanda e, aos 17 anos, mudou-se para Amsterdã. Queria estudar biologia. Nos fins do ano 60, a cidade fervilhava, era a capital da contestação. John Lennon e Yoko Ono haviam escolhido a cidade para protestar contra a Guerra do Vietnã. Os rebeldes desfilavam pelas ruas, enquanto John Lennon e Yoko Ono incitavam a quebra de valores deitados uma semana num hotel da cidade, consumindo droga e criando suas canções. O gosto pela contracultura crescia, agigantava-se. Rebelde, Roosmarc desfilava pelas ruas, gritando pela paz, também queimando maconha e outras ervas.
Mas foi, nesta época, que ele se interessou pelos primatas. Depois que terminou a universidade, fez amizade com uma estudante, que também saboreava a contracultura, o desprezo a normas e procedimentos, e com ela, vivendo um romance apaixonado, deu volta ao mundo, como se fosse o famigerado navegante português Vasco da Gama. Estudante de artes plásticas, Marie tinha sede por aventuras: o novo lhe apetecia; o velho não era mais do que um mundo cinzento. A Europa, com seus prédios cinzentos e frios, uma população resignada, não lhe apetecia. Queria quebrar barreiras, outras fronteiras. Não queria apodrecer naquelas cidadezinhas holandesas, onde as mulheres envelheciam rapidamente e só cuidavam de casa. Não queria se transformar num símbolo de cama, fogão e igreja. Menosprezava o título “rainha do lar”, que os pastores tanto veneravam entre a população fiel. Tinha horror ao ver sua mãe de lenço na cabeça e avental cobrindo a gordura da barriga. Se ficasse numa daquelas cidadezinhas, em poucos anos estaria como a mãe – brigava constantemente com o seu pai, saía de casa aos domingos para assistir a mesmice do partor Simeão, e que, rapidamente, voltava para casa para preparar o almoço para os filhos. Que destino! A liberdade a chamava. Não era o que dizia a canção de John Lennon? Ao conhecer Roosmarc, o desejo por aventuras avivou como brasa viva. Quando convidada para segui-lo, e ela queria produzir desenhos e aquarelas jamais vistas no mundo, não titubeou, como se a oportunidade fosse um cavalo encilhado. E cavalo encilhado passa por nós somente uma vez ...
(GONÇALVES, David. Sangue verde. Joinville: Sucesso Pocket, 2014. p. 200-201.Adaptado.)
Analise as afirmativas a seguir:
I- Se dentro do botijão for armazenado um gás perfeito, o volume ocupado pelas suas moléculas e as interações entre elas serão desprezíveis.
II-Pela lei da conservação das massas, a queima de 13 kg de gás de cozinha irá produzir 13 kg de produtos da reação.
III-Em um botijão contendo 31,5 L de um gás perfeito, submetido à pressão de 1 atm e temperatura de 0ºC, haverá aproximadamente 8,5 x 1023 moléculas do referido gás. Dados: número de Avogadro 6,022 x 1023; volume molar 22,4 L/mol.
IV- Supondo-se que um botijão de gás cheio, com 13 kg de uma mistura em estado gasoso composta por 55% de butano e 45% de propano, a pressão parcial desses gases é, respectivamente, de 97 atm e 104 atm. Dados: R = 0,082 atm.L/mol.K; T = 273,15K; V = 31,5 L.
Em relação às proposições analisadas, assinale a única alternativa cujos itens estão todos corretos:
Para diferenciar os hidrocarbonetos etano e eteno em uma mistura gasosa, utiliza-se uma reação com bromo molecular: o etano não reage com esse composto, enquanto o eteno reage de acordo com a seguinte equação química:
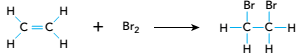
Considere um cilindro de capacidade igual a 10 L, contendo apenas esses hidrocarbonetos em uma mistura com massa igual a 200 g. Ao se adicionar bromo em excesso à mistura, todo o eteno reagiu, formando 940 g de 1,2-dibromoetano.
A concentração inicial de etano, em mol.L–1, no interior do cilindro, corresponde a:

