Questões de Vestibular
Sobre representação das transformações químicas em química
Foram encontradas 889 questões
O sulfato de potássio e o permanganato de potássio são duas importantes substâncias. O sulfato de potássio é utilizado na agricultura como um dos constituintes dos fertilizantes, pois ajuda na adubação das culturas que estão com carência de potássio, ao passo que o permanganato de potássio é utilizado no tratamento da catapora, pois ajuda a secar os ferimentos causados pela doença. A reação a seguir mostra uma maneira de produzir o sulfato de potássio a partir do permanganato de potássio. Considerando as informações apresentadas e a análise da reação não balanceada, assinale a alternativa CORRETA.
Dados: massas atômicas em (g/mol): H= 1, O= 16, S = 32, K = 39, Mn = 55
KMnO4(aq) + H2SO4(aq) + H2O2(aq) → K2SO4(aq) + H2O(l) + MnSO4(aq) + O2(g)
TEXTO 8
IX
Horas depois, teve Rubião um pensamento horrível. Podiam crer que ele próprio incitara o amigo à viagem, para o fim de o matar mais depressa, e entrar na posse do legado, se é que realmente estava incluso no testamento. Sentiu remorsos. Por que não empregou todas as forças, para contê-lo? Viu o cadáver do Quincas Borba, pálido, hediondo, fitando nele um olhar vingativo; resolveu, se acaso o fatal desfecho se desse em viagem, abrir mão do legado.
Pela sua parte o cão vivia farejando, ganindo, querendo fugir; não podia dormir quieto, levantava-se muitas vezes, à noite, percorria a casa, e tornava ao seu canto. De manhã, Rubião chamava-o à cama, e o cão acudia alegre; imaginava que era o próprio dono; via depois que não era, mas aceitava as carícias, e fazia-lhe outras, como se Rubião tivesse de levar as suas ao amigo, ou trazê-lo para ali. Demais, havia-se-lhe afeiçoado também, e para ele era a ponte que o ligava à existência anterior. Não comeu durante os primeiros dias. Suportando menos a sede, Rubião pôde alcançar que bebesse leite; foi a única alimentação por algum tempo. Mais tarde, passava as horas, calado, triste, enrolado em si mesmo, ou então com o corpo estendido e a cabeça entre as mãos.
Quando o médico voltou, ficou espantado da temeridade do doente; deviam tê-lo impedido de sair; a morte era certa.
— Certa?
— Mais tarde ou mais cedo. Levou o tal cachorro?
— Não, senhor, está comigo; pediu que cuidasse dele, e chorou, olhe que chorou que foi um nunca acabar. Verdade é, disse ainda Rubião para defender o enfermo, verdade é que o cachorro merece a estima do dono; parece gente.
O médico tirou o largo chapéu de palha para concertar a fita; depois sorriu. Gente? Com que então parecia gente? Rubião insistia, depois explicava; não era gente como a outra gente, mas tinha coisas de sentimento, e até de juízo. Olhe, ia contar-lhe uma...
— Não, homem, não, logo, logo, vou a um doente de erisipela... Se vierem cartas dele, e não forem reservadas, desejo vê-las, ouviu? E lembranças ao cachorro, concluiu saindo.
Algumas pessoas começaram a mofar do Rubião e da singular incumbência de guardar um cão em vez de ser o cão que o guardasse a ele. Vinha a risota, choviam as alcunhas. Em que havia de dar o professor! sentinela de cachorro! Rubião tinha medo da opinião pública. Com efeito, parecia-lhe ridículo; fugia aos olhos estranhos, olhava com fastio para o animal, dava-se ao diabo, arrenegava da vida. Não tivesse a esperança de um legado, pequeno que fosse. Era impossível que lhe não deixasse uma lembrança.
(ASSIS, Machado de. Quincas Borba. São Paulo: Ática, 2011. p. 30-31.)
Note e adote: Composição aproximada do ar em volume: 80% de N2 e 20% de O2.
Em uma aula experimental, dois grupos de alunos (G1 e G2) utilizaram dois procedimentos diferentes para estudar a velocidade da reação de carbonato de cálcio com excesso de ácido clorídrico. As condições de temperatura e pressão eram as mesmas nos dois procedimentos e, em cada um deles, os estudantes empregaram a mesma massa inicial de carbonato de cálcio e o mesmo volume de solução de ácido clorídrico de mesma concentração.
O grupo G1 acompanhou a transformação ao longo do tempo, realizada em um sistema aberto, determinando a variação de massa desse sistema (Figura 1 e Tabela).
O grupo G2 acompanhou essa reação ao longo do tempo, porém determinando o volume de dióxido de carbono recolhido (Figura 2).
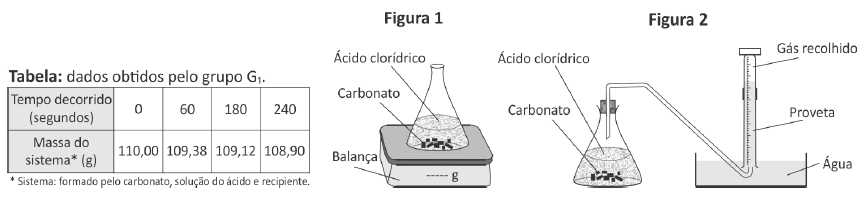
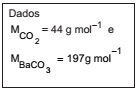
Comparando os dois experimentos, os volumes aproximados de CO2, em litros, recolhidos pelo grupo G2 após 60, 180 e 240 segundos devem ter sido, respectivamente,
Note e adote:
massa molar do CO2: 44 g/mol;
volume molar do CO2: 24 L/mol;
desconsidere a solubilidade do CO2 em água.
Em ambientes naturais e na presença de água e gás oxigênio, a pirita, um mineral composto principalmente por dissulfeto de ferro (FeS2), sofre processos de intemperismo, o que envolve transformações químicas que acontecem ao longo do tempo.
Um desses processos pode ser descrito pelas transformações sucessivas, representadas pelas seguintes equações químicas:
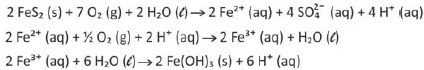
Considerando a equação química que representa a
transformação global desse processo, as lacunas da frase
“No intemperismo sofrido pela pirita, a razão entre as
quantidades de matéria do FeS2(s) e do O2(g) é __________,
e, durante o processo, o pH do solo __________” podem ser
corretamente preenchidas por
O mercúrio é um metal prateado que, em temperatura ambiente, é líquido e inodoro. Quando a temperatura é aumentada, transforma-se em vapor tóxico e corrosivo. Trata-se de produto perigoso à saúde quando inalado, ingerido ou em contato, causando irritação na pele, olhos e vias respiratórias. Uma forma de obtenção de mercúrio se dá por ustulação do sulfeto de mercúrio II (ou cinábrio) segundo a reação:
HgS + O2 → Hg + SO2
Sabendo-se que o sulfeto de mercúrio II possui 70 % de pureza, a massa de mercúrio produzida pela ustulação de uma tonelada do composto é
O hélio é um gás monoatômico, incolor e inodoro,
que apresenta o menor ponto de evaporação de todos os
elementos químicos, e só pode ser solidificado sob
pressão elevada. Embora seja o segundo elemento
químico em abundância no universo, encontram-se, na
atmosfera terrestre, apenas traços provenientes da
desintegração de alguns de seus elementos. Em alguns
depósitos naturais de gás, é encontrado em quantidade
suficiente para a sua exploração. Estima-se que uma
reserva encontrada na Tanzânia contenha mais de 15
bilhões de metros cúbicos desse gás.
Considerando a densidade He = 0.18 kg/m³ , indique o número de átomos do gás hélio existente na reserva.
Dado: Volume de 1 mol de gás na CNTPé 22,4 L
A água oxigenada é o nome dado à solução comercial de peróxido de hidrogênio (H2 O2 ) em água. Em lojas de produtos químicos é possível adquirir frascos contendo água oxigenada 200 volumes. Essa concentração indica que a decomposição total do peróxido de hidrogênio contida em 1,0 L de solução produz 200 L de gás oxigênio medidos na CNTP.
A reação de decomposição da água oxigenada é representada pela equação química a seguir

Desse modo, 50 mL dessa solução contém,
aproximadamente,
I. A pólvora negra é uma mistura de carvão vegetal, nitrato de potássio e enxofre em que predominam substâncias representadas, respectivamente, por: C, KNO3 e S.
II. A neutralização do hidróxido de amônio é representada por: NH4 Cl(s) + H2 O(l) → NH4 + (aq) + OH- (aq) + H+ (aq) + Cl- (aq).
III. A combustão de uma porção de palha de aço é representada pela seguinte equação: 2 Fe(s) + O2(g) → 2 FeO(s)
IV. Os elementos químicos do terceiro período da tabela periódica − que estão, respectivamente, no segundo e terceiro grupos − são representados por: Mg e Al.
De acordo com as informações acima, são corretas apenas as afirmativas
As unidades de concentração podem ser expressas de diferentes formas. Usualmente utilizamos a concentração comum e o título na maioria dos produtos alimentícios e farmacêuticos. Os cálculos químicos estequimétricos, porém, levam em consideração, preferencialmente, a molaridade.
A água oxigenada, por exemplo, tem sua concentração analisada por uma porcentagem ou pelo volume de oxigênio molecular produzido pela decomposição do peróxido de hidrogênio. Considere a análise de uma solução aquosa com 6 % em massa de peróxido de hidrogênio. A concentração aproximada dessa solução expressa em volume de gás oxigênio formado nas CNTP é de
- Volume molar nas CNPT = 22,4 L.
- Considere que 1 litro de água oxigenada libera 10 litros de gás oxigênio (O2), dessa forma, 10 litros de oxigênio é 10 vezes o volume de 1 litro de água oxigenada, por isso ela é chamada de 10 volumes.
- Considere também que a densidade da água oxigenada em questão é de 1 g.cm-3 .
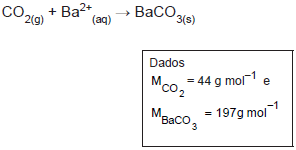
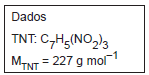
Uma amostra de um composto orgânico foi queimada em atmosfera rica em oxigênio de forma a transformar todo o carbono em gás CO2 . Esse gás foi borbulhado em uma solução de hidróxido de bário, onde todo o CO2 foi precipitado na forma de BaCO3 (ver equação). Se 0,106 g de amostra produziu 0,296 g de BaCO3 , a percentagem (valor mais próximo) de carbono na substância é
CO2(g) + Ba2+(aq) → BaCO3(s)
O titânio é obtido a partir do mineral rutilo (TiO2 ) em duas etapas: a primeira, formando cloreto de titânio a 1000 °C (Equação I); e a segunda, usando magnésio para promover a redução e obter o titânio (Equação II).
TiO2(s) + 2 C(s) + 2 Cl2(g) → TiCl4(g) + 2CO(g) (Equação I)
TiCl4(l) + 2 Mg(s) → Ti(s) + 2 MgCl2(l) (Equação II)
Considere que 6,0 ton de minério produziram massa igual a 2,4 ton de Ti, considerando as reações completas. A porcentagem (valor arredondado mais próximo) de TiO2 originalmente no minério é: