Questões de Vestibular
Sobre representação das transformações químicas em química
Foram encontradas 889 questões
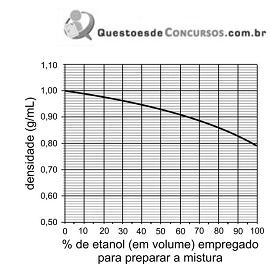
Se 50 mL de etanol forem misturados a 50 mL de água, a 20 °C, o volume da mistura resultante, a essa mesma temperatura, será de, aproximadamente,
Qual é o grau de pureza da amostra?
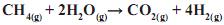
Em relação a este processo, é CORRETO afrmar que, ao reagir
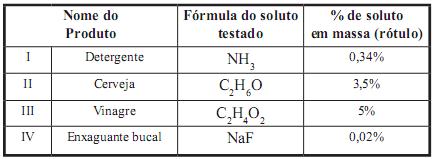
onsiderando que as soluções sejam formadas exclusivamente pelo soluto testado e que suas densidades sejam 1,0 g/mL, o aluno chegou às seguintes conclusões:
I) 1 mol de NH3 em 500 mL de detergente.
II) 21 g de C2 H6 0 em 600 mL de cerveja.
III) 25 g de C2 H4 O2 em 1000 mL de vinagre.
IV) 0,1 mol de NaF em 60 mL de enxaguante bucal.
Assinale a alternativa em que o produto nomeado relaciona CORRETAMENTE a percentagem, em massa, contida no rótulo e os valores encontrados na conclusão do aluno:

Essa afirmação está baseada na lei de:

Assinale abaixo a fórmula molecular correta da glicerina.

Assim, pode-se afirmar que um frasco de vidro contendo 100 mL de mercúrio possui uma massa, em Kg, correspondente a:
I) X H2 + O2 → H2O
II) Ca(OH)2 + H3PO4 → H2O + A
III) Na + ZnCl2 → NaCl + Zn.
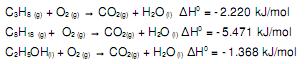
Com base nas fórmulas dos combustíveis e nas equações, considere as afirmativas a seguir:
I) O propano e o noctano são hidrocarbonetos saturados.
II) O noctano é aquele que libera maior quantidade de CO2(g) por mol de combustível
III) A soma dos coeficientes estequiométricos da reação de combustão do etanol é 8.
IV) 50 g de noctano libera maior quantidade de energia do que 100 g de propano.
Estão corretas apenas as afirmativas:
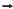 Al 2 O3(s) , não balanceada, pode-se afirmar que a massa de alumínio necessária para produzir 51 g de óxido de alumínio é
Al 2 O3(s) , não balanceada, pode-se afirmar que a massa de alumínio necessária para produzir 51 g de óxido de alumínio é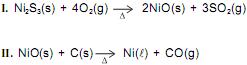
Um dos processos de obtenção do níquel, metal utilizado na fabricação de moedas, consiste, inicialmente, no aquecimento de sulfeto de níquel(III) na presença de ar. Durante esse processo, são formados óxido de níquel(II) e de dióxido de enxofre, de acordo com a equação química I, e, posteriormente, o NiO(s) reage com o carvão, em forno siderúrgico, com obtenção do níquel metálico e do monóxido de carbono, conforme reação representada na equação química II.
Considerando-se as informações do texto e as equações químicas I e II que representam, resumidamente, esse processo, é correto afirmar:
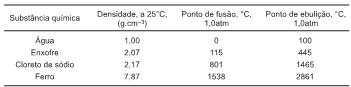
As substâncias químicas têm propriedades bem definidas e, eventualmente, duas substâncias diferentes podem possuir algumas propriedades iguais, mas não todas elas.
Considerando-se essas informações e os dados da tabela que representa algumas propriedades de substâncias químicas, é correto afirmar:
Considere que a análise das cinzas geradas pela queima da casca do fruto de macaúba tenha evidenciado a presença de 0,040 g de óxido de sódio e 0,044 g de óxido de magnésio. Nesse caso, a massa de sódio presente na casca analisada é superior à massa de magnésio.


