Questões de Vestibular
Sobre representação das transformações químicas em química
Foram encontradas 889 questões
2 Se + Sn -> SnSe2
Em um experimento, deseja-se que haja reação completa, isto é, que os dois reagentes sejam totalmente consumidos. Sabendo-se que a massa molar do selênio (Se) é 2/3 da massa molar do estanho (Sn), a razão entre a massa de selênio e a massa de estanho (mSe : mSn), na reação, deve ser de
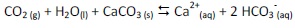
De acordo com essa equação química, dadas as afirmativas seguintes,
I. A reação química é reversível.
II. As espécies químicas presentes no lado dos produtos são chamadas de íons.
III. A equação química não está corretamente balanceada.
IV. A reação química para estar em equilíbrio, a velocidade da reação direta tem que ser igual à velocidade da reação inversa.
verifica-se que estão corretas
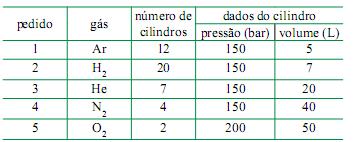
Sabendo que os cilindros rígidos e fechados estão armazenados na mesma condição de temperatura, o pedido que tem maior quantidade de matéria, em mol de gás, é o de número
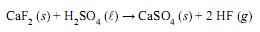
Considere que a massa molar do HF seja igual a 20 g·mol –1 e que a massa molar do CaF2 seja igual a 78 g·mol –1 . Se 100 kg de ácido fluorídrico são obtidos a partir de 260 kg de fluorita impura, é correto afirmar que o teor percentual, em massa, de CaF2 nesse minério é
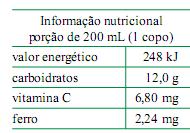
Dada a constante de Avogadro, 6,0 × 1023 mol –1 , é correto afir- mar que 1 litro desse suco contém um número total de espécies de ferro, massa molar 56 g·mol –1 , igual a
Após balancear a equação, pode-se afirmar que a quantidade de
NaOH(aq) + Cl 2 (g) → NaCl(aq) + NaClO(aq) + H2 O(l)
Quando a água sanitária é estocada por longo tempo, o hipoclorito sofre lenta decomposição por meio da reação inversa à de sua produção.
Sobre esse processo, é correto afrmar:
A busca de fontes energéticas sustentáveis e alternativas aos combustíveis fósseis tem sido uma preocupação cada vez mais premente na sociedade contemporânea. A cana-de-açúcar, que no Brasil é empregada há anos para a produção de etanol combustível, promete tornar-se também uma fonte de um novo tipo de diesel, o diesel de cana. Variedades da levedura Saccharomyces cerevisiae, tradicionalmente empregada para produzir o etanol, foram modifcadas para produzir farneseno, um composto que pode ser usado no lugar do diesel. Entre as vantagens de usar o farneseno como um novo diesel está a ausência de enxofre, um elemento poluente que ocorre no diesel do petróleo.
A estrutura do farneseno é mostrada a seguir:
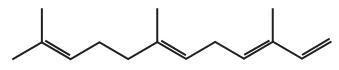
Em relação às informações, é correto afrmar que

Sobre essa tentativa de síntese da quinina de Perkin, é correto afirmar que
Supondo rendimento de 100%, a massa, em gramas, de cloreto de cálcio que deve reagir para produzir 10 g de carbonato de cálcio é, aproximadamente,
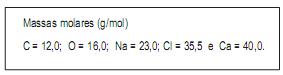
Consultando artigos em revistas especializadas, verificou que, empregando métodos, materiais e reagentes simples, poderia obter, em média, 5 gramas de prata por metro quadrado de chapas de raios X e 5 gramas de prata por litro da solução de fixador.
Para testar essas informações, o jovem decidiu utilizar 10 chapas retangulares de 30 cm x 40 cm e 2 L de solução de fixador.
Caso as informações consultadas estejam corretas, ele deverá obter uma massa total de prata, em gramas, próxima de
Na2CO3(aq) + HCI(aq) ➙ NaCI(aq) + CO2(g) + H2O(L)
Com base na informação, e tendo sido balanceada a equação dada, pode-se afirmar que a concentração molar do HCl é aproximadamente
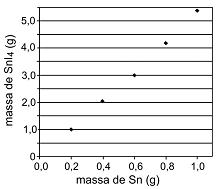
Com base nesses resultados experimentais, é possível afirmar que o valor da relação
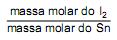
é, aproximadamente,

