Questões de Vestibular
Sobre sistemas homogêneos: constantes: kc e kp. deslocamento do equilíbrio: fatores. em química
Foram encontradas 232 questões
Quando borbulhado em água, o H2S comporta-se como ácido fraco, estabelecendo-se os equilíbrios simultâneos representados pelas equações a seguir:
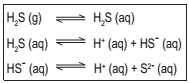
Dentre os procedimentos a seguir, o único que provoca um aumento do escape de sulfeto de hidrogênio de uma solução aquosa para o ar é
PCl3(g) + Cl2(g) PCl5(g)
Sob essas condições, o efeito causado sobre a referida reação é:
TEXTO 2
XX
Os Homens
nesta manhã de sangrenta primavera
parecem não mais saber
o que nunca souberam,
que a Vida é para sempre
sã ou demente
tão de repente
tão de repente!
(VIEIRA, Delermando. Os tambores da tempestade. Goiânia: Poligráfica, 2010. p. 108.)
Hb + O2
 HbO2
HbO2Com base nessas informações, analise as afirmativas a seguir:
I- O sangue, por ser uma solução tampão, não sofrerá alteração de pH, mesmo com a adição de grande quantidade de ácidos ou de bases.
II- O sangue tem pH em torno de 7, e o suco gástrico,em torno de 2. Isso significa uma diferença de concentração de íons hidrônio na ordem de 105.
III- Ao se subir a montanha Everest, a mudança na pressão atmosférica resulta no deslocamento da reação da hemoglobina com o oxigênio para a esquerda.
IV-O CO2 proveniente da respiração celular pode reagir com a água antes de ser transportado pela hemoglobina e ser transformado em íons hidrônio e carbonato (CO32–). A geometria molecular desse ânion é piramidal.
Em relação às proposições analisadas, assinale a única alternativa cujos itens estão todos corretos:
2SO3(g)
 2SO2(g) + O2(g)
2SO2(g) + O2(g)Assinale a alternativa que apresenta, para a reação dada, a expressão da constante de equilíbrio em termos de pressão parcial:
CO2 (aq) + H2O (l)
 H+ (aq) + HCO3– (aq)
H+ (aq) + HCO3– (aq)A diminuição do pH do sangue constitui a acidose, que provoca náusea, vômito e cansaço. O aumento do pH do sangue corresponde à alcalose, que provoca distúrbios respiratórios, cãibras e convulsões. Considere as seguintes afirmações:
I. Pessoas com deficiência respiratória não exalam CO2 suficientemente, com o que a reação deste com H2O se desloca para a esquerda.
II. Pessoas ansiosas respiram rapidamente, eliminando muito CO2 , com o que a reação deste com H2O se desloca para a esquerda.
III. Pessoas com diarreia sofrem grande perda de íons bicarbonato, com o que a reação do CO2 com H2O se desloca para a direita.
É correto o que se afirma em:
NH3 (g) + H2O ( l) ⇌ NH4 + (aq) + OH− (aq)
A liberação de gás amônia ocorrerá com maior intensidade quando a essa solução for adicionado
I. NH4Cl (aq).
II. FeCl3 (aq).
III. NaOH (aq).
Está correto o que consta APENAS em
CO2(g), dissolvido em água, H2CO3 no meio aquoso, e HCO3-, no meio aquoso, encontram-se em equilíbrio de acordo com as representações abaixo:
(I) CO2(aq) + H2O
 H2CO3 (aq)
(II) H2CO3(aq) + H2O
H2CO3 (aq)
(II) H2CO3(aq) + H2O HCO3-(aq) + H3O+(aq)
HCO3-(aq) + H3O+(aq)(III) HCO3- (aq) + H2O
 CO32-(aq) + H3O+(aq)
CO32-(aq) + H3O+(aq)Sobre esse comportamento é correto afirmar que:
O eugenol, extraído de plantas, pode ser transformado em seu isômero isoeugenol, muito utilizado na indústria de perfumes. A transformação pode ser feita em solução alcoólica de KOH.
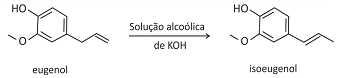
Foram feitos três experimentos de isomerização, à mesma temperatura, empregando-se massas iguais de eugenol e volumes iguais de soluções alcoólicas de KOH de diferentes concentrações. O gráfico a seguir mostra a porcentagem de conversão do eugenol em isoeugenol em função do tempo, para cada experimento.
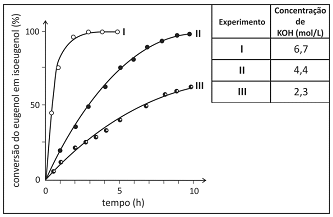
Analisando-se o gráfico, pode-se concluir corretamente que
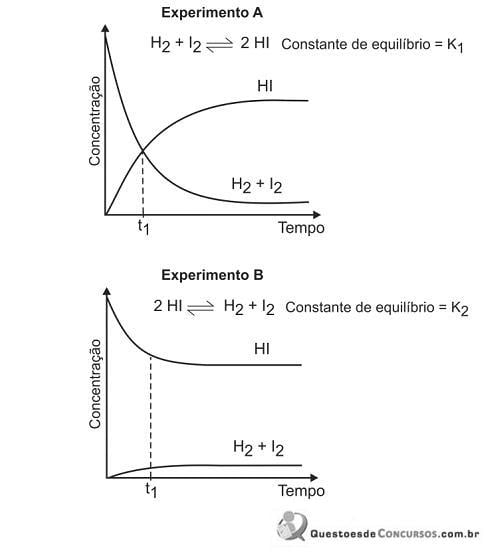
Pela análise dos dois gráficos, pode-se concluir que

A análise do gráfico permite concluir, corretamente, que:
De acordo com a figura e as informações do texto,infere-se que:


Pela análise do texto, é correto afirmar que
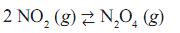
Quando esse recipiente é colocado em um banho de água e gelo, o gás torna- se incolor. Em relação a esse sistema, são feitas as seguintes afirmações:
I. A reação no sentido da formação do gás incolor é exotérmica.
II. Com o aumento da pressão do sistema, a cor castanha é atenuada.
III. Quando o sistema absorve calor, a cor castanha é acentuada.
Dentre as afirmações, as corretas são:
4 NH3(g) + 5 O2(g) 4 NO(g) + 6 H2O(g) ΔH = -900KJ
Sobre a reação, é correto afirmar que:

Considerando as informações acima, julgue os itens 50 e 51, assinale a opção correta no item 52, que é do tipo C, e faça o que se pede no item 53, que é do tipo D.
O lança-perfume é uma droga inalante consumida principalmente no Carnaval. É constituído por solventes voláteis que, quando inalados, são levados, via corrente sanguínea, para todo o organismo. Por induzir a produção de adrenalina no organismo, a droga acelera a frequência cardíaca, proporcionando sensação de euforia e desinibição, ao mesmo tempo em que confere
perturbações auditivas e visuais, perda de autocontrole e visão confusa. O cloreto de etila
 e o éter dietílico
e o éter dietílico  , componentes principais do lança-perfume, podem ser sintetizados a partir do
, componentes principais do lança-perfume, podem ser sintetizados a partir do  , de acordo com as
, de acordo com asreações a seguir.

Considerando as reações acima e os valores de entalpias padrão de
formação —
 — a 25 ºC, apresentados na tabela, julgue os itens seguintes.
— a 25 ºC, apresentados na tabela, julgue os itens seguintes.  . Sabendo que as concentrações de N2 e O2 no equilíbrio acima, a 800 °C, são iguais a 0,10 mol L-1 para ambos, calcule a concentração molar de NO no equilíbrio se K = 4,0 x 10-20 a 800 °C.
. Sabendo que as concentrações de N2 e O2 no equilíbrio acima, a 800 °C, são iguais a 0,10 mol L-1 para ambos, calcule a concentração molar de NO no equilíbrio se K = 4,0 x 10-20 a 800 °C.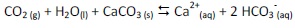
De acordo com essa equação química, dadas as afirmativas seguintes,
I. A reação química é reversível.
II. As espécies químicas presentes no lado dos produtos são chamadas de íons.
III. A equação química não está corretamente balanceada.
IV. A reação química para estar em equilíbrio, a velocidade da reação direta tem que ser igual à velocidade da reação inversa.
verifica-se que estão corretas

