Questões de Vestibular
Sobre transformações químicas e energia em química
Foram encontradas 975 questões
Com relação à pilha Fe0 /Fe2+║Cu2+/Cu0 , assinale o que for correto.
Dados:
Fe2+ + 2e- → Fe0 E0
= - 0,44 V
Cu2+ + 2e- → Cu0 E0 = + 0,34 V
Com relação à pilha Fe0 /Fe2+║Cu2+/Cu0 , assinale o que for correto.
Dados:
Fe2+ + 2e- → Fe0 E0
= - 0,44 V
Cu2+ + 2e- → Cu0 E0 = + 0,34 V
Com relação à pilha Fe0 /Fe2+║Cu2+/Cu0 , assinale o que for correto.
Dados:
Fe2+ + 2e- → Fe0 E0
= - 0,44 V
Cu2+ + 2e- → Cu0 E0 = + 0,34 V
Com relação à pilha Fe0 /Fe2+║Cu2+/Cu0 , assinale o que for correto.
Dados:
Fe2+ + 2e- → Fe0 E0
= - 0,44 V
Cu2+ + 2e- → Cu0 E0 = + 0,34 V
Com relação à pilha Fe0 /Fe2+║Cu2+/Cu0 , assinale o que for correto.
Dados:
Fe2+ + 2e- → Fe0 E0
= - 0,44 V
Cu2+ + 2e- → Cu0 E0 = + 0,34 V
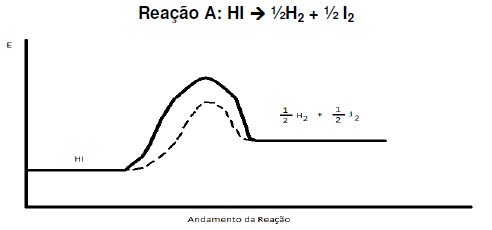
Considere a reação de combustão de 1,0 mol de eteno (C2H4), a 25 o C e 1,0 atm, conforme a equação a seguir:
(Dado: volume molar nas CNTP = 22,4 L)

Considere a reação de combustão de 1,0 mol de eteno (C2H4), a 25 o C e 1,0 atm, conforme a equação a seguir:
(Dado: volume molar nas CNTP = 22,4 L)

Considere a reação de combustão de 1,0 mol de eteno (C2H4), a 25 o C e 1,0 atm, conforme a equação a seguir:
(Dado: volume molar nas CNTP = 22,4 L)

Considere a reação de combustão de 1,0 mol de eteno (C2H4), a 25 o C e 1,0 atm, conforme a equação a seguir:
(Dado: volume molar nas CNTP = 22,4 L)

Considere a reação de combustão de 1,0 mol de eteno (C2H4), a 25 o C e 1,0 atm, conforme a equação a seguir:
(Dado: volume molar nas CNTP = 22,4 L)
1. A primeira célula (I) contém uma solução de AgNO3 entre dois eletrodos de prata;
2. A segunda (II) contém uma solução de um único sal de ouro (onde o nox do ouro é desconhecido) entre dois eletrodos de ouro.
Deixando a corrente passar durante certo tempo por este conjunto, observa-se que no catodo da célula (I) são depositados 1,079 g de prata, enquanto no catodo de célula (II) são depositados 0,657 g de ouro. Sabendo que no cátodo de cada célula ocorre somente um tipo de reação, qual das opções a seguir contém a afirmação FALSA em relação aos procedimentos e informações relacionados com a questão?
Dados: (1F = 96.500C).
Marque a opção correta:
Durante a última parte da viagem, Eduardo pega um pacote contendo 40g de biscoito e lê o rótulo. A tabela que Eduardo vê foi adaptada e está representada a seguir:
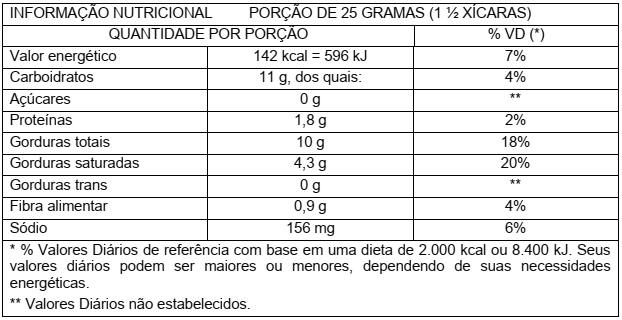
Considere que o total de gordura refere-se apenas a triglicerídeos. Com base nas informações acima, assinale a proposição CORRETA.
Segundo o rótulo do produto, seriam necessários mais de 30 pacotes de biscoito para suprir
a necessidade energética.
Após o problema da bateria ter sido resolvido, eles continuaram a viagem. Percorridos alguns quilômetros Carlos precisou frear bruscamente o veículo, devido a um acidente ocorrido na rodovia. Passado o susto, Eduardo pergunta com ironia:
- Seu carro tem airbag?
- É obvio que não, responde Carlos.
- Você saberia me dizer como funciona um airbag?
- Não tenho ideia. O que você acha de consultarmos aquele livro de Química?
- Legal!
Então, Eduardo estica a mão e pega, no banco de trás, um livro no qual se lê:
O airbag é formado por um dispositivo que contém a mistura química de NaN3 (azida de sódio), KNO3 e SiO2 que é responsável pela liberação do gás. Esse dispositivo está acoplado a um balão que fica no painel do automóvel e quando ocorre uma colisão (ou desaceleração), os sensores localizados no para-choque do automóvel transmitem um impulso elétrico (faísca) que causa a detonação da reação. Em aproximadamente 25 milésimos de segundo, o airbag está completamente inflado.
Veja as equações do processo:
I - 2 NaN3 → 2 Na + 3N2
II - 10 Na + 2 KNO3 → K2O + 5 Na2O + N2
III - K2O + Na2O + SiO2 → silicato alcalino
Dado: um airbag contém aproximadamente 130 g de azida.
Disponível em: <http://www.brasilescola.com/quimica/air-bag-reacao-decomposicao.htm> (adaptado) Acesso em: 12 set. 2011.
Assinale a proposição CORRETA.
Em contato com a água, o sódio metálico reage gerando um forte aquecimento, fenômeno
típico de uma reação endotérmica.
Após o problema da bateria ter sido resolvido, eles continuaram a viagem. Percorridos alguns quilômetros Carlos precisou frear bruscamente o veículo, devido a um acidente ocorrido na rodovia. Passado o susto, Eduardo pergunta com ironia:
- Seu carro tem airbag?
- É obvio que não, responde Carlos.
- Você saberia me dizer como funciona um airbag?
- Não tenho ideia. O que você acha de consultarmos aquele livro de Química?
- Legal!
Então, Eduardo estica a mão e pega, no banco de trás, um livro no qual se lê:
O airbag é formado por um dispositivo que contém a mistura química de NaN3 (azida de sódio), KNO3 e SiO2 que é responsável pela liberação do gás. Esse dispositivo está acoplado a um balão que fica no painel do automóvel e quando ocorre uma colisão (ou desaceleração), os sensores localizados no para-choque do automóvel transmitem um impulso elétrico (faísca) que causa a detonação da reação. Em aproximadamente 25 milésimos de segundo, o airbag está completamente inflado.
Veja as equações do processo:
I - 2 NaN3 → 2 Na + 3N2
II - 10 Na + 2 KNO3 → K2O + 5 Na2O + N2
III - K2O + Na2O + SiO2 → silicato alcalino
Dado: um airbag contém aproximadamente 130 g de azida.
Disponível em: <http://www.brasilescola.com/quimica/air-bag-reacao-decomposicao.htm> (adaptado) Acesso em: 12 set. 2011.
Assinale a proposição CORRETA.
Na reação representada pela equação I, o sódio se oxida e o nitrogênio se reduz.