Questões Militares
Sobre eletroquímica: oxirredução, potenciais padrão de redução, pilha, eletrólise e leis de faraday. em química
Foram encontradas 195 questões
O esquema abaixo, ilustra uma pilha eletroquímica conhecida como Pilha da Daniell.
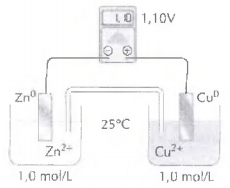
Assinale a opção correta com relação ao processo eletroquímico que ocorre na pilha de Daniell.
Observe a tabela a seguir.
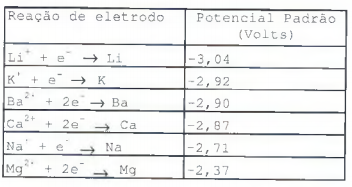
O potencial padrão de eletrodo é uma expressão quantitativa
da facilidade com que um elemento perde elétrons. A tabela
acima exibe valor do potencial padrão de eletrodos de metal.
Sendo assim, é correto afirmar que o agente redutor mais
forte do Cálcio é o:
Observe a figura a seguir.
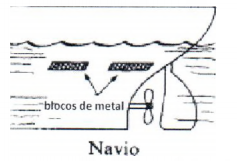
Para proteger da corrosão os cascos de navios, que são constituídos basicamente de ferro, é comum utilizarem-se blocos de um metal acoplados ao casco, conhecidos como metais de sacrifício, conforme representado na figura acima.
Dados:
Potenciais Padrão de Redução:
Fe2+ + 2e ↔ Fe E° = -0,44V
Cu2+ + 2e ↔ Cu E° = +0,34V
Zn2- + 2e ↔ Zn E° = -0,76V
Ni2+ + 2e ↔ Ni E° = -0,25V
Ag+ + e ↔ Ag E° = +0,79V
Pb2+ + 2e ↔ Pb E° = -0,13V
Utilizando os valores de potenciais acima relacionados, qual
é o metal de sacrifício que oferecerá melhor proteção ao
casco do os valores do navio?
Sabendo-se que
( 1 ) Mg → Mg2+ + 2e- com E10 = 2,37 V, e
( 2 ) Sn2+ + 2e- → Sn com E20 = -0,14 V,
Em que E10 e E20 são as tensões elétricas decorrentes dessas reações, respectivamente, calcule a tensão obtida na reação abaixo.
Mg(s) + Sn2+ → Mg2+ + Sn
Sendo assim, assinale a opção correta.
Pb(s) + PbO2(s) + 2H2SO4(aq) → 2Pb2+ SO4 2- (aq) + 2H2O(ℓ)
É de 0,76 V a força eletromotriz padrão, E°, de uma célula eletroquímica, conforme a reação
Zn(s) + 2H+ (aq) → Zn2+ (aq) + H2 (g).
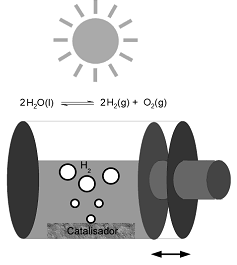
Recentemente, a produção fotocatalítica de hidrogênio vem atraindo atenção devido ao processo que gera um combustível limpo, o qual é utilizado em células a combustível. O processo se baseia na separação da água nos seus componentes, conforme equilíbrio inserido no esquema, utilizando luz solar e um fotocatalisador (p. ex. NaTaO3:La). O processo é extremamente endotérmico, necessitando 1,23 eV para ocorrer. Num experimento, o processo foi realizado num sistema fechado, como esquematizado abaixo. Considerando essas informações, identifique as afirmativas a seguir como verdadeiras (V) ou falsas (F):
( ) A quantidade de fotocatalisador limita a conversão.
( ) O aumento da temperatura irá favorecer a conversão.
( ) A diminuição do volume do sistema irá favorecer a conversão.
( ) É condição necessária para a produção de hidrogênio que o fotocatalisador absorva energia solar superior a 1,23 eV.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
1a Etapa: o composto A (C7H6O) sofre oxidação em solução básica de permanganato de potássio. O produto gerado, após neutralizado, é o ácido benzoico;
2a Etapa: o ácido benzoico reage com etanol em solução ácida, produzindo o composto B e água;
3a Etapa: o composto B sofre forte redução com hidreto de lítio-alumínio em éter, gerando dois produtos que, depois de neutralizados, formam então o composto C e o etanol.
Considerando as etapas supracitadas, são feitas as seguintes afirmações:
I) o composto A e o composto C são isômeros.
II) o composto B é um éster.
III) o composto B é o acetato de benzila.
Com base na análise das afirmações acima, assinale a opção correta.
As equações que representam as semirreações de cada espécie e os respectivos potenciais- padrão de redução (25 ºC e 1 atm) são apresentadas a seguir.
Zn2+(aq) + 2 e- → Zn (s) Eo = - 0,76 V
Ag+ (aq) + 1 e- → Ag (s) Eo = + 0,80 V
Com base nas informações apresentadas são feitas as afirmativas abaixo.
I – No eletrodo de zinco ocorre o processo químico de oxidação.
II – O cátodo da pilha será o eletrodo de prata.
III – Ocorre o desgaste da placa de zinco devido ao processo químico de redução do zinco.
IV – O sentido espontâneo do processo será Zn+2 + 2 Ago → Zno + 2 Ag+
V – Entre os eletrodos de zinco e prata existe uma diferença de potencial padrão de 1,56 V.
Estão corretas apenas as afirmativas
Realiza-se a eletrólise de uma solução aquosa diluída de ácido sulfúrico com eletrodos inertes durante 10 minutos. Determine a corrente elétrica média aplicada, sabendo-se que foram produzidos no catodo 300 mL de hidrogênio, coletados a uma pressão total de 0,54 atm sobre a água, à temperatura de 300 K.
Considere:
• Pressão de vapor da água a 300 K = 0,060 atm;
• Constante de Faraday: 1 F = 96500 C.mol–1;
• Constante universal dos gases perfeitos: R = 0,08 atm.L.K–1.mol–1
.
Considere uma célula a combustível alcalina (hidrogênio-oxigênio) sobre a qual são feitas as seguintes afirmações:
I. Sob condição de consumo de carga elétrica, a voltagem efetiva de serviço desse dispositivo eletroquímico é menor que a força eletromotriz da célula.
II. O combustível (hidrogênio gasoso) é injetado no compartimento do anodo e um fluxo de oxigênio gasoso alimenta o catodo dessa célula eletroquímica.
III. Sendo o potencial padrão dessa célula galvânica igual a 1,229 VEPH (volt na escala padrão do hidrogênio), a variação de energia livre de Gibbs padrão (∆G°) da reação global do sistema redox atuante é igual a − 237,2 kJ ∙ mol−1.
Das afirmações acima, está(ão) CORRETA(S) apenas
As pilhas ou baterias que possuem o lítio como principal constituinte têm como uma de suas características o fato de serem leves, pois o lítio é o metal menos denso descoberto até o momento.
Considere as semi-reações: Li (s) +1 + e-
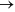 Li (s) E0 = -3, 05 V
Ag(aq)+1 + e-
Li (s) E0 = -3, 05 V
Ag(aq)+1 + e- 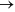 Ag (aq) E0 = +0,80 V
Ag (aq) E0 = +0,80 V
Se uma pilha é composta pelos dois elementos químicos acima, pode-se afirmar que o elemento que constitui o ânodo da reação eletroquímica espontânea e o Potencial da pilha são dados, respectivamente, por:
Baseando-se nos potenciais padrão de redução das semi-reações a seguir, são feitas as seguintes afirmativas:
Sn 2+ (aq) + 2 e- → Sn (s) E0 red = - 0,14 V
Li+ (aq) + 1 e- → Li (s) E0 red = - 3,04 V
I-O estanho cede elétrons para o lítio.
II-O eletrodo de estanho funciona como cátodo da pilha.
III-A reação global é representada pela equação: 2 Li0 (s)+ Sn2+ (aq) → Sn0 (s) + 2 Li+ (aq)
IV-No eletrodo de estanho ocorre oxidação.
V-A diferença de potencial teórica da pilha é de 2,90 V, (∆E = + 2,90 V).
Das afirmativas apresentadas estão corretas apenas:
Quando a temperatura cai, o reluzente estanho metálico exposto ao oxigênio do ar começa a se tornar friável e a se esboroar (desfazer) num pó acinzentado e não metálico - continua sendo estanho, mas com forma estrutural diferente”. (Adaptado de Os Botões de Napoleão - Penny Le Couteur e Jay Burreson - Pag 8).
I – o texto faz alusão estritamente a ocorrência de fenômenos físicos.
II – o texto faz alusão a ocorrência de uma reação de oxidação do estanho do botão.
III – o texto faz alusão a ocorrência de uma reação de síntese.
IV – o texto faz alusão a ocorrência de uma reação sem transferência de elétrons entre espécies estanho metálico e o oxigênio do ar.
Das afirmativas apresentadas estão corretas apenas:
nessa peça foi de
Dados:
massas atômicas Cr = 52 u e Cl = 35,5 u.
1 Faraday = 96500 C/mol de e-