Questões de Concurso
Sobre eletroquímica: oxirredução, potenciais padrão de redução, pilha, eletrólise e leis de faraday. em química
Foram encontradas 659 questões
As bactérias redutoras de sulfato (BRS) têm grande importância na biocorrosão. Embora, até o momento não exista a determinação de um mecanismo único de corrosão ocasionado pela ação das BRS, Kuhr e Vlug (1934) propuseram um mecanismo no qual essas bactérias utilizam o hidrogênio proveniente do consumo realizado pela hidrogenase, catalisando a ativação reversível de hidrogênio. Em condições anaeróbicas, essa reação de corrosão é a evolução de hidrogênio pela dissociação da água, em que os íons de hidrogênio produzidos se encontram adsorvidos sobre a superfície metálica, sendo posteriormente consumidos pelo processo metabólico, como mostra a figura abaixo:
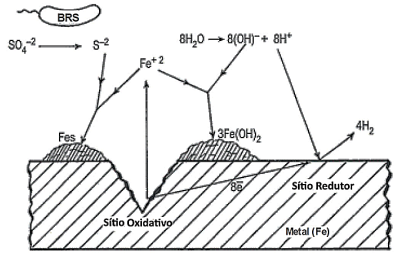
De acordo com o que mostra a figura e a descrição do mecanismo de corrosão supracitado, esse tipo de biocorrosão é classificado como
Julgue o próximo item, a respeito da equação de Nernst e de potencial de eletrodo, eletrodos indicadores e medidas de pH.
Potencial de eletrodo é a medida do potencial individual de
um eletrodo reversível no estado-padrão, ou seja, solutos em
concentração de 1 mol/kg e gases à pressão de 1 bar, ambos
a 273 K.
Julgue o próximo item, a respeito da equação de Nernst e de potencial de eletrodo, eletrodos indicadores e medidas de pH.
Para determinar a capacidade de um metal em atuar como anodo de sacrifício, é adequado montar um eletrodo com o referido metal, com potencial desconhecido, ligá-lo a um eletrodo de potencial conhecido e medir a diferença de potencial entre os eletrodos. Nesse contexto, pode-se usar, para a avaliação, um eletrodo de zinco metálico (Zn), que, em uma célula eletroquímica com solução 1 mol/L de ZnSO4, apresenta a seguinte semirreação no anodo.
Zn (s) → Zn2+ (aq) + 2 e−
Julgue o próximo item, a respeito da equação de Nernst e de potencial de eletrodo, eletrodos indicadores e medidas de pH.
A equação de Nernst tem por finalidade prever o potencial
de uma pilha durante o seu funcionamento, correlacionando
a variação do potencial da pilha em certo instante da reação
com a variação das concentrações de produtos e reagentes.
Julgue o próximo item, a respeito da equação de Nernst e de potencial de eletrodo, eletrodos indicadores e medidas de pH.
O pH é uma medida que indica o grau de acidez,
neutralidade ou alcalinidade de uma solução e varia de 0 a
14: se o pH for menor que 7, a solução será ácida; acima de
7, será básica; e na faixa de 6 até 8, será neutra.
Uma corrente elétrica que percorre um condutor gera, em torno desse condutor, um campo magnético com direção determinada pela regra da mão esquerda.
2 H2O ⇌ 2 H2 + O2
Considerando a reação de eletrólise da água mostrada acima, e sabendo que ZH = 1, ZO = 8, ZP = 15, MH = 1,0 g/mol, MO = 16,0 g/mol e que R = 0,082 atm ∙ L ∙ K−1 ∙ mol−1 é a constante universal dos gases perfeitos, julgue o item que se segue.
Supondo que todo o oxigênio produzido na eletrólise seja
lançado na atmosfera, então, a 1 atm de pressão e 298 K de
temperatura, uma tonelada de água submetida à eletrólise
lançará mais de 500.000 L de oxigênio na atmosfera.
2 H2O ⇌ 2 H2 + O2
Considerando a reação de eletrólise da água mostrada acima, e sabendo que ZH = 1, ZO = 8, ZP = 15, MH = 1,0 g/mol, MO = 16,0 g/mol e que R = 0,082 atm ∙ L ∙ K−1 ∙ mol−1 é a constante universal dos gases perfeitos, julgue o item que se segue.
Uma tonelada de água produzirá menos de 120 kg de
hidrogênio em uma eletrólise.
Assinale a alternativa que cujas palavras ou expressões completam corretamente as lacunas da frase.
Julgue o seguinte item, em relação à eletroquímica.
O potencial da semirreação representada a seguir não depende do pH.
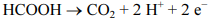
Julgue o seguinte item, em relação à eletroquímica.
Os potenciais-padrão das semirreações de oxirredução são
medidos com base no eletrodo-padrão de hidrogênio, cujo
valor estabelecido é 0,00 V.
Julgue o seguinte item, em relação à eletroquímica.
Considerando-se os potenciais de redução 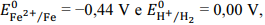 é correto afirmar que
um prego de ferro colocado em uma solução de HCl 1 mol/L
permanece em seu estado inalterado.
é correto afirmar que
um prego de ferro colocado em uma solução de HCl 1 mol/L
permanece em seu estado inalterado.
Segundo a IUPAC, a dupla barra vertical na notação das pilhas eletroquímicas representa a ponte salina.
A Lei de Faraday da eletrólise enuncia que “a quantidade do produto formado ou do reagente consumido por uma corrente elétrica é estequiometricamente equivalente à quantidade de elétrons fornecidos”. Pode-se afirmar, portanto, que a quantidade (em mols) de Al(s) que pode ser produzida a partir do alumínio no composto Al2O3, se 5 mols de elétrons forem fornecidos, é aproximadamente:
(ATKINS; JONES, Princípios de Química: questionando a vida moderna e o meio ambiente, Editora Bookman, 2006)
O ácido ascórbico (AA) é uma cetolactona, presente em frutas cítricas, tomate e vegetais de folhas verdes. O AA atua em reações de oxirredução em pelo menos 10 sistemas enzimáticos e na captura de radicais livres:
C6H8O6 + 2H+ + 2NO2 ⟶ C6H6O6 + 2H2O + 2NO
Qual dos seguintes pares identifica os agentes redutores e oxidantes, respectivamente?
A análise titrimétrica desempenha um papel importante na análise quantitativa. Os diferentes métodos titrimétricos são classificados em função das reações que ocorrem durante a titulação. O permanganato de potássio, o ácido etilenodiaminotetracético e o cloreto de prata são comumente empregados, respectivamente, nas análises titrimétricas denominadas reações de:
Um analista utilizou para a determinação de Fe3+ uma solução de Mg-EDTA. Em uma primeira etapa, ocorre a seguinte reação:
Fe3+ + MgY2- → FeY- + Mg2+
Posteriormente, os íons Mg2+ são titulados com solução padrão de EDTA. Assinale a opção que apresenta o nome correto do procedimento adotado para essa titulação com EDTA.
Considere a pilha galvânica Cd(s)|Cd(NO3)2(aq)||AgNO3(aq)|Ag(s).
Os potenciais-padrão de redução, de cada meia-célula, em relação ao Eletrodo Padrão de Hidrogênio são dados abaixo:
Cd2+(aq) + 2e- → Cd(s) Eº = -0,402 V
Ag+(aq) + e- → Ag(s) Eº = +0,799 V
Sabe-se que o potencial padrão de redução do eletrodo de calomelano em relação ao eletrodo padrão de hidrogênio é +0,268 V.
Assim, assinale a opção que apresenta o potencial de redução do cátodo da pilha supracitada em relação ao eletrodo de calomelano, em Volts.
Observe a figura abaixo e considere a seguinte reação de eletrólise de NaCI aquoso 1 mol L-1:
Semicélula: 2Cl-(aq) → Cl2(g) + 2e-
Semicélula: 2e- + 2H2O → H2(g) + 2OH-(aq)
Célula: 2H2O(aq) + 2Cl-(aq) → H2(g) + Cl2(g) + 2OH-(aq)
Com base nas informações pode-se afirmar que:
Considere a célula eletroquímica abaixo.
A diferença de potencial elétrico da célula é dada por: E= 0,5580 + 0,05916 log([Ag+]), em Volts.
Na titulação de 30mL de uma solução de KCI 0,4M foi usada uma solução de AgNO3 0,15M. Sabendo que a diferença de potencial elétrico foi medida pela célula acima, assinale a opção que apresenta o valor da diferença de potencial elétrico, em Volts, após a adição de 20ml da solução de AgNO3.
Dado: KPS,AgCI = 1,8 x 10-10