Questões de Concurso
Sobre termoquímica: energia calorífica, calor de reação, entalpia, equações e lei de hess. em química
Foram encontradas 453 questões
Julgue o item a seguir, relativo à termoquímica e a assuntos correlatos.
A termoquímica refere‐se ao estudo das transferências de calor que ocorrem durante as transformações químicas.
Qual o ∆H° para a seguinte reação química a 25°C?
NH3 (g) + HCl (g) → NH4Cl (s)
Utilize, nesta questão, os seguintes calores molares de formação:
1/2 N2(g) + 3/2 H2 (g) → NH3(g) ∆H° f = -46,1 kJ/mol
1/2 H2(g) + 1/2 Cl2 (g) → HCl(g) ∆H° f = -92,3 kJ/mol
1/2 N2(g) + 2 H2 (g) + 1/2 Cl2 (g) → NH4Cl(s)
∆H° f = -314,4 kJ/mol
Dados: calor específico da água (c) = 4,18 J/goC.
I. Em uma reação endotérmica, a entalpia do sistema reativo cresce, ou seja, a entalpia dos produtos é maior do que a entalpia dos reagentes. II. A lei da conservação de energia estabelece que a energia não é criada nem destruída em uma mudança de estado físico. III. A variação de entalpia da reação depende do caminho que as reações ocorrem – Lei de Hess.
Está(Estão) correta(s) a(s) afirmativa(s)
gás N2O que provocou em Humpry Davyum irresistível desejo de rir recebendo o nome degás hilariante, decompõe-se isotermicamente a 27 °C de acordo com a reação:N2O(g) → N2(g) + ½ O2(g).
Sabendo-se que a variação de entalpia é–20 kcal/mol e a variação de entropia é18 cal/K.mol, é correto afirmar que
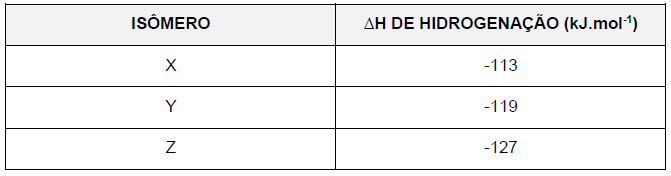
Sobre esses isômeros, é correto afirmar que
O valor da variação de entropia da vizinhança desse sistema a 25°C, em J.K-1 , é:
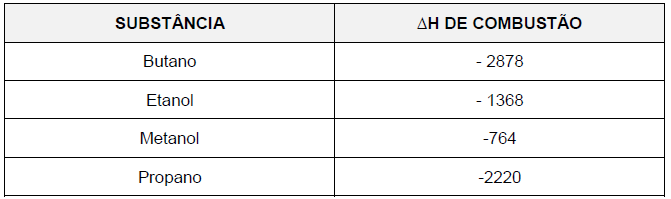
O combustível que lança na atmosfera a maior quantidade de gás poluente, para uma mesma quantidade de energia produzida, é
A seguir são apresentadas informações referentes à reação de decomposição do H2O2.


Considerando que a reação de decomposição do H2O2 seja exotérmica e se processe de acordo com uma cinética de primeira ordem, e que a constante universal dos gases seja igual a 8,3 J × mol-1 × K-1 , julgue o item subsequente, acerca da reação em questão.
As entalpias padrão de ligação fornecidas permitem determinar que a decomposição de 1,00 mol de H2O2, quando realizada à pressão constante de 1 bar e a 25 ºC, libera quantidade de calor superior a 100 kJ.
A seguir são apresentadas informações referentes à reação de decomposição do H2O2.


Considerando que a reação de decomposição do H2O2 seja exotérmica e se processe de acordo com uma cinética de primeira ordem, e que a constante universal dos gases seja igual a 8,3 J × mol-1 × K-1 , julgue o item subsequente, acerca da reação em questão.
A reação de decomposição do H2O2 libera maior quantidade de calor quando é realizada à pressão constante de 1 bar do que quando é realizada a volume constante.


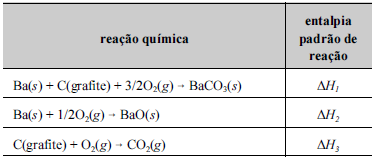
Tendo como referência a figura e os dados da tabela precedentes, julgue o item a seguir.
Se, na queima de um artefato pirotécnico ocorrera decomposição do carbonato de bário, de acordo coma reação química BaCO3(s) → BaO(s) + CO2(g), entãoa entalpia padrão dessa reação de decomposição (ΔHx),calculada a partir dos dados listados na tabela seguinte,será ΔHx = ΔH1 - ΔH2 + ΔH3.
( ) Se ΔG = 0, a reação não ocorre. ( ) Uma reação espontânea ocorre em qualquer sentido (direto e indireto). ( ) Se ΔG < 0, a reação é espontânea no sentido direto (reagentes→ produtos). ( ) Se ΔG > 0, a reação é espontânea no sentido indireto (produtos→reagentes).
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
N2O5(g) + H2O(l) → 2 HNO3(aq)
Utilizando as equações termoquímicas:
N2(g) + 3 O2(g) + H2(g) → 2 HNO3(aq) ∆H= – 415 kJ 2 H2(g) + O2(g) → 2 H2O (l) ∆H= – 572 kJ 2 N2(g) + 5 O2(g) → 2 N2O5(g) ∆H = + 22 kJ
Assinale a alternativa que contém o valor da entalpia envolvida na obtenção de quatro mols de ácido nítrico:
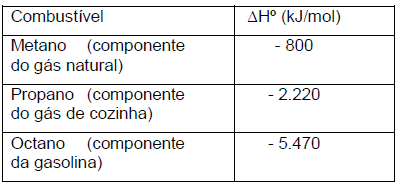
Com base nesses dados, são feitas as seguintes afirmativas:
I. O poder calorífico do Propano é maior que do Octano. II. A queima de um mol de Metano absorve cerca de 50 kJ de energia. III. A energia proveniente da queima de 1 kg de Metano é cerca de 2,8 vezes menor que a energia da queima de 1 kg de Propano.
Assinale a alternativa em que toda(s) a(s) afirmativa(s) está(ão) CORRETA(S):
CH4 (g) + 2 O2 (g) → CO2 (g) + 2 H2O (g) ΔH1 CH4 (g) + 2 O2 (g) → CO2 (g) + 2 H2O (l) ΔH2
Assinale a alternativa que apresenta a relação entre essas variações de entalpia.
Texto para a questão.
Curvas de solubilidade em água em função da temperatura para algumas substâncias
