Questões de Concurso Público Transpetro 2018 para Engenheiro Júnior - Processamento (Químico)
Foram encontradas 70 questões
Qual o limite para o aumento do ganho K, em dB, até que o sistema se torne instável?
Qual é a vazão de refrigeração nesse ciclo frigorífico?
Qual o valor da nova constante de tempo do sistema?
Qual o valor do coeficiente de transferência de calor na região hidrodinâmica e termicamente desenvolvida?
Dado k = 0,03 W/(m.s), ν = 20 x 10-6 m2 /s NuT = 3,657
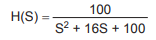
Qual o valor do tempo de acomodação do sistema para o critério de 2%?
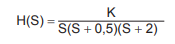
Qual o erro estático de posição do sistema, se a temperatura do forno permanecer constante e o ganho K for dobrado?
A primeira camada da parede tem espessura de 9 cm e é formada de fibra de vidro cuja condutividade térmica é 0,03 W m-1 oC-1. A segunda camada da parede tem espessura de 14 cm e é formada de tijolos cuja condutividade térmica é 0,7 W m-1 oC-1. A área da parede é 4 m2. A temperatura na superfície da parede em contato com o interior da unidade industrial é 85 oC, e a temperatura na superfície da parede em contato com o meio externo é 35 oC.
O fluxo de calor estabelecido através da parede, em J s-1, é igual a
Assumindo-se o comportamento de gás ideal para o H2, o trabalho de expansão realizado por esse gás, em kJ, é igual a
Dado Constante dos gases: 8,31 J mol-1 K-1 ln 2 = 0,69 Massa molar H2 : 2 g mol-1
Esse Número é função das seguintes grandezas: μ = viscosidade dinâmica [kg s-1m-1] Cp = calor específico a pressão constante [ J kg-1 K-1] K = condutividade térmica [W m-1 K-1]
A expressão que define o Número de Prandtl corresponde a
A fração molar do CO2 na mistura é igual a
A massa da amostra, em gramas, de N2 líquido que evaporou é igual a
Dado Massa molar do N2 : 28 g mol-1
A massa de H2S presente no reservatório corresponde a
Dado Massa molar do H2S: 34 g mol-1
A pressão parcial de CH4 nessa mistura é igual a
A corrente X é encaminhada para a segunda etapa, sendo separada em duas novas correntes: W e Z. A corrente W tem vazão de 80 kg h-1 e contém 95% de A. Por sua vez, a corrente Z tem vazão de 20 kg h-1 e contém 20% de A.
A concentração percentual de A na corrente de alimentação é igual a
Em uma etapa posterior, o reagente em excesso que não participou da reação é recuperado, sendo completamente separado do produto formado. A vazão de reagente recuperado, em kg h-1, é igual a
Dado Massas molares: C2H4 : 28 g mol-1, H2 : 2g mol-1
da = –sdT – Pdv
Utilizando-se as relações de Maxwell e a equação de estado do gás ideal (PV = RT), a relação (∂s/∂v)T para um gás ideal é
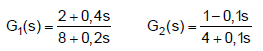
Para controle dessas malhas, um engenheiro deve levar em consideração vários fatores, como estabilidade, margem de fase, ganho, entre outros.
Nesse caso, em relação às funções de transferência G1(s) e G2(s), tem-se o seguinte:
C4H6O3 + H2 O → 2 CH3COOH
A reação deverá produzir 20 kg/h de ácido acético, a constante de velocidade é aproximadamente 0,05 min-1 , a concentração inicial de anidrido acético é de 100 g/L, e a conversão, de 80%.
O volume aproximado, em litros, desse reator é
Dados Massa Molar do Ácido Acético (CH3COOH) = 60 g/mol Massa Molar do Anidrido Acético (C4H6O3 ) = 102 g/mol
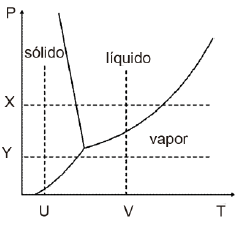
Nesse contexto, em referência ao diagrama, a passagem de