Questões de Vestibular de Química - Equilíbrio Químico
Foram encontradas 630 questões
NaOH 5,6 mol.L-1 e ao qual foi adicionado 150 mL de uma solução de HCl 2,0 mol.L-1 . A solução resultante dessa mistura deverá apresentar um pH:
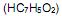 com o hidróxido de sódio. Se em uma solução aquosa 0,072 mol/L de ácido benzóico, no equilíbrio apresenta uma concentração de íons hidrônio
com o hidróxido de sódio. Se em uma solução aquosa 0,072 mol/L de ácido benzóico, no equilíbrio apresenta uma concentração de íons hidrônio 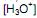 de 2,1 x 10-3 mol/L, qual é o valor de
de 2,1 x 10-3 mol/L, qual é o valor de 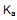 (constante de ionização ácida) deste ácido?
(constante de ionização ácida) deste ácido?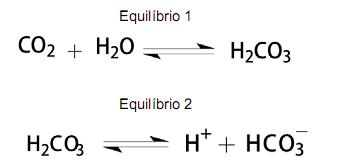
Sobre o sangue e o seu sistema tamponado, é CORRETO afirmar:
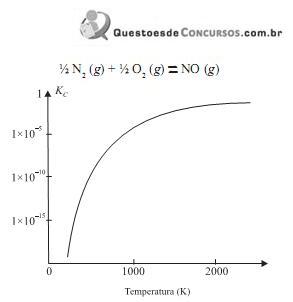
Considere as seguintes afirmações:
I. Um catalisador adequado deslocará o equilíbrio da reação no sentido da conversão do NO em
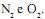
II. O aumento da pressão favorece a formação do NO.
III. A 2400 K há maior quantidade de NO do que a 1200 K. IV. A reação de formação do NO é endotérmica.
São corretas as afirmações contidas somente em
Sabe-se que, no equilíbrio, a velocidade de formação dos produtos, V, e a velocidade inversa, de formação dos reagentes, V’ , são iguais:

Foram realizados dois experimentos envolvendo essa reação, com apenas uma diferença: um, na presença de catalisador; o outro, na ausência deste.
Comparando-se esses dois experimentos, é CORRETO afirmar que, na reação catalisada, aumenta
PbS (s) ⇄ Pb2- (aq) + S2- (aq) S2- (aq) + 2 H- (aq)⇄ H2S (aq)
Neste gráfico, estão representadas as concentrações de Pb 2+ e S 2– , originadas exclusivamente do PbS, em função do pH da água:
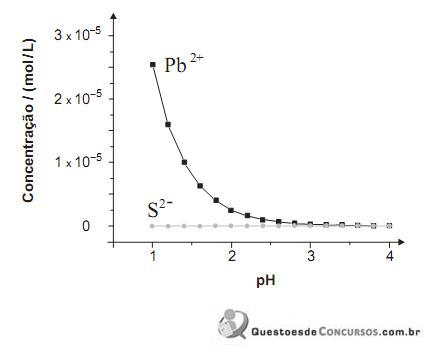
Considere que a incidência de chuva ácida sobre o mesmo lago altera a concentração das espécies envolvidas nos dois equilíbrios.
Com base nessas informações, é CORRETO afirmar que, na situação descrita,
Nos três casos, ocorreu reação química e observou-se a formação de bolhas.
Ao final das reações, as três soluções tornaram-se cor-de-rosa.
O tempo necessário para que cada uma dessas reações se complete está registrado neste quadro:
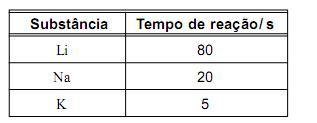
Considerando-se essas informações, é INCORRETO afirmar que
Nestas fguras, estão representados, esquematicamente, os materiais então utilizados por eles:
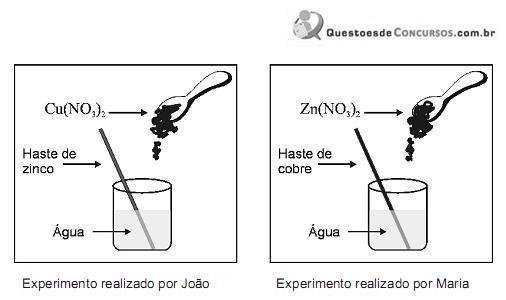
Para facilitar a dissolução de nitrato de cobre em água, João usou uma haste de zinco. No fnal do experimento, a haste estava corroída e formou-se uma solução incolor e um sólido, que, após algum tempo, se depositou no fundo do recipiente.
Maria, por sua vez, utilizou uma haste de cobre para dissolver nitrato de zinco em água. No fnal do experimento, ela obteve uma solução incolor e a haste manteve- se intacta.
Sabe-se que as soluções aquosas de nitrato de cobre (II),
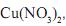 são azuis e que as de nitrato de zinco (II),
são azuis e que as de nitrato de zinco (II), 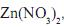 são incolores.
são incolores. Considerando-se os dois experimentos descritos, é CORRETO afrmar que

A diminuição da concentração de oxigênio nas redondezas da célula:

Nesse caso, a substância responsável por essa mudança de coloração é o cloreto de cobalto,
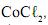 que, de acordo com a situação, apresenta duas cores distintas — azul ou rosa —, como representado nesta equação:
que, de acordo com a situação, apresenta duas cores distintas — azul ou rosa —, como representado nesta equação: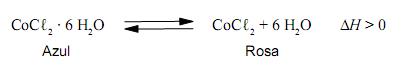
Considerando-se essas informações, é CORREtO afrmar que as duas condições que favorecem a ocorrência, no “galinho do tempo”, da cor azul são
Analise estas três afrmativas concernentes a esse sistema:
I. O sistema é ácido.
II. O pH do sistema é maior que 7.
III. No sistema, a concentração dos íons H+ é maior que a dos OH– .
A partir dessa análise, é CORREtO afrmar que
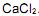 Esses dois métodos fornecem valores diferentes de pH, nos quais o pH em água é maior em relação ao pH em
Esses dois métodos fornecem valores diferentes de pH, nos quais o pH em água é maior em relação ao pH em 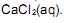 Esse fato ocorre porque
Esse fato ocorre porque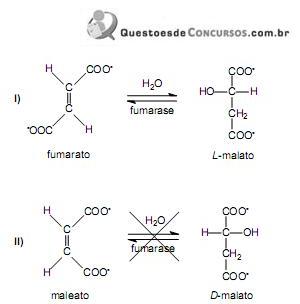
A reação representada em II não ocorre porque
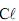 (aq), adicionou-se água pura, em quantidade sufciente para se obterem 100,0 mL de solução diluída.
(aq), adicionou-se água pura, em quantidade sufciente para se obterem 100,0 mL de solução diluída.Considerando-se essas informações, é CORRETO afrmar que o pH da solução resultante é
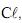 observou-se, durante a dissolução, um resfriamento do sistema
observou-se, durante a dissolução, um resfriamento do sistemaConsiderando-se a situação descrita e outros conhecimentos sobre o assunto, é CORRETO afrmar que


