Questões de Vestibular
Sobre equilíbrio químico em química
Foram encontradas 630 questões
Frasco 1: 100 mL de H2O( L )
Frasco 2: 100 mL de solução aquosa de ácido acético de concentração 0,5 mol/L
Frasco 3: 100 mL de solução aquosa de KOH de concentração 1,0 mol/L
Frasco 4: 100 mL de solução aquosa de
 de concentração 1,2 mol/L
de concentração 1,2 mol/L
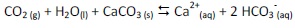
De acordo com essa equação química, dadas as afirmativas seguintes,
I. A reação química é reversível.
II. As espécies químicas presentes no lado dos produtos são chamadas de íons.
III. A equação química não está corretamente balanceada.
IV. A reação química para estar em equilíbrio, a velocidade da reação direta tem que ser igual à velocidade da reação inversa.
verifica-se que estão corretas
Contribuem, para a transformação do Fe (III) em Fe (II), substâncias redutoras presentes no suco gástrico. Por sua vez, outras substâncias podem facilitar ou dificultar a biodisponibilidade do Fe ( II) para sua absorção pelo organismo. Em presença da vitamina C, o Fe (II) forma complexos solúveis, enquanto que, com o oxalato, forma um composto cujo valor de Kps é muito baixo.
Algumas pessoas recomendam consumir espinafre por conter alto teor de Fe (I I), mas que também contém elevada quantidade de oxalato. Também aconselham que a feijoada, rica em Fe (II), seja consumida juntamente com suco de laranja, rico em vitamina C. Em relação às recomendações para se consumir espinafre com o suco de laranja, nessas condições, é correto afirmar:
definem-se valores aceitos, como os apresentados no quadro abaixo.

Em um laboratório de análise de águas, obtém-se os seguintes valores de [H3O+ ] para quatro amostras de águas, identificadas como IAD, IIAD, IIIAD e IVAD.
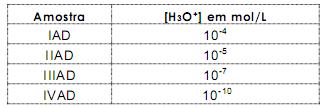
Em relação à qualidade da água, a amostra adequada para consumo humano é a
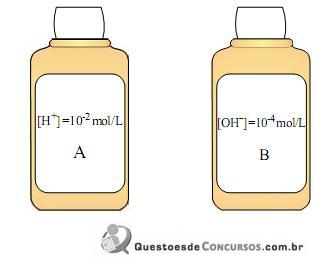
A razão entre os valores de pH da solução B e da solução A, a 25 °C, é
O fenômeno referido é motivado
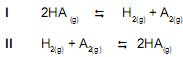
O valor da constante de equilíbrio (KI ) para a reação (I) é 4,17 x 10-34 a 25o C. Assim sendo, pode-se afirmar que o valor da constante de equilíbrio (KII ) para a reação (II) na mesma temperatura será
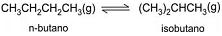
é atingido após certo tempo, sendo a constante de equilíbrio igual a 2,5. Nesse processo, partindo exclusivamente de 70,0 g de n-butano, ao se atingir a situação de equilíbrio, x gramas de n-butano terão sido convertidos em isobutano. O valor de x é
Analise as proposições a seguir:
I. Um dos componentes mais importantes do xampu são os surfactantes, substâncias responsáveis pela eliminação da oleosidade, atuando pela interação entre a gordura, o xampu e a água mediante ligações intermoleculares.
II. Para garantir o pH do xampu por volta de 6, valor próximo ao pH do cabelo, o ácido cítrico pode ser utilizado, o que indica que nestes produtos a concentração hidrogeniônica é da ordem de 1,0 x 10-6 mol/L.
III. Os xampus destinados ao uso infantil contêm surfactantes-anfotéricos (estrutura a seguir), que em meio ácido captura o íon H+ , e em solução básica liberam um dos hidrogênios ligados ao nitrogênio, o que os tornam menos irritantes aos olhos.
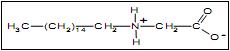
IV. Ao utilizarmos um xampu formado por surfactante aniônico, e não enxaguarmos adequadamente para remover todo o produto usado na lavagem, parte desse ficará aderida aos cabelos e o atribuirão cargas negativas que causam repulsão entre eles, sendo indicado para diminuir essa repulsão, o uso de condicionadores por apresentarem na sua composição substâncias com cargas positivas.
É CORRETO o que se afirma em:
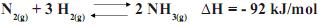
Sobre o equilíbrio do processo acima, é CORRETO afrmar que

Sabendo-se, então, que o coeficiente de solubilidade do K2Cr2O7 é de 12,0 gramas em 100 mL de água à T=200 C, que tipo de sistema será formado quando forem adicionadas 120 gramas de K2Cr2O7 em 600 mL de água à T=200 C?

Considerando-se, por exemplo, que um solo ideal para a cultura da soja necessite de um pH= 5,0, este solo possuirá uma concentração de íons Hidrogênio (H+ ) e pOH, respectivamente iguais a:
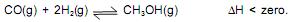
A produção industrial de metanol envolve a reação do monóxido de carbono com o hidrogênio, em determinadas condições, de acordo com o sistema em equilíbrio representado pela equação química.
Considerando-se essas informações e a equação química que representa o sistema em equilíbrio, é correto afirmar:

Os indicadores ácido-base são substâncias químicas que, em solução aquosa, têm a propriedade de mudar de cor, na presença de íons H+ (aq) ou íon OH- (aq) e identificar se uma solução aquosa é ácida ou básica, a exemplo de fenolftaleína e de tornassol, representados na tabela.
Considerando-se as informações do texto e os dados da tabela, é correto afirmar:

