Questões de Vestibular
Sobre grandezas: massa, volume, mol, massa molar, constante de avogadro e estequiometria. em química
Foram encontradas 623 questões
Uma amostra de 4,99 g desse sal hidratado foi aquecida até que toda a água nela contida evaporou, obtendo-se uma massa de 3,19 g de sulfato de cobre II. O número de mols de água por mol de sulfato de cobre II na composição do sal hidratado equivale a:
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO QUÍMICO NÚMERO ATÔMICO MASSA ATÔMICA
H 1 1,0
He 2 4,0
Li 3 6,9
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Ne 10 20,2
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Ca 20 40,0
Mn 25 55,0
Co 27 58,9
Zn 30 65,4
Ge 32 72,6
As 33 75,0
Nb 41 93,0
Pb 82 208,0
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO QUÍMICO NÚMERO ATÔMICO MASSA ATÔMICA
H 1 1,0
He 2 4,0
Li 3 6,9
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Ne 10 20,2
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Ca 20 40,0
Mn 25 55,0
Co 27 58,9
Zn 30 65,4
Ge 32 72,6
As 33 75,0
Nb 41 93,0
Pb 82 208,0
As2S3 +HNO3 + H2O → H3AsO4 + H2SO4 +NO,
marque a única afirmação verdadeira.
N2 + 3H2 → 2NH3
Substâncias nitrogênio hidrogênio amônia
1º experimento 14 g 3 g 17 g 2º experimento 70 g X Y
Os valores das massas, em gramas, que correspondem a X e Y no quadro apresentado, são, respectivamente,
Considerando a massa molar do mercúrio 201 g/mol e a constante de Avogadro 6,0 × 1023/mol, a quantidade de átomos de mercúrio por grama de fio de cabelo tolerada pela OMS é de, aproximadamente:
KO2(s) + CO2(g) → K2CO3(s) + O2(g)
Ajustando-se à equação química, é correto afirmar que a quantidade de gás oxigênio produzido quando se usa 852g de superóxido de potássio é
NaCl(aq) + NH3(g) + CO2(g) + H2O(l) -> NaHCO3(s) + NH4Cl(aq) e 2 NaHCO3(s) -> Na2CO3(s) + CO2(g) + H2O(l)
Sendo assim, é correto dizer que a massa de carbonato de sódio produzida a partir de 23,4 g de cloreto de sódio é
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO QUÍMICO NÚMERO ATÔMICO MASSA ATÔMICA
H 1 1,0
He 2 4,0
Li 3 6,9
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Ne 10 20,2
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Ca 20 40,0
Mn 25 55,0
Co 27 58,9
Zn 30 65,4
Ge 32 72,6
As 33 75,0
Nb 41 93,0
Pb 82 208,0
É dada a equação não balanceada: ZnS(s) + O2(g) → ZnO(s) + SO2(g) e conhecem-se os valores do calor de combustão do zinco = -108,85 kcal/mol, e dos calores de formação do ZnS = - 44,04 kcal/mol, e do SO2 = - 71,00 kcal/mol. Com essas informações, pode-se afirmar corretamente que o calor de formação do óxido de zinco será, em kcal/mol, aproximadamente
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO QUÍMICO NÚMERO ATÔMICO MASSA ATÔMICA
H 1 1,0
He 2 4,0
Li 3 6,9
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Ne 10 20,2
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Ca 20 40,0
Mn 25 55,0
Co 27 58,9
Zn 30 65,4
Ge 32 72,6
As 33 75,0
Nb 41 93,0
Pb 82 208,0
Com relação aos dados dessa solução, assinale a afirmação correta.
TiCl4(s) + Mg(s) → Ti(s) + MgCl2(s).
O número aproximado de átomos de magnésio consumidos quando 63,3 g de tetracloreto de titânio reagem totalmente é
DADOS QUE PODEM SER USADOS NESTA PROVA:

ELEMENTO NÚMERO MASSA
QUÍMICO ATÔMICO ATÔMICA
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Cr 24 52,0
Cu 29 63,5
As 33 75,0
Br 35 80,0
Ag 47 108,0
Sn 50 119,0
Ir 77 192,0
Au 79 197,0
Hg 80 200,0
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO NÚMERO MASSA ATÔMICA
QUÍMICO ATÔMICO
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
S 16 32,0
Cl 17 35,5
Ca 20 40,0
Fe 26 56,0
Cu 29 63,5
Zn 30 65,4
Ag 47 108,0
Sn 50 119,0
Xe 54 131,0
W 74 184,0
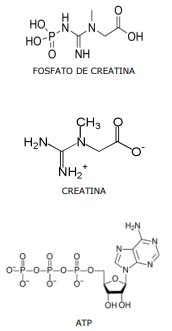 Sobre essas três substâncias, assinale a opção
correta.
Sobre essas três substâncias, assinale a opção
correta.C7H16(V) + O2(g) → CO2(g) + H2O(v).
Faça o ajustamento dessa equação química e determine a quantidade de gás carbônico formado, em kg, para a queima de 100 kg de heptano.
Esse sistema flutua na água porque
4 KO2 (s) + 2 CO2 (g) → 2 K2 CO3 (s) + 3 O2 (g)
Em um processo a 27 ºC e 1 atm, são produzidos 1476 L de oxigênio. A quantidade de peróxido de potássio, em kg, mínima para esse processo é aproximadamente
Adote: R = 0,082 atm. L. mol–1 .K–1
