Questões de Vestibular
Sobre grandezas: massa, volume, mol, massa molar, constante de avogadro e estequiometria. em química
Foram encontradas 614 questões
I. C(graf) + O2(g) → CO2(g) ΔH°= – 394 kJ/mol
II. H2(g) + 1/2 O2(g) → H2O(ℓ) ΔH° = – 242 kJ/mol
III. C(graf) + 2 H2(g) → CH4(g) ΔH° = – 74 kJ/mol
IV. 2 C(graf) + 3 H2(g) + 1/2 O2(g) → C2H5OH(ℓ) ΔH° = – 278 kJ/mol
É correto afirmar que
A adição de sulfato de alumínio é o primeiro passo desse processo e pode ser representado pela equação química NÃO BALANCEADA abaixo.
Aℓ2(SO4)3 + H2O
 Aℓ(OH)3 + H2SO4
Aℓ(OH)3 + H2SO4
Assim, de acordo com a equação dada, de adição de sulfato de alumínio, é correto afirmar que
Dado: massa molar em (g/mol) H = 1, O = 16, Aℓ = 27 e S = 32.
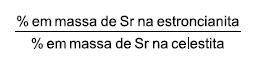
O valor desse quociente é, aproximadamente,

Considere um reservatório hipotético com água de densidade 1 g/mL e volume igual ao do “volume morto” do Sistema Cantareira. Se a água desse reservatório encontra-se contaminada com 20 ppm de chumbo, a massa total deste metal na água do reservatório hipotético é
Questão

3NaHCO3(aq) + H3C6H5O7(aq) → 3CO2(g) + 3H2O(l) + Na3C6H5O7(aq)
Considerando-se essa informação associada aos conhecimentos sobre estequiometria e propriedades das substâncias químicas envolvidas na reação, é correto afirmar:
Considerando que um termômetro possua cerca de 4,0 g de mercúrio, qual o número de átomos presentes no instrumento?
Dados: Massa atômica do Hg = 200 g.mol-1 ; número de Avogadro = 6,0 x 1023
A Aspirina, o medicamento mais conhecido e consumido no mundo, completou cem anos em 1999. Além de atuar como analgésico, é anti-inflamatório, antipirético e antiplaquetário. Seu princípio ativo é o ácido acetilsalicílico, C9H8O4 sintetizado pela reação do ácido salicílico, C7H6O3, com anidrido acético, C4H6O3 como mostrado pela equação química:
C7H6O3(s) + C4H6O3(l) → C9H8O4(s) + C2H4O2(l)
Calcule a massa de anidrido acético necessária para consumir completamente 2,00 . 102 g ácido salicílico.
Dados: Massas molares em g . mol−1 : H = 1; C = 12; O = 16.
Pequenas quantidades de óxido nítrico (NO) ocorrem naturalmente em nossos corpos, nos quais age como um neurotransmissor, ajuda a dilatar os vasos sanguíneos e participa em outras mudanças psicológicas. Considere a reação de obtenção do óxido nítrico a partir de amônia e oxigênio, como mostra a equação química não-balanceada:
x NH3(g) + y O2(g) → z NO(g) + w H2O(g)
Após balancear a referida equação com os menores
números inteiros possíveis, a soma dos coeficientes
estequiométricos é:
NaHCO3(s) → NaOH(s) + CO2(g)
Qual o volume em litros de gás carbônico produzido a uma temperatura de 27 °C e uma pressão de 1 atm pela decomposição de 4,2 g de bicarbonato de sódio (massa molar 84,00 g mol–1)?
C6H12O6(s) → 2 C2H5OH(l) + 2 CO2(g) ∆H°= −74,0 kJ.mol−1
Calcule a quantidade de glicose, em gramas, a ser fermentada para produzir 300 kJ de calor.
Dados: Massas molares em g.mol−1: H = 1; C = 12; O = 16.
Ca3(PO4)2(s) + 3 H2SO4(aq) → 3 CaSO4(s) + 2 H3PO4(aq)
A mistura resultante de CaSO4 e H3PO4 é seca, pulverizada e espalhada pelos campos para plantações, onde o fosfato é dissolvido pelas águas das chuvas. Calcule a quantidade de ácido fosfórico produzida a partir de 1,00 kg de ácido sulfúrico.
Dados: Massas molares em g . mol−1: H = 1; O = 16; P = 31; S = 32.
Dado: massa molecular do metano = 16 g.mol-1.
w Ca3(PO4)2(aq) + x H2SO4(aq) → y H3PO4(aq) + z Ca(SO4)(aq)
Se utilizarmos 50 g de Ca3(PO4)2 e ácido sulfúrico em excesso, quantos gramas de ácido fosfórico podem ser obtidos através dessa reação?
Dados: massas moleculares em g.mol-1 : Ca3(PO4)2 = 310; H3PO4 = 98.
O gás butano (C4 H10) é um combustível não renovável derivado do petróleo, cuja combustão incompleta ocorre quando a quantidade de oxigênio é insuficiente para que ocorra a combustão completa.
Considere a equação da reação de combustão incompleta do gás butano:
2C4 H10 (g) + 9O2 (g) 8CO (g) + 10H2 O (g)
A massa do gás monóxido de carbono (massa molar = 28 g/mol) formada quando 522 kg de gás butano (massa molar = 58 g/mol) sofrem combustão incompleta, numa reação com rendimento total, é de


Após o problema da bateria ter sido resolvido, eles continuaram a viagem. Percorridos alguns quilômetros Carlos precisou frear bruscamente o veículo, devido a um acidente ocorrido na rodovia. Passado o susto, Eduardo pergunta com ironia:
- Seu carro tem airbag?
- É obvio que não, responde Carlos.
- Você saberia me dizer como funciona um airbag?
- Não tenho ideia. O que você acha de consultarmos aquele livro de Química?
- Legal!
Então, Eduardo estica a mão e pega, no banco de trás, um livro no qual se lê:
O airbag é formado por um dispositivo que contém a mistura química de NaN3 (azida de sódio), KNO3 e SiO2 que é responsável pela liberação do gás. Esse dispositivo está acoplado a um balão que fica no painel do automóvel e quando ocorre uma colisão (ou desaceleração), os sensores localizados no para-choque do automóvel transmitem um impulso elétrico (faísca) que causa a detonação da reação. Em aproximadamente 25 milésimos de segundo, o airbag está completamente inflado.
Veja as equações do processo:
I - 2 NaN3 → 2 Na + 3N2
II - 10 Na + 2 KNO3 → K2O + 5 Na2O + N2
III - K2O + Na2O + SiO2 → silicato alcalino
Dado: um airbag contém aproximadamente 130 g de azida.
Disponível em: <http://www.brasilescola.com/quimica/air-bag-reacao-decomposicao.htm> (adaptado) Acesso em: 12 set. 2011.
Assinale a proposição CORRETA.
Considerando apenas a equação I, a massa de azida necessária para a formação de 67,2 L
de N2 nas CNTP seria 130 g.