Questões de Vestibular
Sobre soluções e substâncias inorgânicas em química
Foram encontradas 980 questões
BICARBONATO DE SÓDIO
O bicarbonato de sódio é uma substância extremamente barata e fácil de encontrar e contém propriedades fabulosas que nos permitem utilizá-lo de inúmeras formas em nosso dia a dia. Atua como um antifúngico e neutralizador de acidez. Quando o bicarbonato de sódio é consumido, alcaliniza o corpo pelo aumento de pH, permitindo a oxigenação e combatendo o crescimento de fungos e leveduras. Ajuda muito na higiene bucal, reduzindo manchas nos dentes, deixando-os brancos e limpos. Além disso, é um bom remédio para pessoas que sofrem de sensibilidade nas gengivas.
É recomendado fazer uma pasta com bicarbonato e algumas gotas de água e aplicar um pouco na escova de dente. Dependendo da sua sensibilidade, pode-se aplicar também com um algodão. Além disso, pode ser utilizado como antisséptico bucal.
Disponível em:<http://belezaesaude.com/bicarbonato-de-sodio/> .
Acesso em: 28 de julho de 2016.
Qual a equação química que melhor representa a ação dessa substância agindo como antiácido?

A solução de Manitol é indicada para promoção da diurese (produção de urina pelos rins); na prevenção da falência renal aguda (perda repentina da capacidade dos rins em realizar suas funções) durante cirurgias cardiovasculares e/ou após trauma; na redução da pressão intracraniana e no tratamento do edema cerebral; na redução da pressão intraocular elevada quando esta não pode ser reduzida por outros meios; no ataque de glaucoma; na promoção da excreção urinária de substâncias tóxicas; no edema cerebral de origem cardíaca e renal.
Disponível em:<http://www.anvisa.gov.br/datavisa/fila_bula/frmVisualizarBula.asp?pNuTransacao=8323132013&pIdAnexo=1812989>. Acesso em: 27 de julho de 2016.
A análise dos dados apresentados permite inferir que,
na preparação de uma bolsa plástica de 500 mL, será(ão)
necessário(s)

A soldagem é a conexão permanente de peças ou materiais metálicos com a utilização de uma liga metálica, geralmente estanho e chumbo. A soldagem é eficaz para uma variedade ampla de metais, tais como o cobre, o zinco, o latão, a prata e o alumínio. É ideal para vários serviços: conexões de tubulações e de encanamentos, reparos de telhados metálicos, de fiação elétrica residencial, automotiva, aparelhos eletroeletrônicos, etc.
Solda estanho/chumbo: As ligas estanho/chumbo são as mais utilizadas. Nesses casos de solda, o conteúdo da liga é expresso em porcentagem de estanho e chumbo, com o conteúdo de estanho sempre listado primeiro. Por exemplo, solda para uso geral 60/40, tal como a Solda em Fio com Resina (189 MSX 10), tem 60% de estanho e 40% de chumbo.
Disponível em: <http://www.soldabest.com.br/tecnicas_soldagem.htm>. Acesso em: 10 de agosto de 2016.
Relacionado ao assunto relatado no texto, pode-se afirmar
que
A partir dessas considerações, é correto afirmar:
Considerando-se essas informações associadas aos conhecimentos das propriedades coligativas e admitindo-se que a pressão osmótica do sangue é, aproximadamente, 7,8atm, a 37° C, é correto afirmar:
No preparo de certas massas culinárias, como pães, é comum adicionar-se um fermento que, dependendo da receita, pode ser o químico, composto principalmente por hidrogenocarbonato de sódio (NaHCO3), ou o fermento biológico, formado por leveduras. Os fermentos adicionados, sob certas condições, são responsáveis pela produção de dióxido de carbono, o que auxilia a massa a crescer. Para explicar a produção de dióxido de carbono, as seguintes afirmações foram feitas.
I. Tanto o fermento químico quanto o biológico reagem com os carboidratos presentes na massa culinária, sendo o dióxido de carbono um dos produtos dessa reação.
II. O hidrogenocarbonato de sódio, presente no fermento químico, pode se decompor com o aquecimento, ocorrendo a formação de carbonato de sódio (Na2CO3), água e dióxido de carbono.
III. As leveduras, que formam o fermento biológico, metabolizam os carboidratos presentes na massa culinária, produzindo, entre outras substâncias, o dióxido de carbono.
IV. Para que ambos os fermentos produzam dióxido de carbono, é necessário que a massa culinária seja aquecida a temperaturas altas (cerca de 200 °C), alcançadas nos fornos domésticos e industriais.
Dessas afirmações, as que explicam corretamente a produção de dióxido de carbono pela adição de fermento à massa culinária são, apenas,
Em ambientes naturais e na presença de água e gás oxigênio, a pirita, um mineral composto principalmente por dissulfeto de ferro (FeS2), sofre processos de intemperismo, o que envolve transformações químicas que acontecem ao longo do tempo.
Um desses processos pode ser descrito pelas transformações sucessivas, representadas pelas seguintes equações químicas:
2FeS2(s) + 7 O2(g) + 2H2O(ℓ) → 2 Fe2+(aq) + 4SO2-4(aq) + 4H+(aq)
2Fe2+(aq) + ½ O2(g) + 2H+(aq) → 2Fe3+(aq) + H2O(ℓ)
2 Fe3+(aq) + 6 H2O(ℓ) → 2 Fe(OH)3 (s) + 6 H+(aq)
Considerando a equação química que representa a transformação global desse processo, as lacunas da frase “No intemperismo sofrido pela pirita, a razão entre as quantidades de matéria do FeS2 (s) e do O2 (g) é __________, e, durante o processo, o pH do solo __________” podem ser corretamente preenchidas por
C6H12O6 → 2 C2H5 OH + 2 CO2
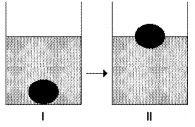
Para determinar a ação destes fungos, muitas pessoas, após prepararem a massa utilizando fermento biológico, separam uma porção dela em forma de “bola” e a mergulham num recipiente com água, aguardando que ela flutue, como pode ser observado, respectivamente, em I e II do esquema a seguir:
Já o fermento químico, é formado basicamente por bicarbonato de sódio, que se decompõe termicamente de acordo com a seguinte equação:
NaHCO3 → Na2 CO3 + H2 O + CO2
Com relação à utilização dos dois tipos de fermentos, é incorreto afirmar que:
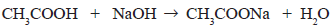
- até 200 mg/dL, DESEJÁVEL; - de 201 a 239 mg/dL, ACEITÁVEL; - a partir de 240 mg/dL, AUMENTADO.
Na análise laboratorial de uma amostra de sangue, foi determinado 2,1 g L-1 de colesterol, cuja fórmula molecular é C27H46O. Quantos mols de colesterol estão presentes aproximadamente e como está o nível de colesterol nessa amostra em relação aos valores tabelados acima?
100g de uva passa são processados adequadamente até se obterem 280ml de solução que contêm 0,975mg de um sal de potássio, K2A, 100% dissociado. A molaridade dos íons potássio, em mols por litro, é: Dado: massa molar K2A = 174g/mol
H3C-NH2 + H3CCOOH
 H3C-N+H3 + H3CCOO- base ácido ácido base
H3C-N+H3 + H3CCOO- base ácido ácido baseDe acordo com essas informações, assinale a alternativa que possui, respectivamente, um ácido e uma base de Brönsted-Lowry.
Na tabela abaixo, segue a relação de algumas dessas substâncias.
Produtos comercializados Substâncias inorgânicas
Água sanitária Hipoclorito de sódio
Desentupidores de pia Hidróxido de sódio
Sal de cozinha Cloreto de sódio
Fermento químico Hidrogenocarbonato de sódio
Creme dental Fluoreto de sódio
Assinale a alternativa na qual encontram-se as fórmulas químicas das substâncias inorgânicas presentes nos produtos comercializados, na ordem que aparecem na tabela, de cima para baixo.
Leia as afirmações abaixo.
I - O amido de milho ou fécula de mandioca são exemplos de substâncias orgânicas.
II - O ácido fumárico, o bicarbonato de sódio e o carbonato de cálcio são exemplos de substâncias inorgânicas.
III - O bicarbonato de sódio e o carbonato de cálcio são exemplos de sais.
IV- O ácido fumárico tem este nome porque ele esta presente na fumaça.
Assinale a alternativa correta