Questões de Vestibular
Sobre termoquímica: energia calorífica, calor de reação, entalpia, equações e lei de hess. em química
Foram encontradas 350 questões
Pode-se concluir corretamente que, na combustão completa de 1 mol desse hidrocarboneto, as quantidades de matéria, e CO2 e de H2O produzidas são, em mol, respectivamente, iguais a
Entre os gráficos 1, 2 e 3, aquele que representa corretamente a reação da fosfina com o oxigênio, descrita no texto, é o
Leia o texto para responder a questão.
De onde vem o cheiro de carro novo?
De acordo com o gerente de uma montadora de veículos, o cheiro é composto por uma combinação de vários tipos de substâncias químicas usadas na fabricação do veículo, incluindo solventes, plásticos, colas, tecidos e borracha. Porém, muitas delas são altamente tóxicas, porque contêm Compostos Orgânicos Voláteis (COVs) em sua composição, como benzeno, tolueno e formol, que podem ser letais dependendo da quantidade. Eles acabam escapando e impregnando o ar, porque não requerem altas temperaturas para evaporarem.
<http://tinyurl.com/y8ucob6c> Acesso em: 13.11.2017. Adaptado.
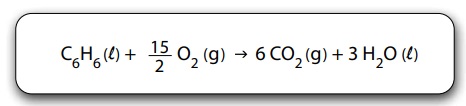
A entalpia de combustão do benzeno pode ser determinada conhecendo-se os valores das entalpias de formação do gás carbônico, assim como da água e do benzeno líquidos.
A tabela apresenta os valores de entalpia de formação de algumas substâncias nas condições padrão.
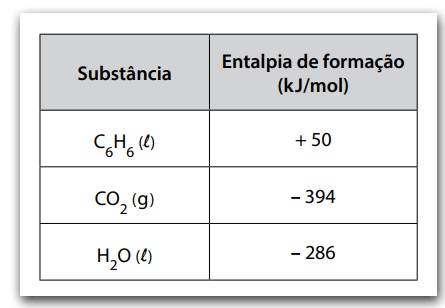
A entalpia de combustão completa do benzeno, em kJ/mol, é
A hipoglicemia é caracterizada por uma concentração de glicose abaixo de 0,70 g L−1 no sangue. O quadro de hipoglicemia em situações extremas pode levar a crises convulsivas, perda de consciência e morte do indivíduo, se não for revertido a tempo. Entretanto, na maioria das vezes, o indivíduo, percebendo os sinais de hipoglicemia, consegue reverter este déficit, consumindo de 15 a 20 gramas de carboidratos, preferencialmente simples, como a glicose.
A metabolização da glicose, C6H12O6, durante a respiração, pode ser representada pela equação química de combustão:
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l)
No quadro a seguir, são informadas reações químicas e seus respectivos calores de formação a 25 °C e 1 atm:

Sabendo que a Massa Molar (MM) da glicose é igual a 180,0 g mol−1, determine a quantidade aproximada de energia
liberada em kJ mol−1 no estado padrão, ΔHr°, na combustão da glicose, consumida em 350 mL de refrigerante
do tipo Cola, o qual possui, em sua composição, 35 g de glicose.
De acordo com a Lei de Hess, a variação de entalpia de uma reação depende apenas dos estados inicial e final.
Considere as afirmações abaixo, sobre a Lei de Hess.
I - A reação reversa de uma reação endotérmica é sempre exotérmica.
II - A reação de combustão de um açúcar produzindo CO2 e água terá a mesma variação de entalpia, caso ocorra em um calorímetro ou no organismo humano.
III- Um catalisador adequado propicia um caminho com menor diferença de entalpia entre reagente e produtos.
Quais estão corretas?
A nitroglicerina - C3H5(NO3)3 – é um nitrato de alquila, descoberta em 1847 por Ascanio Sobrero (químico italiano, 1812-1888), que a obteve misturando glicerina, ácido nítrico e ácido sulfúrico. No estado puro e à temperatura ambiente, a nitroglicerina é um líquido muito explosivo e perigoso. Em 1867, Alfred Nobel (químico sueco, 1833-1896) realizou testes no sentido de melhorar a manipulação da nitroglicerina, misturando-a com materiais inertes, como sílica, pós cerâmicos, argila, gesso, carvão e terras diatomáceas. Esses materiais, agora moldáveis, viriam a se tornar um explosivo muito importante, conhecido como dinamite.
A equação abaixo (não balanceada) representa a reação de decomposição da nitroglicerina:
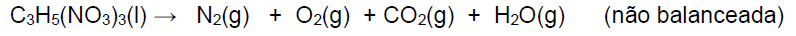
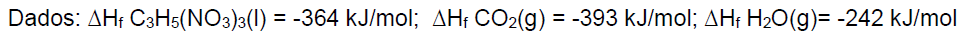
De posse das informações, assinale a alternativa que representa a variação de entalpia da
reação acima, em kJ por mol de nitroglicerina.
A lactose é hidrolisada no leite “sem lactose”, formando dois carboidratos, conforme a equação química:
lactose + água → glicose + galactose
Se apenas os carboidratos forem considerados, o valor calórico de 1 litro tanto do leite integral quanto do leite “sem lactose” é igual a −90 kcal, que corresponde à entalpia-padrão de combustão de 1 mol de lactose.
Assumindo que as entalpias-padrão de combustão da glicose e da galactose são iguais, a entalpia de combustão da glicose, em kcal/mol, é igual a:
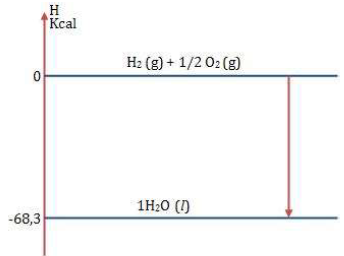
Disponível em: <https://www.colegioweb.com.br/wp-content/uploads/21337.jpg.> Acesso em 30/03/2018.
O esquema ilustra o aspecto energético da reação de formação de água líquida a partir dos gases hidrogênio e oxigênio. Essa reação é uma
C6H12O6
 2 C2H5OH + 2 CO2
2 C2H5OH + 2 CO2 Sendo os calores de formação da glicose, do gás carbônico e do álcool, respectivamente, –302, –94 e –66 kcal/mol, pode-se afirmar que a fermentação ocorre com:
Considere a equação química (não balanceada) para a combustão do etanol:
C2H6O(l) + O2(g) ➜ CO2(g) + H2O(l)
Dados: Entalpia de formação de C2H6O(l) = – 66 kcal/mol
Entalpia de formação de CO2(g) = – 94 kcal/mol
Entalpia de formação de H2O(l) = – 68 kcal/mol
A entalpia de combustão em kcal/mol será:
Leia o texto e analise a tabela sobre entalpias de ligação para responder à questão.
O lixo urbano pode ser usado para a produção de uma importante fonte de energia, o metano. Essa substância é produzida na decomposição anaeróbica da matéria orgânica, podendo ser usada como combustível em veículos e na indústria.
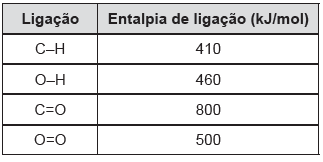
Considerando os valores aproximados das entalpias
de ligação apresentados na tabela, em relação ao
metano é possível afirmar que
A produção de muitos dos alimentos e bebidas mais apreciados envolve processos fermentativos. A produção do vinho e da cerveja, realizada com auxílio do Saccharomyces cerevisiae, é um exemplo. Esse micro-organismo é capaz de alimentar-se de açúcares simples, como a glicose, produzindo etanol e dióxido de carbono, como mostra a equação química não balanceada a seguir.
C6 H12O6 → CH3 CH2 OH + CO2
Sobre esse assunto, é correto afirmar que
O benzeno reage completamente com oxigênio, conforme indicado na equação:
2 C6 H6 (l) + 15 O2 (g) → 12 CO2 (g) + 6 H2O (g); ∆H° = -6.600 kJ
Um volume, em mL, de benzeno foi reagido em excesso de oxigênio produzindo -132 kJ de energia. Se a densidade do benzeno é 0,88 g mL-1 , o volume do hidrocarboneto mais próximo daquele que reagiu foi
Dado
M (C6
H6
) = 78,0 g mol-1
I - A vaporização do etanol é um processo exotérmico.
II - Os produtos de uma reação de combustão têm entalpia inferior aos reagentes.
III- A reação química da cal viva (óxido de cálcio) com a água é um processo em que ocorre absorção de calor.
Quais estão corretas?
LIMA, M. E. C. C.; DAVID, M. A.; MAGALHÃES, W. F de. Ensinar Ciências por investigação: um desafio para os formadores. Química Nova na Escola, n. 29, ago. 2009. p. 25. Adaptado.
De acordo com o texto, marque a alternativa que apresenta uma informação INCORRETA sobre o que ocorre na bolsa térmica.
No gráfico a seguir, é apresentada a variação da energia durante uma reação química hipotética.
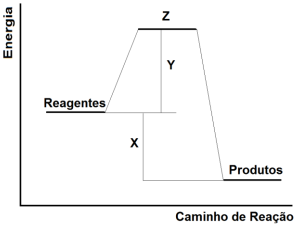
Com base no gráfico, pode-se correlacionar X, Y e Z, respectivamente, como
CaO(s) + H2O(l) → Ca(OH)2 + 63,7 kJ
afirma-se que temos uma reação
CaCO3(s)
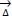 CaO(s) + CO2(g)
CaO(s) + CO2(g)
Que volume de CO2 será obtido, considerando o rendimento reacional de 80%?
