Questões de Concurso
Sobre cinética química em química
Foram encontradas 829 questões
O etilenoglicol (C2H6O2) é um álcool muito utilizado como anticongelante automotivo. Adicionado à água, ele atrai fortemente suas moléculas. Isso acontece porque o etilenoglicol é capaz de fazer pontes de hidrogênio com a água, o que resulta em um abaixamento da temperatura de congelamento. Pode-se dizer que a interação dos dois dificulta a "organização" para a formação de um sólido, que resulta em um ponto de congelamento menor que o das duas substâncias separadas. Diante do que foi exposto, qual o ponto de congelamento de uma solução que contém 250g de etilenoglicol e 1350g de água. Dados: (Kc água = 1,86ºC Kg/mol; Metilenoglicol = 62,1g/mol).
Pressão de vapor é a pressão exercida por um vapor quando este está em equilíbrio termodinâmico com o líquido que lhe deu origem. A pressão de vapor de uma mistura é diferente da pressão de vapor do solvente puro. No caso de uma solução líquida com um soluto não-volátil, a pressão de vapor é sempre menor que a do solvente. Supondo que uma solução contém 20g de um soluto orgânico não volátil em 250g de álcool etílico tem uma pressão de vapor de 316,0 torr, a 25ºC. Se a pressão de vapor do álcool etílico puro é de 368,3 torr, nesta temperatura, qual será o número de mols do soluto? (Dados: Málcool etílico = 46,07g/mol)
A oxigenoterapia consiste no tratamento da hipóxia que é diminuição das taxas de oxigênio no sangue arterial ou nos tecidos. Esse tratamento consiste na inalação de oxigênio, a uma pressão maior que a do ar ambiente, o que facilita a troca gasosa e reduz o trabalho da respiração. (II Consenso Brasileiro de Ventilação Mecânica. J Pneumol 2000;26 (Suppl 2): S1-2.)
O gás oxigênio usado nesse tratamento pode ser comercializado em cilindros a elevada pressão. Supondo que o cilindro contém 200 cm3 de gás oxigênio (O2), submetido à temperatura constante de 150°C e pressão total de 1,0 atm. Assumindo que o O2 se comporta como gás ideal, assinale a opção CORRETA que apresenta os respectivos valores numéricos do número de moléculas e da massa específi ca, em kg m-3, desse gás quando exposto às condições de pressão e temperatura apresentadas. : (Dados: R=0,082 dm3 atm mol-1 K-1 Número de Avogadro 6,02x1023)
Os agentes sulfitantes são classif cados como aditivos alimentares e atuam na inibição da deterioração provocada por bactérias, fungos e leveduras em alimentos ácidos, e na inibição de reações de escurecimento enzimático e não enzimático, durante processamento e estocagem. No entanto, apesar da eficácia dos sulfitos na indústria alimentícia, inúmeros efeitos adversos à saúde humana têm sido relacionados à sua ingestão, principalmente, anafilaxia, urticária, angioedema, hipotensão, náusea, irritação gástrica local, diarréia e crise asmática em indivíduos asmáticos sensíveis a sulfitos. Na União Europeia, os sulf tos são considerados, a partir de 2005, como alergênicos, devendo obedecer ao limite máximo de 10mg/L. Uma vez ultrapassado este valor, é obrigatória a menção no rótulo. (http://www.sciencedirect.com/science/ article/pii/S0956566310003106.Adaptado)
Supondo que a produção anual de suco industrializado na União Europeia é de 450 milhões de litro por ano, a quantidade máxima de sulfitos, em quilogramas, que pode ser encontrada no volume considerado de suco industrializado, produzido durante um ano e que respeita o limite máximo de sulfito nessa bebida é:
Ao adicionar 4 mol de cloreto de sódio a uma solução aquosa que contêm 510 g de nitrato de prata. Podemos afirmar que: (Dados: massa molar em g/mol: Ag=108; Na=23; O=16; N=14; Cl=35,5.)
De acordo com o gráfico a seguir, escolha a alternativa CORRETA entre as afirmativas abaixo:
(Fonte: http://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/physprop.htm)
I. A molécula de água (H2O) realiza ligações covalentes entre seus átomos e entre suas moléculas, por isso apresenta o ponto de ebulição mais elevado entre as substâncias mostradas no gráfico.
II. O fluoreto de hidrogênio (HF) apresenta maior ponto de ebulição que o cloreto de hidrogênio (HCl), pois entre suas moléculas são realizadas ligações iônicas (fortes), enquanto que entre as moléculas do HCl são realizadas ligações de pontes de hidrogênio (mais fracas).
III. O gráfico mostra que, conforme aumenta a massa molar das substâncias, aumenta a temperatura de ebulição das mesmas, com exceção às moléculas de H2O em relação a H2S e HF em relação HCl.
IV. Em temperatura ambiente (27 ºC), as substâncias químicas HCl e HBr são líquidas, pois realizam ligações de pontes de hidrogênio e de Van der Waals, respectivamente.
V. O gás metano (CH4) apresenta o menor ponto de ebulição entre todas as substâncias mostradas no gráfico, pois além de realizar ligações de Van der Waals intermoleculares também é a molécula de menor massa molar.
São CORRETAS apenas as afirmativas:
Qual a quantidade de hidróxido de sódio necessária para o preparo de 200 ml de uma solução aquosa na concentração de 40 g/L?
Para o preparo de uma solução de Ácido Clorídrico (HCL) 1+1 (50%) deve-se, em um balão volumétrico de 1L, adicionar aproximadamente 400mL de água destilada e acrescentar, vagarosamente, um volume de ácido concentrado e completar o volume para 1L com água destilada. Para esta solução, qual deve ser o volume de ácido concentrado? Analise as afirmativas seguintes e marque a alternativa CORRETA:
I – O volume do ácido concentrado é de 500mL.
II – O volume do ácido concentrado é de 200mL.
III – O volume do ácido concentrado é de 100mL
IV - O volume do ácido concentrado é de 50mL.
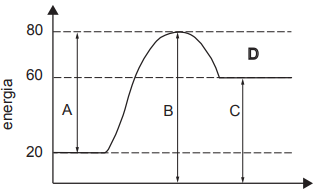
caminho da reação
Em relação a essa reação, é CORRETO afirmar que
( ) Catalizadores são substâncias que, quando participam da reação, são consumidas e podem ser classificados como homogêneos ou heterogêneas. ( ) A ordem de reação é sempre determinada pelos coeficientes estequiométricos da reação. ( ) A velocidade de uma reação de ordem zero é independente da concentração do reagente. ( ) O tempo de meia-vida de uma substância numa reação química é o tempo necessário para que sua concentração se reduza à metade da inicial. ( ) A constante de equilíbrio de uma reação química é adimensional e seu valor numérico depende da temperatura.
Assinale a alternativa que indica a sequência correta, de cima para baixo.
Atenção: Considere as informações abaixo para responder a questão.
A síntese de Haber-Bosch é o método industrial para a produção de amônia utilizada na fabricação de fertilizantes e de muitos outros compostos.
A equação global de reação é dada por:
N2(g) + 3H2(g) ⇋ 2NH3(g) ΔH = −92,22 kcal . mol−1
A tabela abaixo mostra os dados experimentais da reação de síntese da amônia realizada a temperatura e pressão constantes.

A reação de cloro gasoso com uma base forte pode ser descrita pela equação
Cℓ2(g) + 2 NaOH(aq) → NaCℓ(aq) + NaOCℓ(aq) + H2O(ℓ)
Para o posterior preparo de 0,5 litro de solução 0,2 mol.L–1 de hipoclorito de sódio obtido por meio desse processo, a massa de hidróxido de sódio que deve reagir em presença de excesso de cloro gasoso é, no mínimo, igual a
Dados: Massas molares H = 1g.mol–1 ; O = 16g.mol–1 Na = 23g.mol–1
O cloreto de titânio(IV), TiCl4, é um importante produto químico industrial. Esse pode ser usado tanto na obtenção do TiO2 quanto de titânio metálico. O TiCl4 pode ser obtido a partir de um minério contendo titânio (TiO2 impuro), utilizado em excesso, com carbono e gás cloro, conforme a equação química a seguir.
TiO2(s) + 2 Cl2(g) + C(s) → TiCl4(l) + CO2(g)
Considere que a obtenção do TiCl4 seja feita a partir de 852 g de C e 852 g de Cl2.
Dados: Cl2 (71 g mol-1 ); C (12 g mol-1 ) e TiCl4 (190 g mol-1 )
O reagente limitante e a massa em gramas de TiCl4 obtida são, respectivamente:
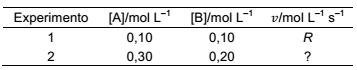
Existem muitos motivos para estudar a velocidade de uma reação, do ponto de vista prático, o conhecimento das velocidades de reações é útil na concepção de medicamentos, no controle da poluição e no processamento de alimentos, bem como nas aplicações de setores produtivos em geral. Então para exemplificar, considere que a velocidade de uma reação entre os compostos A e B segue a lei de velocidade, v = k [A] 2 [B] . Com base nos dados da tabela abaixo, determine a velocidade do Experimento 2 observada a mesma temperatura do Experimento 1.
A palavra cinética, no caso da Química, refere-se à velocidade de uma reação, isto é, à variação da concentração de desaparecimento de um reagente ou de surgimento de um produto com o tempo. Para exemplificar, considere que a 280 °C, o dióxido de nitrogênio se decompõe no óxido nítrico e oxigênio:
2NO2(g) → 2NO(g) + O2(g)
E que em um experimento, a concentração de NO2 diminui de 0,010 mol L–1 a 0,005 mol L–1 no período de 100 s. Qual é a velocidade média de desaparecimento de NO2?
O processo Haber-Bosch é utilizado industrialmente para a produção de amônia. A quantidade de NH3 produzida na reação entre N2 e H2 é influenciada, entre outros fatores, por pressão e temperatura. A produção da amônia pode ser representada pela equação química a seguir:

O gráfico 1 representa a variação de porcentagem de amônia produzida em reações realizadas a diferentes temperaturas, à pressão de 500 atm.
O quadro 1 apresenta quatro diferentes condições de reação testadas, variando-se a temperatura e as quantidades dos gases reagentes. Considere que o gás apresentado no quadro seja o reagente limitante na condição em questão.

Uma certa reação química em fase gasosa é representada pela equação abaixo. Sabe-se que o reagente B e C não influi na velocidade da reação, mas o A quando elevado ao quadrado, altera a velocidade quadruplicada. Deste modo, assinale a alternativa que fornece a equação da velocidade CORRETA.
2A + 2 B → C
NH3 + H2SO4 → (NH4)2SO4
Se a obtenção deste sal for obtida através da lavagem do gás amônia com uma solução de ácido sulfúrico, dado que a concentração de amônia é de 34.000 mg/L, qual seria a concentração de ácido sulfúrico em mol/L necessária para se obter 100% de rendimento? (Dados: massas molares: H= 1,0 g/mol, N= 14 g/mol, O= 16 g/mol, S= 32 g/mol)
A expressão de velocidade para a reação descrita a seguir, é corretamente apresentada na alternativa.
