Questões de Concurso
Sobre propriedades físicas dos compostos orgânicos: polaridade das ligações e moléculas, forças intermoleculares, ponto de fusão e ponto de ebulição, solubilização das substâncias orgânicas. em química
Foram encontradas 219 questões
Texto para a questão.
A exploração, em sala de aula, do tema sabões e detergentes permite diferentes enfoques e técnicas de ensino, que promovem o pensamento crítico dos alunos por se tratar de um tema organizador relacionado a seu cotidiano. Tal proposta valoriza o aluno como indivíduo pensante, promovendo o papel do professor a mediador e orientador do processo educacional. Isso valoriza o papel desempenhado pela escola e contribui com o processo de aprendizagem da química, favorecendo, encorajando e sustentando a autoconstrução e o desenvolvimento do conhecimento por parte dos alunos. Nesse contexto, a equação genérica seguinte descreve o processo de saponificação, em que R corresponde a cadeias iguais ou diferentes, contendo entre 12 e 18 átomos de carbono.

Texto para a questão.
A solubilidade é um dos temas mais relevantes da área da química, tanto por sua importância intrínseca quanto pela variedade de fenômenos e propriedades químicas envolvidas em seu entendimento. O processo de solubilização de uma substância resulta da interação entre a espécie que se deseja solubilizar (soluto) e a substância que a dissolve (solvente) e pode ser definida como a quantidade de soluto que dissolve, em uma determinada quantidade de solvente, em condições de equilíbrio. Solubilidade é, portanto, um termo quantitativo.
C. R. Martins, W. A. Lopes e J. B. Andrade. Solubilidade das
substâncias orgânicas. In: Química Nova, v. 36, n.° 8,
2013, p. 1.248-1.255 (com adaptações).
Texto para a questão.
A solubilidade é um dos temas mais relevantes da área da química, tanto por sua importância intrínseca quanto pela variedade de fenômenos e propriedades químicas envolvidas em seu entendimento. O processo de solubilização de uma substância resulta da interação entre a espécie que se deseja solubilizar (soluto) e a substância que a dissolve (solvente) e pode ser definida como a quantidade de soluto que dissolve, em uma determinada quantidade de solvente, em condições de equilíbrio. Solubilidade é, portanto, um termo quantitativo.
C. R. Martins, W. A. Lopes e J. B. Andrade. Solubilidade das
substâncias orgânicas. In: Química Nova, v. 36, n.° 8,
2013, p. 1.248-1.255 (com adaptações).
As interações intramoleculares e intermoleculares são as responsáveis pelas várias fases (estados) da matéria e pelas propriedades físico-químicas dos materiais, além de necessárias para a determinação de estruturas de moléculas biologicamente importantes. Acerca das ligações químicas nos materiais, julgue o próximo item.
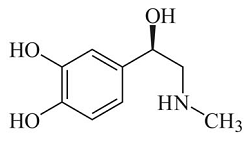
A estrutura química da epinefrina, mostrada a seguir, dispõe de sítios capazes de interagir com seus receptores no organismo, por meio de interações químicas de Van der Waals e de ligação de hidrogênio, além de ligação iônica.
De acordo com a nova definição de mol recomendada pela IUPAC, um mol contém exatamente 6,02214076 × 1023 entidades elementares. Esse número é o valor numérico fixo da constante Avogadro, NA, quando expresso em mol-1 , e é chamado de número de Avogadro. A nova definição enfatiza que a quantidade de substância está relacionada com as entidades de contagem em vez da massa de uma amostra.
Internet:<https://iupac.org>
Com relação a essas informações, julgue o item que se segue.
A substituição de 1, 2 ou 3 átomos de hidrogênio por
átomos de cloro na molécula de metano tornaria polares
todos os compostos formados, contudo, caso os 4 átomos
de hidrogênio na molécula de metano fossem substituídos
por átomos de cloro, a molécula formada seria mantida
apolar, como o próprio metano.
Considerando os dados da tabela precedente, assim como as características e as propriedades das substâncias nela apresentadas, julgue o item a seguir.
A partir de 18 °C, uma mistura de partes iguais em massa
de propanotriol e cicloexano se torna homogênea.
Considerando os dados da tabela precedente, assim como as características e as propriedades das substâncias nela apresentadas, julgue o item a seguir.
Dado que viscosidade é a resistência que um líquido apresenta
para fluir, o propanotriol é mais viscoso que o álcool etílico.
Considerando os dados da tabela precedente, assim como as características e as propriedades das substâncias nela apresentadas, julgue o item a seguir.
As ligações intermoleculares predominantes na sacarose
a 25 °C são as ligações covalentes.
Considerando os dados da tabela precedente, assim como as características e as propriedades das substâncias nela apresentadas, julgue o item a seguir.
Os sólidos moleculares são razoavelmente macios, têm
pontos de fusão baixos a moderados e apresentam baixa
condução térmica.
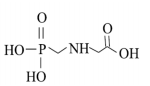
Sobre esse composto, assinale a alternativa correta.
Coluna - 1 (pares de substâncias) (I) Cloreto de sódio e glicose (II) Naftaleno e sacarose (III) Nitrato de sódio e bicarbonato de sódio
Coluna - 2 (testes) (X) pH de suas soluções aquosas (Y) Dissolução em água (Z) Condutividade de suas soluções aquosas
Quais os testes (Coluna - 2) devem ser usados para distinguir os pares de substâncias em I, II e III, (Coluna - 1), respectivamente.
Assinale a alternativa que corresponde à ordem correta de solventes que o técnico deveria apresentar para avaliar a redução progressiva na solubilidade do iodo molecular, do tubo 1 para o tubo 4.
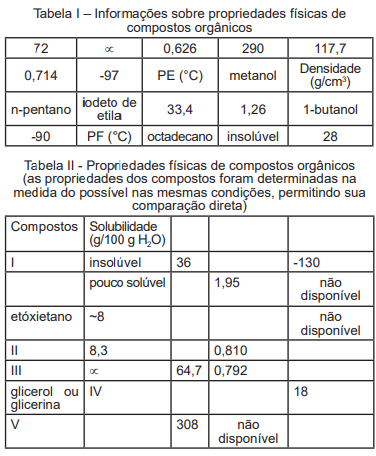 I. Sabendo-se que o composto I tem densidade de
0,626 g/cm3
, a menor densidade da lista de compostos
apresentados, ele certamente representa o n-pentano,
pois tal composto possui também baixo ponto de
ebulição e é insolúvel em água.
II. O composto II representa o n-butanol e seu ponto de
fusão é -97°C.
III. O composto III representa o metanol e sua mais alta
solubilidade em relação ao n-butanol está relacionada a
sua maior interação por ligação de hidrogênio, já que a
molécula é menor.
IV. A glicerina ou glicerol (também conhecida como 1, 2, 3-
propanotriol) tem ponto de ebulição muito alto, 290°C,
devido aos grupos hidroxila, mesmo motivo que deixa
este composto extremamente solúvel em água. Assim
sendo, IV representa o símbolo do infinito.
V. O composto V é sólido à temperatura ambiente de 25°C. Assinale a alternativa correta:
I. Sabendo-se que o composto I tem densidade de
0,626 g/cm3
, a menor densidade da lista de compostos
apresentados, ele certamente representa o n-pentano,
pois tal composto possui também baixo ponto de
ebulição e é insolúvel em água.
II. O composto II representa o n-butanol e seu ponto de
fusão é -97°C.
III. O composto III representa o metanol e sua mais alta
solubilidade em relação ao n-butanol está relacionada a
sua maior interação por ligação de hidrogênio, já que a
molécula é menor.
IV. A glicerina ou glicerol (também conhecida como 1, 2, 3-
propanotriol) tem ponto de ebulição muito alto, 290°C,
devido aos grupos hidroxila, mesmo motivo que deixa
este composto extremamente solúvel em água. Assim
sendo, IV representa o símbolo do infinito.
V. O composto V é sólido à temperatura ambiente de 25°C. Assinale a alternativa correta: 