Questões de Concurso
Sobre sistemas homogêneos: equilíbrio químico na água: ph e poh, indicadores ácido-base, solução tampão. em química
Foram encontradas 590 questões
Indique, dentre os ácidos listados abaixo, aquele cuja base conjugada será a mais forte:
ácido Ka
Acético 1,75 x 10-5
Bórico 6,4 x 10-10
Benzoico 6,3 x 10-5
Lático 1,4 x 10-4
Oxálico 6,5 x 10-2
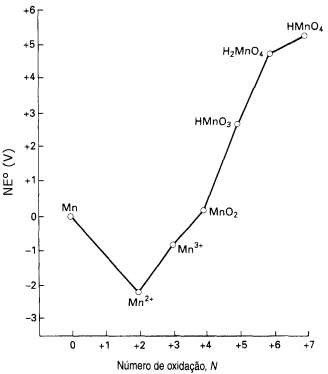
Fonte: SHRIVER, D. F.; ATKINS, P.W, C.H. Química Inorgânica, 3ª edição, Porto Alegre:
A partir da análise do diagrama, pode-se afirmar que a espécie de manganês que se apresenta com o estado de oxidação mais estável em meio ácido, e uma das espécies de manganês que sofre desproporcionamento espontaneamente são, respectivamente,
Dados: Mg = 24,3 g mol -1 ; H = 1,0 g mol -1 ;Cl = 35,5 g mol -1 ; log 2=0,30.
Dado: pKa do ácido acético = 4,74
Em um erlenmeyer é feita a combustão do enxofre; ao produto dessa reação, adiciona-se água e obtém-se uma substância A, que torna vermelho o papel azul de tornassol. Em outro erlenmeyer, faz-se a combustão do magnésio, adiciona-se água e obtém-se uma substância B, que torna azul o papel vermelho de tornassol. Em seguida, promove-se a reação entre A e B, formando uma substância C, em meio aquoso.
O nome da substância C é:
I. O oxigênio pode comportar-se como acelerador do processo eletroquímico de corrosão.
II. A corrosão eletroquímica será tanto mais intensa quanto maior o valor de pH.
III. Na corrosão eletroquímica, o metal se oxida num lugar, o oxidante se reduz em outro e o produto de corrosão se forma em regiões intermediárias, não apresentando características protetoras.
Está(ão) correta(s) a(s) afirmativa(s)
Os sistemas de refrigeração industrial atualmente utilizados nas indústrias de pescado, laticínios, bebidas, frigoríficos e em
outros setores econômicos baseiam-se na capacidade de algumas substâncias químicas, denominadas agentes refrige-
rantes, absorverem significativa quantidade de calor quando passam do estado líquido para o gasoso.
A amônia é um importante agente refrigerante por apresentar diversas vantagens adicionais, como, por exemplo, a de ser
natural e não agredir a camada de ozônio.
Considere 100 mL de uma solução 0,3 mol.L-1
de amônia que foram diluídos por adição de 50 mL de água destilada. Con-
sidere, também, que a constante de ionização da amônia (Kb) a 25°C é 2 x 10-5.

Indicadores ácido-base Cor e pH
fenolftaleína Incolor em pH ≤ 8,3
Rosa-claro em pH entre 8,3 e 10,0
Vermelho em pH ≥ 10,0
Azul de bromotimol amarelo em pH ≤ 6
azul em pH ≥ 7,6
verde em pH entre 6,0 e 7,6
Alaranjado de metila vermelho em pH ≤ 3,1
alaranjado em pH entre 3,1 e 4,4
amarelo em pH ≥ 4,4
A amostra da água da chuva em contato com a solução de:
Dados que as concentrações iniciais do CH 3 COOH CH3COO– são iguais e valem 0,125 mol/L, o pKa = 4,75, e que log 0,98 = -0,007, pode-se afirmar que:
O pH de uma solução 0,006 mol.L -1 deste ácido, que possui Kaigual a 1,5x10-5 , é, aproximadamente, Dado: log 3 = 0,48
N2(g)+ O2(g) →2NO(g)
Essa equação representa uma reação que pode ser classificada como