Questões de Concurso
Sobre sistemas homogêneos: equilíbrio químico na água: ph e poh, indicadores ácido-base, solução tampão. em química
Foram encontradas 590 questões
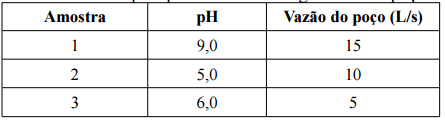
Sendo assim, o pH resultante desta mistura será:
Sabões são sais de sódio ou potássio de ácidos graxos, obtidos pela reação de gorduras e óleos (triglicerídeos) com NaOH, KOH ou Na2CO3. A reação de saponificação é representada a seguir:
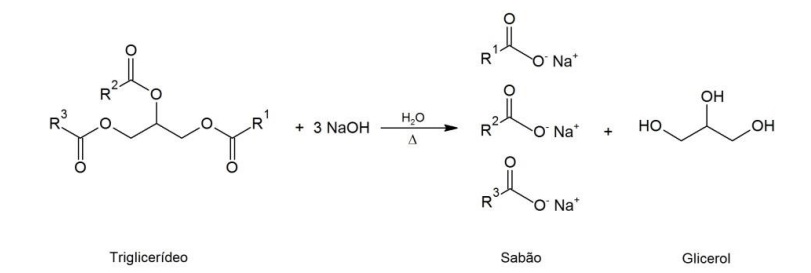
em que R1 , R2 e R3 são cadeias lineares saturadas ou insaturadas, geralmente com doze ou mais átomos de carbono.
Com base nessas informações, considere as seguintes afirmativas:
1. Uma solução aquosa de sabão puro apresenta pH < 7.
2. Adição de ácido forte a uma solução de sabão acarreta precipitação de ácidos graxos.
3. Ca(OH)2 não pode ser usado na obtenção de sabão, pois sais de cálcio de ácidos graxos são insolúveis em água.
4. A obtenção de sabão com Na2CO3 segue a mesma estequiometria que no uso do NaOH.
Assinale a alternativa correta.
O ácido etilenodiamino tetra-acético (EDTA) é usado como “sequestrante” em detergentes, impedindo a precipitação do surfactante (princípio ativo) pelos íons Ca+2, Mg+2 e Fe+3 presentes na água. Em análise química, o EDTA é utilizado como titulante para a determinação de dureza (Ca+2 , Mg+2) de águas, cujo sal dissódico é obtido pela seguinte reação:
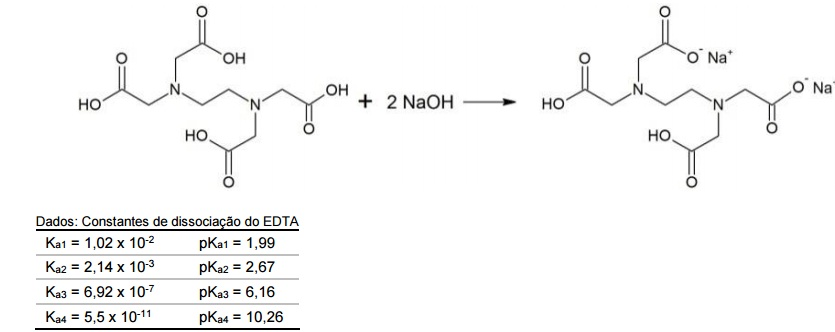
De acordo com a reação de neutralização parcial do EDTA acima apresentada, assinale a alternativa que apresenta o
intervalo de pH no qual é obtido apenas o sal dissódico.
A constante de equilíbrio para a dissociação de um mol ácido monoprótico em 1 litro de água é aproximadamente 1x10-5 à temperatura de 25 ºC. Se a pressão é constante, o valor aproximado da variação na energia de Gibbs (kJ mol-1) para essa reação é de
DADOS:
Constante dos gases ideais = 8,31 J K-1 mol-1 Log10 e = 0,434
Cada curva na figura abaixo representa a mobilidade efetiva de uma espécie química em função do pH, utilizada para se determinar as condições de separação dessas espécies por eletroforese.
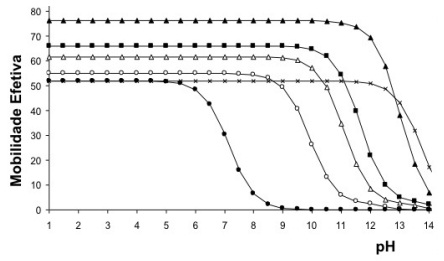
Fonte: PIOVEZAN, Marcel. Desenvolvimento de Metodologias por Eletroforese Capilar para Avaliação de Parâmetros Químicos da Qualidade de Biodiesel, 2010.70 f. Dissertação (Mestrado em Química) – PPGQ-UFSC, Florianópolis - SC. Adaptado.
Assim, o pH que deve ser utilizado para a separação de tais espécies por este experimento de eletroforese
deve ser
O aumento no pH sanguíneo resulta
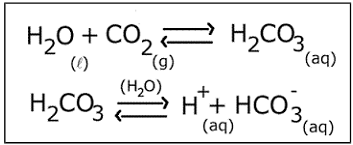
Os óxidos de enxofre e de nitrogênio presentes na atmosfera apresentam caráter ácido, o que leva a um aumento a acidez da água da chuva. A chuva ácida pode causar muitos problemas para as plantas, os animais, o solo, a água, e também para as pessoas. Sobre o tema, analise as afirmações.
I. O pH da água pura é 7,0, mas o dióxido de carbono (CO2 ) presente na atmosfera se dissolve na água, levando à formação do ácido carbônico (H2CO3), e, portanto, o pH da água em equilíbrio com o CO2 atmosférico é de 5,6; ou seja, a chuva é naturalmente ácida.
II. A chuva ácida pode levar à acidificação do solo, porém alguns tipos de solo são capazes de neutralizar pelo menos parcialmente a acidez da chuva devido à presença de calcário (CaCO3). Os solos que não têm calcário são mais suscetíveis à acidificação.
III. O excesso de acidez na chuva pode provocar a acidificação de lagos, principalmente aqueles de pequeno porte. O pH em torno de 5,5 já pode matar larvas, pequenas algas e insetos, prejudicando também os animais que dependem desses organismos para se alimentar.
É correto o que se afirma em:
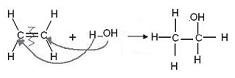
Para que a reação anterior aconteça, o meio reacional deve apresentar a seguinte característica:
Leite I: pH = 7,0 Leite II: pH = 3,0 Leite III: pOH = 11,0
Com base nas informações acima classifique os leites: