Questões de Concurso
Sobre sistemas homogêneos: equilíbrio químico na água: ph e poh, indicadores ácido-base, solução tampão. em química
Foram encontradas 590 questões
A água pura a 25°C em equilíbrio com o ar contendo 390 ppm CO2 possui uma concentração de CO2 dissolvido próximo a 1 x 10–5 mol/L, conforme reação a seguir.
CO2 + H2O 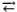 HCO3–
+ H+
HCO3–
+ H+
Considerando que a constante de equilíbrio da reação anterior é igual a 4 x 10–7, qual será o pH da água?
Acerca das teorias ácido-base e tampão são feitas as seguintes afirmações:
I. Segundo a teoria de Arrhenius ácidos e bases são classificados segundo sua capacidade de doar e receber prótons.
II. Quanto maior o valor da constante de ionização de uma base, maior será o valor do pH da solução.
III. Para uma solução de amônia que apresenta concentração dos íons OH- igual a 10-3 mol L-1, o pH é igual a 3.
IV. Um sistema tampão pode ser formado por um ácido forte e sua base conjugada.
V. Dobrando a concentração de ácido e sua base conjugada, que formam a solução tampão, o pH permanece constante, porém o poder tamponante aumenta.
É CORRETO o que se afirma em:
Basicamente, existem dois tipos de pólvora: a pólvora negra e a pólvora sem fumo. Quase todas as armas de fogo modernas usam a pólvora sem fumo. A pólvora negra, classificada como explosivo, é composta por enxofre, carvão e nitrato de potássio. Entre as várias reações que ocorrem na explosão da pólvora negra, a mais simples está descrita pela seguinte equação química:
2KNO3(s) + S(s) + 3C(s) 6 K2S(s) + N2(g) + 3CO2(g).
Com base nessas informações, julgue o item.
O nitrato reage com a água conforme a reação
NO3 – + H2O-> HNO3 + OH– ,
aumentando significativamente o pH da solução formada,
haja vista que o caráter básico do OH–
é mais forte que o
caráter ácido do NO3
–
.
Um técnico de laboratório necessita preparar 500 mL de uma solução tampão de pH = 7,2, em que a soma das concentrações do ácido e de sua base conjugada deva ser 0,100 mol  L-1 . Para isso, o técnico tem à sua disposição as soluções de ácido fosfórico (H3PO4; pKa1 = 2,12; pKa2 = 7,20; e pKa3 = 12,67) de concentração 0,500 mol
L-1 . Para isso, o técnico tem à sua disposição as soluções de ácido fosfórico (H3PO4; pKa1 = 2,12; pKa2 = 7,20; e pKa3 = 12,67) de concentração 0,500 mol  L-1 e NaOH 1,00 mol
L-1 e NaOH 1,00 mol  L-1. Considerando essa situação e as informações apresentadas, julgue o item a seguir, com relação a preparo, aplicação e equilíbrios químicos envolvidos em soluções tampões.
L-1. Considerando essa situação e as informações apresentadas, julgue o item a seguir, com relação a preparo, aplicação e equilíbrios químicos envolvidos em soluções tampões.
Caso a solução tampão mencionada, com pH = 7,2, tenha sido
preparada pelo técnico, é correto afirmar que ela possui uma
capacidade tamponante maior para pequenas adições de base
do que para pequenas adições de ácido.
Um técnico de laboratório necessita preparar 500 mL de uma solução tampão de pH = 7,2, em que a soma das concentrações do ácido e de sua base conjugada deva ser 0,100 mol  L-1 . Para isso, o técnico tem à sua disposição as soluções de ácido fosfórico (H3PO4; pKa1 = 2,12; pKa2 = 7,20; e pKa3 = 12,67) de concentração 0,500 mol
L-1 . Para isso, o técnico tem à sua disposição as soluções de ácido fosfórico (H3PO4; pKa1 = 2,12; pKa2 = 7,20; e pKa3 = 12,67) de concentração 0,500 mol  L-1 e NaOH 1,00 mol
L-1 e NaOH 1,00 mol  L-1. Considerando essa situação e as informações apresentadas, julgue o item a seguir, com relação a preparo, aplicação e equilíbrios químicos envolvidos em soluções tampões.
L-1. Considerando essa situação e as informações apresentadas, julgue o item a seguir, com relação a preparo, aplicação e equilíbrios químicos envolvidos em soluções tampões.
A partir das soluções descritas no texto, é possível o preparo
de uma solução tampão que seja adequada para tamponar um
sistema em pH = 11.
Um técnico de laboratório necessita preparar 500 mL de uma solução tampão de pH = 7,2, em que a soma das concentrações do ácido e de sua base conjugada deva ser 0,100 mol  L-1 . Para isso, o técnico tem à sua disposição as soluções de ácido fosfórico (H3PO4; pKa1 = 2,12; pKa2 = 7,20; e pKa3 = 12,67) de concentração 0,500 mol
L-1 . Para isso, o técnico tem à sua disposição as soluções de ácido fosfórico (H3PO4; pKa1 = 2,12; pKa2 = 7,20; e pKa3 = 12,67) de concentração 0,500 mol  L-1 e NaOH 1,00 mol
L-1 e NaOH 1,00 mol  L-1. Considerando essa situação e as informações apresentadas, julgue o item a seguir, com relação a preparo, aplicação e equilíbrios químicos envolvidos em soluções tampões.
L-1. Considerando essa situação e as informações apresentadas, julgue o item a seguir, com relação a preparo, aplicação e equilíbrios químicos envolvidos em soluções tampões.
Para o preparo da referida solução tampão, serão necessários
100 mL de ácido fosfórico e mais de 70 mL de hidróxido de
sódio.
Um técnico de laboratório necessita preparar 500 mL de uma
solução tampão de pH = 7,2, em que a soma das concentrações do
ácido e de sua base conjugada deva ser 0,100 mol  L-1
. Para isso,
o técnico tem à sua disposição as soluções de ácido fosfórico
(H3PO4; pKa1 = 2,12; pKa2 = 7,20; e pKa3 = 12,67) de concentração
0,500 mol
L-1
. Para isso,
o técnico tem à sua disposição as soluções de ácido fosfórico
(H3PO4; pKa1 = 2,12; pKa2 = 7,20; e pKa3 = 12,67) de concentração
0,500 mol  L-1 e NaOH 1,00 mol
L-1 e NaOH 1,00 mol  L-1. Considerando essa situação
e as informações apresentadas, julgue o item a seguir, com relação
a preparo, aplicação e equilíbrios químicos envolvidos em soluções
tampões.
L-1. Considerando essa situação
e as informações apresentadas, julgue o item a seguir, com relação
a preparo, aplicação e equilíbrios químicos envolvidos em soluções
tampões.
Considere que o tampão tenha sido preparado pelo técnico e
utilizado para tamponar uma reação que produziu
2,0 × 10-2 mol de H+ após 2 horas de reação. Em face dessa
situação, é correto concluir que o tampão continua ativo e
trabalhando dentro da sua faixa de uso.
O coordenador de um laboratório decide utilizar uma técnica eletroquímica para realizar a determinação de chumbo em amostras de efluente. Com base nessa informação, julgue o item seguinte acerca de eletroquímica.
Aferições de pH em soluções são comumente realizadas
utilizando-se um potenciômetro conectado a um eletrodo de
vidro combinado, o qual é composto, resumidamente, por dois
eletrodos de prata-cloreto de prata e pela membrana de vidro.
O coordenador de um laboratório decide utilizar uma técnica eletroquímica para realizar a determinação de chumbo em amostras de efluente. Com base nessa informação, julgue o item seguinte acerca de eletroquímica.
Quando são realizadas medidas com o eletrodo de vidro de
soluções muito ácidas, podem ser observados valores de pH
menores que os reais, que são conhecidos como erros ácidos.
Sua principal origem consiste na saturação da membrana de
vidro por íons H+
.
O gráfico acima mostra os espectros UV-VIS da forma ácida (--) e básica (-) de um ácido monoprótico que apresenta pKa = 3,5 e massa molar = 150,00 g/mol. Com base nessas informações, julgue o item subsequente, acerca da espectroscopia de absorção molecular na região ultravioleta/visível e da determinação dessas espécies por essa técnica espectroscópica.
Em comparação com a espécie básica, a espécie ácida
apresenta espectro mais característico e possui uma banda de
absorção que possibilita o desenvolvimento de um método
mais sensível para a determinação do composto.
O teor de cálcio em uma amostra de água de rejeito industrial foi determinado por volumetria de complexação. Na análise, transferiram-se para um erlenmeyer 5,00 mL da amostra, 5,00 mL de solução tampão, 10,00 mL de uma solução de complexo magnésio-EDTA e uma ponta de espátula de negro de eriocromo. Em seguida, procedeu-se a titulação com 38,0 mL de uma solução padrão de EDTA 0,01 mol/L. Considerando essas informações, julgue o item subsequente, com relação à análise de cálcio na água descrita acima, à volumetria e aos equilíbrios de complexação.
Titulações de complexação com EDTA devem ser realizadas
com pH controlado, preferencialmente pH ácido, para evitar a
formação de hidróxidos dos metais de interesse.
O teor de cálcio em uma amostra de água de rejeito industrial foi determinado por volumetria de complexação. Na análise, transferiram-se para um erlenmeyer 5,00 mL da amostra, 5,00 mL de solução tampão, 10,00 mL de uma solução de complexo magnésio-EDTA e uma ponta de espátula de negro de eriocromo. Em seguida, procedeu-se a titulação com 38,0 mL de uma solução padrão de EDTA 0,01 mol/L. Considerando essas informações, julgue o item subsequente, com relação à análise de cálcio na água descrita acima, à volumetria e aos equilíbrios de complexação.
Sabendo-se que as constantes de formação dos complexos de
Mg2+ e Zn2+ com EDTA são 4,9 × 108
e 3,2 × 1016,
respectivamente, é correto afirmar que o pH mínimo necessário
para a realização da titulação de complexação de Zn2+ é menor
que o do cátion Mg2+.
Uma solução aquosa de um soluto desconhecido é testada com papel tornassol azul e apresenta coloração vermelha. A solução é um condutor fraco comparado com uma solução de NaCl da mesma concentração.
A partir dessas informações, é correto afirmar que o soluto dessa solução é o composto:
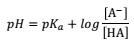
em que, o HA é o ácido e A– é a base conjugada.
Com base no exposto, identifique as afirmativas verdadeiras.
I. O pH da solução será igual ao pKa se a [A– ] for igual a [HA]
II. O pH tende a aumentar se a concentração a [A– ] for maior que [HA]
III. O pH tende a diminuir se a concentração a [A– ] for maior que [HA]
IV.O pH tende a aumentar se a concentração a [A– ] for menor que [HA]
V. O pH tende a diminuir se a concentração a [A– ] for menor que [HA]
Assinale a alternativa correta:
Os indicadores são substâncias naturais ou sintéticas que apresentam cores bem distintas em ácido e básico. Para uma série de indicadores, as seguintes cores e faixa de pH sobre a qual a mudança de cor ocorre são apresentadas na tabela abaixo:

Assinale a alternativa que apresenta a afirmação
CORRETA:
