Questões de Concurso
Sobre transformações químicas e energia em química
Foram encontradas 1.539 questões
NH3 (g) + O2 (g) → NO (g) + H2O (L)
O quadro a seguir apresenta os valores da entalpia-padrão de formação e da entropia molar dos compostos NH3 , NO, O2 e H2O, respectivamente.
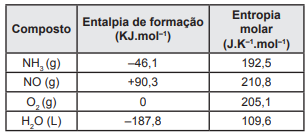 A partir dessas informações, assinale a alternativa
INCORRETA.
A partir dessas informações, assinale a alternativa
INCORRETA.Considere a Tabela de potencial padrão de redução para algumas semicelas abaixo para responder a questão.

A força eletromotriz de uma pilha galvânica formada por duas semicelas nos estados padrões e conectadas por uma ponte salina pode ser estimada a partir da tabela de potenciais de redução.
O módulo da força eletromotriz para uma pilha de Cu e Zn, em V, é
Considere a Tabela de potencial padrão de redução para algumas semicelas abaixo para responder a questão.

Considere a Tabela de potencial padrão de redução para algumas semicelas abaixo para responder a questão.

A respeito das emissões radioativas, julgue o item subsequente.
Em reatores nucleares, a fissão nuclear ocorre com a partição de núcleo atômico pesado e instável em núcleos menores, liberando uma grande quantidade de energia.
A respeito das emissões radioativas, julgue o item subsequente.
A emissão gama apresenta alto poder de penetração, pois possui comprimentos de onda menores, sendo detida por placas de chumbo ou por grossas paredes de concreto.
A respeito das emissões radioativas, julgue o item subsequente.
Partículas alfa apresentam carga elétrica negativa e massa desprezível, enquanto partículas beta são constituídas de dois prótons e dois nêutrons.
A respeito das emissões radioativas, julgue o item subsequente.
Radioatividade é a capacidade que certos átomos
possuem de emitir radiações eletromagnéticas e
partículas de seus núcleos instáveis.
Com relação às aplicações da química e aos processos eletroquímicos, julgue o item que se segue.
A eletricidade pode ser usada para fazer com que ocorram reações de oxirredução não espontâneas; na eletrólise, uma reação é levada à direção não espontânea pela passagem de uma corrente elétrica através da solução.
Com relação às aplicações da química e aos processos eletroquímicos, julgue o item que se segue.
Em uma pilha galvânica, uma reação química é realizada, utilizando‐se corrente elétrica para sua ocorrência, de forma que a voltagem necessária é a subtração entre os potenciais de redução dos reagentes envolvidos.