Questões de Concurso Público PETROQUÍMICA SUAPE 2011 para Técnico de Laboratório Júnior
Foram encontradas 25 questões
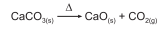
A quantidade máxima, em kg, de óxido de cálcio que se obtém a partir de 200 kg de calcário, contendo 90% em massa de carbonato de cálcio, é


Se, no frasco Erlenmeyer, há 25,00 mL de HCL(aq) 0,200 mol/L, o volume de NaOH(aq) 0,100 mol/L que deve escoar da bureta, em mL, até se atingir o ponto estequiométrico, é
No meio aquoso, esses dois sais reagem instantaneamente, de acordo com a equação balanceada abaixo, e nela se forma um sal muito pouco solúvel.

A quantidade máxima, em gramas, de AgCL sólido (massa molar = 143,5 g/mol e Kps = 10-10 ) que se forma é de, aproximadamente,
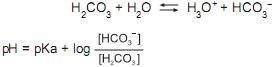
Sobre o equilíbrio de um sistema contendo 100 mL de solução 0,1 mol/L de H 2CO3 e 0,1 mol/L de HCO3– , quando se adiciona(m)
E° Ag+1 /Ago = + 0,80 V
E° Cu+2 /Cuo = + 0,34 V
Sobre a pilha, conclui-se que ela funciona de maneira espontânea e que
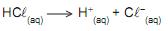
O volume, em mL, de solução aquosa de HCL0,1 mol/L necessário para o preparo de 1 L de solução com pH = 3 é
Na etapa anterior ao forte aquecimento, pesou-se um sulfa- to ferroso hidratado (amostra), e a massa medida foi igual a 2,010 g. Após forte aquecimento em mufla, pesou-se o sulfato ferroso, sem a água de hidratação, e a massa medida foi igual a 1,095 g. De posse desses dados obtidos, conclui-se que o sal hidratado tem fórmula
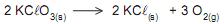
Sendo o volume molar igual 22,4 L/mol (na condição normal de temperatura e pressão), o volume máximo de oxigênio que pode ser obtido a partir da decomposição de 4,00 mol de KCLO3 , com o rendimento percentual de 90%, em L, é
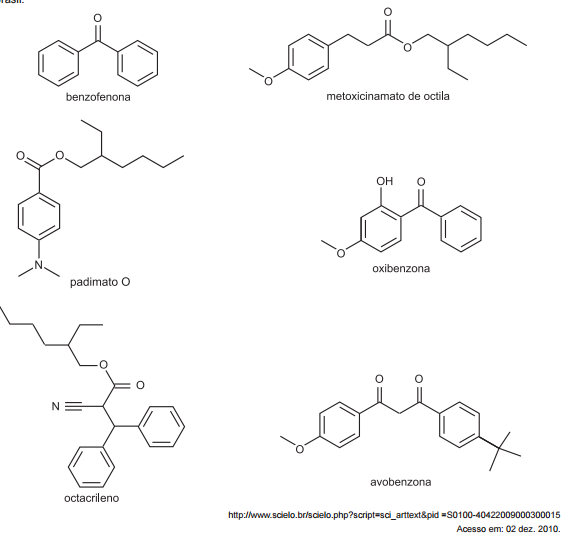
As substâncias representadas abaixo são os principais fotoprotetores presentes nos bloqueadores solares comercializados no Brasil.
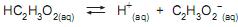
A uma dada temperatura, a constante de equilíbrio (Ka ) é igual a 1 x 10-5 . A concentração da espécie química H+ na solução em equilíbrio é

