Questões de Concurso
Sobre cinética química em química
Foram encontradas 829 questões

A partir dos dados extraídos do gráfico responda aos itens abaixo:
Admitindo-se que, para uma certa reação, o segmento AB representa o nível da entalpia dos reagentes e o segmento FG o nível da entalpia dos produtos, podemos afirmar que:
1. A reação direta é exotérmica.
2. A energia de ativação desse processo é representada pelo segmento FG. 3. O perfil do gráfico permite afirmar que a reação direta representa uma reação de combustão. 4. A variação de entalpia (energia) de reação direta é de ΔH = – 600,00 kJ. 5. A reação inversa é exotérmica.
Assinale a alternativa que indica todas as afirmativas corretas.
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item
As expressões da constante de equilíbrio são muito
importantes porque permitem que os químicos possam
prever a direção e a extensão de uma reação química.
Contudo, uma expressão da constante de equilíbrio não
fornece informações relacionadas à velocidade na qual
o equilíbrio é alcançado.
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item
Catalisador é a substância ou espécie que aumenta a
velocidade de reação, não é consumida e fornece um
mecanismo alternativo de baixa energia de ativação
para a reação. Um catalisador é capaz de afetar a
constante de equilíbrio da reação considerada, por
modificar a velocidade da reação direta, aumentando o
tempo requerido para o estabelecimento do equilíbrio.
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item
A velocidade de uma reação é proporcional às
concentrações dos reagentes, com exceção das reações
de ordem zero, em que as variações de concentração
não produzem nenhum efeito.
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item
A velocidade de uma reação química depende,
essencialmente, do número total de colisões por
unidade de tempo entre as partículas (átomos,
moléculas ou íons) das espécies que participam da
reação, bem como da fração de tais colisões que,
efetivamente, promove a reação química.
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item
A velocidade de uma reação química é calculada pela
multiplicação da variação de concentração de uma
substância pelo intervalo de tempo em que a variação
considerada ocorre, levando em conta o coeficiente
estequiométrico da substância.
Texto 19A1CCC
Além do emprego como combustível, o CH4 pode ser utilizado como insumo para a síntese de diversos compostos químicos. A seguir, destaca-se a sua oxidação parcial para a síntese de metanol, reação esta que pode ser catalisada por um óxido metálico.
CH4 + ½ O2 ⇌ CH3OH
Texto 19A1CCC
Além do emprego como combustível, o CH4 pode ser utilizado como insumo para a síntese de diversos compostos químicos. A seguir, destaca-se a sua oxidação parcial para a síntese de metanol, reação esta que pode ser catalisada por um óxido metálico.
CH4 + ½ O2 ⇌ CH3OH
Considerando:
I) Os dados da questão anterior, II) Que o decaimento radioativo é um processo cinético de primeira ordem que atende à equação: ln N – ln N0 = λ. t III) ln 2 = 0,693.
A constante de decaimento, em ano-1 , para o césio 137 nesse caso seria igual a:
Considerando I) os dados da questão anterior, II) que o decaimento radioativo é um processo cinético de primeira ordem que atende à equação ln N – ln N0 = λ. t e III) que ln 2 = 0,693,
a constante de decaimento, em ano-1 , para o césio 137, nesse caso, seria igual a
Dados: [A]0 = concentração inicial; k= constante de velocidade e t = tempo
O monóxido de nitrogênio, quando liberados pelos automóveis na baixa atmosfera, rapidamente se transforma em dióxido de nitrogênio, que em seguida, irá colaborar na formação do ozônio troposférico, um poluente. Um estudo dessa reação no laboratório revelou que, para que ela se tornasse quatro vezes mais rápida, poderia ser feita a seguinte alteração: manter fixa a concentração de O2 e duplicar a de NO.
Considerando o enunciado acima, atente para as seguintes afirmações:
I. A lei da velocidade dessa reação pode ser dada por: v = k[NO]2 [O2].
II. Essa deve ser uma reação elementar, ou seja,
realizada em apenas uma etapa.
Sobre essas afirmações, é correto diz que
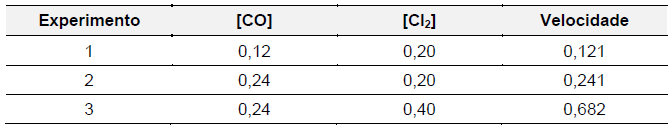
Dado que log 2,8 = 0,45 e log 2 = 0,3, o valor da constante da velocidade desta reação é