Questões de Concurso
Sobre eletroquímica: oxirredução, potenciais padrão de redução, pilha, eletrólise e leis de faraday. em química
Foram encontradas 659 questões
Considere as equações químicas a seguir.
I NH3 + H2O ⇌ NH4+ + OH−
II Cu2+ + 4 NH3 ⇌ [Cu(NH3)4] 2+
III 2 Fe3+ + Sn2+ ⇌ 2 Fe2+ + Sn4+
Ocorre reação de oxirredução apenas na(s) equação(ões)
Quanto ao equilíbrio químico e às características das soluções-tampão e das pilhas, julgue o item.
O termo pilha é empregado para se referir a um
dispositivo constituído de dois eletrodos e um eletrólito,
arranjados de maneira a produzir energia elétrica.
Quando os eletrodos são conectados a um aparelho
elétrico, uma corrente flui pelo circuito, pois o material
de um dos eletrodos oxida-se espontaneamente,
liberando elétrons (ânodo), enquanto o material do
outro eletrodo reduz-se, usando esses elétrons (cátodo).
No que se refere aos processos de corrosão, julgue o item a seguir.
Zinco e magnésio são frequentemente utilizados como
anodos de sacrifício em métodos de proteção galvânica em
ferro, por possuírem maior potencial eletroquímico.
No que se refere aos processos de corrosão, julgue o item a seguir.
A corrosão galvânica consiste na remoção de elétrons do
catodo na presença de um material com potencial de eletrodo
maior.
Sabendo-se que o equivalente eletroquímico da prata é 1,118mg/C, o tempo foi de cerca de:
Um metal que tenha sofrido processo corrosivo por formação de trincas microscópicas ao longo do contorno dos grãos da estrutura metalúrgica, sem alteração significativa nas dimensões da peça, foi vítima de corrosão:
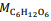 = 180 g/mol e
= 180 g/mol e 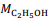 = 46 g/mol.
= 46 g/mol. De acordo com os experimentos de Faraday, a quantidade de produto formado ou de reagente consumido em uma reação eletrolítica é estequiometricamente proporcional à diferença de potencial aplicada entre os eletrodos da célula eletrolítica.
A alternativa que apresenta os coeficientes estequiométricos na ordem a, b, c, d, e, f, g que respeitam a reação de oxirredução a seguir é:
a KMnO4 + b H2S + c HCl
→ d MnCl2 + e S + f H2O + g KCl
[Feº (s) l Fe2+ (aq) (1 mol/ L) II Pb2+(aq) (1mol/L) I Pbº (s) ]
Nessa pilha, a espécie química que atua como oxidante é:
luz e clorofila 6 H2O (I) + 6 CO2 (g) → C6H12O6 (aq) + O2 (g)
Sobre essa reação química, é correto afirmar:
1- Pilha seca comum
( ) Não forma amônia como camada isolante.
2- Pilha alcalina
( ) Sua semirreação catódica é:
2 Ni(OH)3 (s) + 2e → 2 Ni(OH)2 (s) + 2 OH– (aq)
3- Pilha de mercúrio
( ) Emprega sais dissolvidos em solventes não aquosos.
4- Bateria de hidreto metálico
( ) Contém pasta úmida de ZnCl2, NH4Cl e H2O.
5- Bateria de íons lítio
( ) É adequada para dispositivos sensíveis, como aparelhos desurdez, instrumentos científicos e relógios.
Assinale a sequência correta.
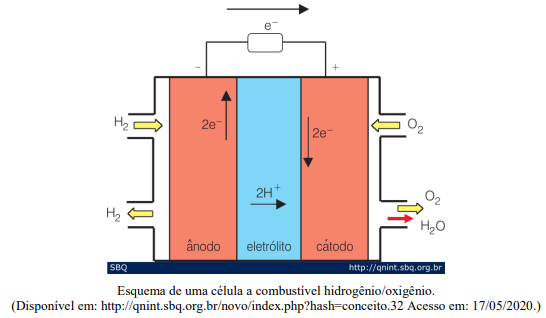
Levando em consideração o funcionamento de uma célula a combustível esquematizado acima, marque V para as afirmativas verdadeiras e F para as falsas.
( ) As células a combustível são células galvânicas nas quais a energia de Gibbs de uma reação química é transformada em energia elétrica (por meio da geração de uma corrente). ( ) A principal semelhança em relação às pilhas e baterias é o fato de, nas células a combustível, os reagentes já estarem armazenados no interior do sistema. ( ) Devido à dificuldade de se armazenar H2, uma alternativa para alimentação das células a combustível é o metanol, que, por sua vez, apresenta a desvantagem de gerar CO e/ou CO2 que são gases de efeito estufa. ( ) O combustível é reduzido de forma contínua no ânodo, enquanto oxigênio é oxidado no cátodo, produzindo água como produto final e energia elétrica.
Assinale a sequência correta.
MnO4 - (aq) + 5Fe2+ (aq) + 8H+ (aq) → Mn2+ (aq) + 5Fe3+ (aq) + 4H2O(l)
Em relação a essa equação química, verifica-se que o
O alumínio já foi o metal mais caro do mundo. Por isso, Napoleão disponibilizava talheres e pratos de alumínio para convidados especiais nos banquetes, enquanto os menos favorecidos usavam de ouro. Em 1855, o norte-americano Charles Martin Hall e o francês Paul Louis Toussaint Héroult descobriram e patentearam quase simultaneamente um processo de obtenção de alumínio a partir do minério bauxita, rico em óxido de alumínio.
KEAN, Sam. A colher que desaparece: Editora Zahar, 2011 (adaptado).O processo ficou conhecido como Hall-Heróult e permitiu o estabelecimento da indústria global do alumínio, cuja obtenção ocorre por meio de:
“A maior ameaça à camada de ozônio no século XXI é o gás hilariante (N2O - óxido nitroso). Segundo o Pnuma (Programa das Nações Unidas para o Meio Ambiente), análises de cientistas de 35 organizações revelaram que o N2O, agora, é o gás mais importante a exaurir o ozônio e o terceiro mais poderoso gás do aquecimento global emitido na atmosfera. Os níveis de N2O aumentaram nas últimas décadas, puxados sobretudo pelos processos de nitrificação e de desnitrificação dos fertilizantes nitrogenados no solo.”
Disponível em: <https://www.terra.com.br/noticias/ciencia/clima/onu-faz-soaroxido-nitroso-a-camada-de-VgnCLD2000000dc6eb0aRCRD.html>. Acesso em: 24 nov. 2020.
O mecanismo de destruição pode ser resumido pelas seguintes equações:
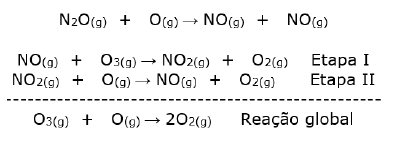
A classificação química do óxido nitroso e a função do NO no mecanismo de destruição do ozônio são, respectivamente:
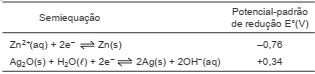
A pilha de zinco e óxido de prata é usada em aparelhos auditivos e relógios de pulso e são menos poluentes do que a de zinco e óxido de mercúrio.
Tendo em vista essas informações e os dados da tabela de
potencial-padrão de redução para as semiequações que
ocorrem nessa pilha, é correto afirmar: