Questões de Vestibular de Química - Equilíbrio Químico
Foram encontradas 630 questões
Em um reservatório contendo água com pH igual a 7, houve um descarte acidental de ácido sulfúrico. Em seguida, foi adicionada uma determinada substância de caráter básico, em quantidade suficiente para neutralizar a acidez.
O gráfico que representa o comportamento do pH durante esse processo é:
Considere a tabela, que apresenta indicadores ácido-base e seus respectivos intervalos de pH de viragem de cor.

Para distinguir uma solução aquosa 0,0001 mol/L de HNO3
(ácido forte) de outra solução aquosa do mesmo ácido
0,1 mol/L, usando somente um desses indicadores, deve-se
escolher o indicador
Deixou-se o NO(g) borbulhar até que fossem acrescidos ao tubo 4 mL desse gás. Após cessar o fluxo de NO(g), o tubo foi mantido imerso na posição vertical, de modo que seu volume pudesse variar, mantendo a pressão em seu interior igual à pressão exterior, mas sem escape de gás. Após certo tempo, o gás dentro do tubo adquire cor castanha, em função da seguinte reação: 2NO(g) + O2(g)
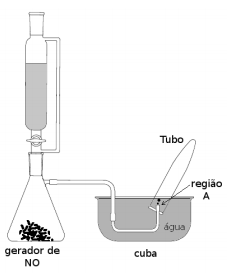
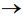 2NO2 (g)
2NO2 (g)
A respeito desse experimento, identifique as afirmativas abaixo como verdadeiras (V) ou falsas (F):
( ) O NO(g) é reagente limitante da reação. ( ) Em relação à condição imediata depois de cessado o fluxo, o volume de gás dentro do tubo irá diminuir após o gás ficar castanho. ( ) Em relação à condição imediata depois de cessado o fluxo, a pressão parcial de N2(g) dentro do tubo irá aumentar após o gás ficar castanho. ( ) O valor de pH da água na região A (dentro do tubo) irá diminuir após o gás se tornar castanho.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
O Princípio de Le Chatelier infere que quando uma perturbação é imposta a um sistema químico em equilíbrio, este irá se deslocar de forma a minimizar tal perturbação.
Disponível em: <brasilescola.com/exercicios-quimica/exercicios-sobre-principio-le-chatelier.htm>
O gráfico apresentado a seguir indica situações referentes à perturbação do equilíbrio químico indicado pela equação
H2(g) + I2(g) 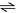 2 HI(g)
2 HI(g)
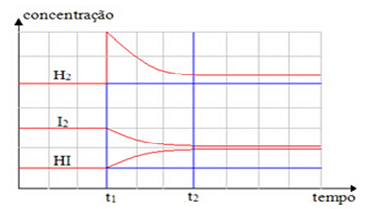
A partir da equação química apresentada e da observação do gráfico, considerando também que a reação é endotérmica
em favor da formação do ácido iodídrico, a dinâmica do equilíbrio favorecerá
I. CO(g) + 1/2 O2
(g)  CO2
(g) ΔHºr1 = – 283,00kJmol–1
CO2
(g) ΔHºr1 = – 283,00kJmol–1
II. CO(g) + H2O(g)  CO2
(g) + H2
(g) ΔHºr2
=?
CO2
(g) + H2
(g) ΔHºr2
=?
Considere as duas reações no estado gasoso e os dados termodinâmicos a 298K.
Dados termodinâmicos:
ΔHºf H2O(g) = –241,82kJmol–1
Sº H2O(g) = 188,83JK–1mol–1
Sº CO(g) = 197,65JK–1mol–1
Sº CO2(g) = 213,74JK–1mol–1
Sº H2(g) = 130,68JK–1mol–1
Sº O2(g) = 205,14JK–1mol–1
Com base nestes dados e nos conhecimentos de química, é correto afirmar:
A adição de um catalisador na reação II, em equilíbrio, favorece o rendimento em H2
.
I. CO(g) + 1/2 O2
(g)  CO2
(g) ΔHºr1 = – 283,00kJmol–1
CO2
(g) ΔHºr1 = – 283,00kJmol–1
II. CO(g) + H2O(g)  CO2
(g) + H2
(g) ΔHºr2
=?
CO2
(g) + H2
(g) ΔHºr2
=?
Considere as duas reações no estado gasoso e os dados termodinâmicos a 298K.
Dados termodinâmicos:
ΔHºf H2O(g) = –241,82kJmol–1
Sº H2O(g) = 188,83JK–1mol–1
Sº CO(g) = 197,65JK–1mol–1
Sº CO2(g) = 213,74JK–1mol–1
Sº H2(g) = 130,68JK–1mol–1
Sº O2(g) = 205,14JK–1mol–1
Com base nestes dados e nos conhecimentos de química, é correto afirmar:
Uma diminuição de pressão favorece a formação de CO2
na reação I.
I. CO(g) + 1/2 O2
(g)  CO2
(g) ΔHºr1 = – 283,00kJmol–1
CO2
(g) ΔHºr1 = – 283,00kJmol–1
II. CO(g) + H2O(g)  CO2
(g) + H2
(g) ΔHºr2
=?
CO2
(g) + H2
(g) ΔHºr2
=?
Considere as duas reações no estado gasoso e os dados termodinâmicos a 298K.
Dados termodinâmicos:
ΔHºf H2O(g) = –241,82kJmol–1
Sº H2O(g) = 188,83JK–1mol–1
Sº CO(g) = 197,65JK–1mol–1
Sº CO2(g) = 213,74JK–1mol–1
Sº H2(g) = 130,68JK–1mol–1
Sº O2(g) = 205,14JK–1mol–1
Com base nestes dados e nos conhecimentos de química, é correto afirmar:
A constante de equilíbrio para a reação II, a 298K, é 1,05.10–5.
INSTRUÇÃO: Para responder à questão, analise o texto e a estrutura a seguir.
Uma das preocupações do Comitê Olímpico Internacional é combater o doping de atletas nas Olimpíadas. Para isso, uma série de análises é realizada rotineiramente com amostras de urina colhidas dos atletas. Nessas análises, uma das substâncias pesquisadas é o THG, que é um esteroide anabolizante. Os métodos de análise são extremamente sensíveis, sendo possível detectar THG em uma concentração tão baixa como 1 ppb (uma parte por bilhão). Isso significa uma concentração em que há um bilionésimo de grama de THG para cada grama de amostra.
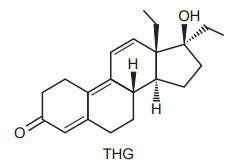
De acordo com as informações acima, assinale a
alternativa correta.

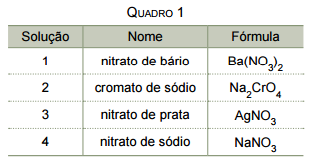
O quadro 2 apresenta o resultado das misturas, de volumes iguais, de cada duas dessas soluções.
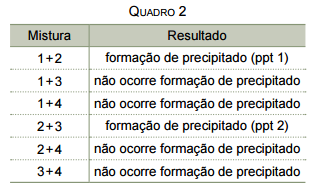
De acordo com essas informações, os precipitados formados, ppt 1 e ppt 2, são, respectivamente,
Os efeitos tóxicos do dióxido de carbono exigem a sua remoção contínua de espaços fechados. A reação entre hidróxido de lítio e de dióxido de carbono é usada para remover o gás de naves espaciais e submarinos. O filtro utilizado nestes equipamentos é basicamente composto de hidróxido lítio. O ar seria direcionado para o filtro através de ventiladores, ao entrar em contato com o hidróxido de lítio presente nos filtros ocorre a reação com o dióxido de carbono existente no ar. A reação global é exotérmica, formando carbonato de lítio sólido e água no estado gasoso.
Disponível em: <http://www.abq.org.br/cbq/2014/trabalhos/14/4463-18723.html>.
Analisando o texto e a reação não balanceada, assinale a alternativa CORRETA.
CO2(g) + LiOH(s) → Li2CO3(s) + H2O(v)
TEXTO 4
Não desejei a morte de minha filha. Ou desejei? Aí é que reside a dúvida, é onde habita o nó que nada nem ninguém no mundo tem o poder de desatar. O inconsciente, desculpe-me a vulgaridade do termo, minha filha, é uma merda. Sendo autônomo, o inconsciente age por si, sem pedir licença nem se revelar. Desejei ou não a morte de minha filha, hein? Você pode responder a essa pergunta? Alguém pode? Eu não posso. Busquei na fonte a resposta e ela não veio. Como minha filha havia feito, busquei nas águas do Cristal a cura imediata para uma dor que parecia infinda. A ferida tinha sido cavada pelas águas, então elas que tratassem de cicatrizá-la. O rio recusou meu corpo, mas não a dor. Nem o aconselhamento. Pediu tempo, apenas. Permaneci plantada no barranco, juntando ao seu caudal minhas lágrimas secas. Disseram que eu tinha enlouquecido, talvez tivesse mesmo. Em diálogo profundo, as águas me fizeram compreender verdades para as quais eu nunca havia me atinado. Todo rio tem seu leito, suas margens, seu limite, toda vez que ele avança além de seu leito original provoca estragos, descalabros. O rio de nossa vida não é diferente. Ele também está sujeito a limitações intransponíveis. Existe você e você; seu campo de visão, a capacidade de administrar o próprio caudal. Tem a hora de abrir e a hora de fechar as comportas. Felicidade ou dor, a escolha é sua, depende do grau de intensidade que você der a cada coisa. Hoje posso dizer que me conheço um pouquinho, mesmo assim, perguntas continuam sem resposta.
(BARROS, Adelice da Silveira. Mesa dos inocentes. Goiânia: Kelps, 2010. p. 23.)
O Texto 4 faz menção a rio, que, muitas vezes é o destino final dos dejetos produzidos pela nossa sociedade. São várias as substâncias que os homens despejam nos rios, causando com isso diversos problemas ambientais. Dentre essas substâncias, podemos encontrar vários compostos inorgânicos, como sais, bases e ácidos. Analise as afirmativas a seguir:
I - A hidrólise de um sal proveniente de ácido forte e uma base fraca em água resultará na redução do pH.
II - Na hidrólise de um sal proveniente de um ácido fraco e base forte, a redução do pOH está em função do deslocamento do equilíbrio (da reação de autoionização da água) para a direita.
III - A adição de NaCl à água provoca a hidrólise desta, por se tratar de um sal proveniente de uma ácido e uma base fracos.
IV - A adição NaCl à água provoca a hidrólise desta, alterando-lhe o equilíbrio iônico.
Em relação às proposições analisadas, assinale a única alternativa cujos itens estão todos corretos:
Em ambientes naturais e na presença de água e gás oxigênio, a pirita, um mineral composto principalmente por dissulfeto de ferro (FeS2), sofre processos de intemperismo, o que envolve transformações químicas que acontecem ao longo do tempo.
Um desses processos pode ser descrito pelas transformações sucessivas, representadas pelas seguintes equações químicas:
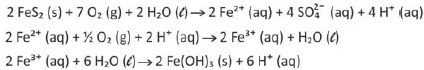
Considerando a equação química que representa a
transformação global desse processo, as lacunas da frase
“No intemperismo sofrido pela pirita, a razão entre as
quantidades de matéria do FeS2(s) e do O2(g) é __________,
e, durante o processo, o pH do solo __________” podem ser
corretamente preenchidas por
Dependendo do pH do solo, os nutrientes nele existentes podem sofrer transformações químicas que dificultam sua absorção pelas plantas. O quadro mostra algumas dessas transformações, em função do pH do solo.
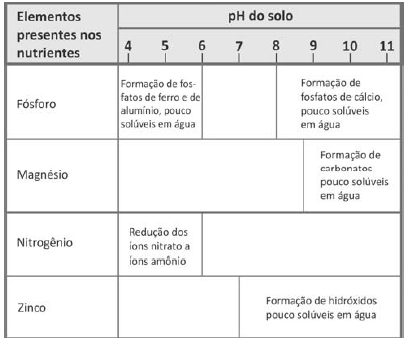
Para que o solo possa fornecer todos os elementos citados
na tabela, o seu pH deverá estar entre
Dados:
Constante de ionização (Ka) do H₂CO₃ = 4 x 10⁻⁷
Constante de ionização (Kb) do NH₃= 2 x 10⁻⁵
Constante de ionização (Kw) do H₂O = 1 x 10⁻¹⁴
Os indicadores ácido base são substâncias cuja cor se altera em uma faixa específica de pH. Atabela a seguir apresenta afaixa de viragem (mudança de cor) de alguns indicadores ácido base.
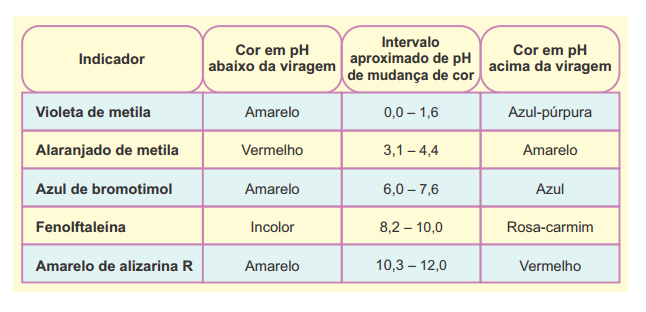
A partir da análise dessa tabela, um técnico executou um procedimento para distinguir algumas soluções.
Para diferenciar uma solução de 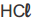 de concentração 1,0 mol.L⁻¹ de uma solução de
de concentração 1,0 mol.L⁻¹ de uma solução de 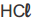 e concentração 0,01 mol.L⁻¹ ele utilizou o indicador X. Para diferenciar uma solução de bicarbonato de sódio (NaHCO₃) de concentração 0,01 mol.L⁻¹ ele utilizou o indicador Y. Para diferenciar uma solução de amoníaco (NH₃) de concentração 1,0 x 10⁻³ mol.L⁻¹ de uma solução de hidróxido de sódio (NaOH) de concentração 0,1 mol.L⁻¹ ele utilizou o indicador Z.
e concentração 0,01 mol.L⁻¹ ele utilizou o indicador X. Para diferenciar uma solução de bicarbonato de sódio (NaHCO₃) de concentração 0,01 mol.L⁻¹ ele utilizou o indicador Y. Para diferenciar uma solução de amoníaco (NH₃) de concentração 1,0 x 10⁻³ mol.L⁻¹ de uma solução de hidróxido de sódio (NaOH) de concentração 0,1 mol.L⁻¹ ele utilizou o indicador Z.
A alternativa que apresenta os indicadores X, Y e Z adequados para cada um dos procedimentos propostos pelo técnico é
