Questões de Vestibular
Sobre equilíbrio químico em química
Foram encontradas 636 questões
O lança-perfume é uma droga inalante consumida principalmente no Carnaval. É constituído por solventes voláteis que, quando inalados, são levados, via corrente sanguínea, para todo o organismo. Por induzir a produção de adrenalina no organismo, a droga acelera a frequência cardíaca, proporcionando sensação de euforia e desinibição, ao mesmo tempo em que confere
perturbações auditivas e visuais, perda de autocontrole e visão confusa. O cloreto de etila
 e o éter dietílico
e o éter dietílico  , componentes principais do lança-perfume, podem ser sintetizados a partir do
, componentes principais do lança-perfume, podem ser sintetizados a partir do  , de acordo com as
, de acordo com asreações a seguir.

Considerando as reações acima e os valores de entalpias padrão de
formação —
 — a 25 ºC, apresentados na tabela, julgue os itens seguintes.
— a 25 ºC, apresentados na tabela, julgue os itens seguintes. 
A infraestrutura precária de alguns locais que sediam
eventos com grande público, como jogos de futebol e shows
musicais, e a falta de educação de pessoas que insistem em urinar
em locais completamente inapropriados, como paredes e viadutos,
têm causado sérios problemas. Além do mau cheiro, o ácido úrico,
presente na urina, penetra pelos poros do concreto e causa corrosão
de estruturas metálicas.
vezes, são negligenciadas. Entre elas, destaca-se o emprego de
revestimentos a base de poliuretano, um polímero altamente
inflamável que pode liberar, em sua combustão, gases tóxicos,
como o CO e o HCN.
Considerando o comportamento ideal para as soluções envolvidas,
julgue os itens subsequentes.
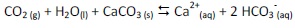
De acordo com essa equação química, dadas as afirmativas seguintes,
I. A reação química é reversível.
II. As espécies químicas presentes no lado dos produtos são chamadas de íons.
III. A equação química não está corretamente balanceada.
IV. A reação química para estar em equilíbrio, a velocidade da reação direta tem que ser igual à velocidade da reação inversa.
verifica-se que estão corretas
Analise os sistemas descritos e assinale a proposição correta:
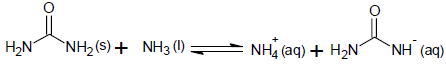
Sobre a natureza das interações entre as espécies envolvidas na reação, o comportamento químico das substâncias reagentes e o átomo de nitrogênio, é correto afirmar:
 Cd + 2 OH− Eº= − 0,81V
Cd + 2 OH− Eº= − 0,81V Ni(OH)2 + OH− Eº= + 0,49 V
Ni(OH)2 + OH− Eº= + 0,49 V 
Cada tipo de planta cresce melhor em solos com faixa específica de pH. Os valores de pH do solo se devem à solução intersticial presente, ou seja, a água presente no solo e seus respectivos solutos. A tabela abaixo fornece a faixa de “pH ótimo” para algumas plantas, o que facilita a produtividade de flores e frutos.

Cada tipo de planta cresce melhor em solos com faixa específica de pH. Os valores de pH do solo se devem à solução intersticial presente, ou seja, a água presente no solo e seus respectivos solutos. A tabela abaixo fornece a faixa de “pH ótimo” para algumas plantas, o que facilita a produtividade de flores e frutos.
CaO(s) + H2O(l)
 Ca(OH)2(aq)
Ca(OH)2(aq) Ca2+(aq) + 2 OH-
(aq)
Ca2+(aq) + 2 OH-
(aq) 
Cada tipo de planta cresce melhor em solos com faixa específica de pH. Os valores de pH do solo se devem à solução intersticial presente, ou seja, a água presente no solo e seus respectivos solutos. A tabela abaixo fornece a faixa de “pH ótimo” para algumas plantas, o que facilita a produtividade de flores e frutos.

Cada tipo de planta cresce melhor em solos com faixa específica de pH. Os valores de pH do solo se devem à solução intersticial presente, ou seja, a água presente no solo e seus respectivos solutos. A tabela abaixo fornece a faixa de “pH ótimo” para algumas plantas, o que facilita a produtividade de flores e frutos.
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO NÚMERO MASSA ATÔMICA
QUÍMICO ATÔMICO
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
S 16 32,0
Cl 17 35,5
Ca 20 40,0
Fe 26 56,0
Cu 29 63,5
Zn 30 65,4
Ag 47 108,0
Sn 50 119,0
Xe 54 131,0
W 74 184,0
2 NO(g) + O2(g)⇽⇾ 2 NO2(g) ΔH <0
Considerando o sistema acima em equilíbrio, é correto afirmar-se que a produção de dióxido de nitrogênio será favorecida quando se
Um sistema químico em equilíbrio, a uma dada temperatura, contém os gases N2, H2 e NH3, como mostra a equação a seguir.
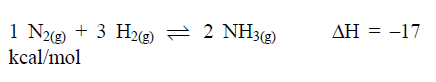
A respeito desse equilíbrio, assinale a afirmativa
incorreta.
Em um reservatório contendo água com pH igual a 7, houve um descarte acidental de ácido sulfúrico. Em seguida, foi adicionada uma determinada substância de caráter básico, em quantidade suficiente para neutralizar a acidez.
O gráfico que representa o comportamento do pH durante esse processo é:
Peter Sorensen, bioquímico dinamarquês, apesar de importantes trabalhos com proteínas, enzimas e aminoácidos, ficou mais conhecido como o criador da escala de pH, usada para medir a acidez de uma solução, que varia de zero a 14. Para preparar uma solução com pH =12 foi adicionado hidróxido de - sódio em 50 mL de água a 25 °C. A quantidade em gramas de soda cáustica necessária é de:
Dados: Na=23u, O=16u, H=1u.
Cores nas lagoas

O listrado multicor que se desenha na areia quando o nível da água baixa nas lagoas do Pantanal da Nhecolândia, conhecidas como salinas, em Mato Grosso do Sul, por muito tempo foi um mistério para observadores. A explicação está numa cianobactéria que sobrevive nas condições dessas águas de pH entre 9 e 11. Na época seca essas bactérias se reproduzem em profusão e pintam as lagoas com substâncias de sua própria decomposição.
(Pesquisa FAPESP, fevereiro de 2012. Adaptado.)
Águas que apresentam pH entre 9 e 11 são



